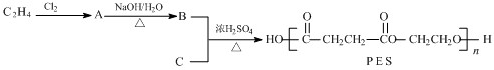
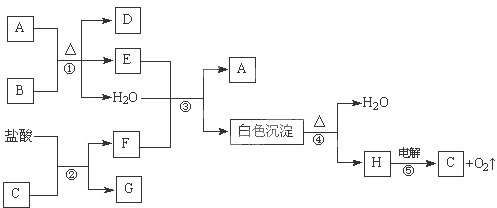
-
从2011年5月1日起,醉酒驾驶将作为危险驾驶罪被追究驾驶人刑事责任.醇脱氢酶和醛脱氢酶可以帮助酒精的代谢,酶是一种蛋白质,由此判断两种酶中可能不含( )
A.H元素
B.C元素
C.Si元素
D.N元素难度: 中等查看答案及解析
-
下列化学事实,可以用胶体的知识解释的现象是( )
A.久置空气中的澄清石灰水变浑浊
B.用激光笔照射鉴别盐水和淀粉溶液
C.浓盐酸与浓氨水靠近时产生浓烟
D.深井水中滴加氯水后颜色变成黄色难度: 中等查看答案及解析
-
下列各组物质互为同分异构体的是( )
A.1H和2H
B.乙烷和丙烷
C.金刚石和石墨
D.正丁烷和异丁烷难度: 中等查看答案及解析
-
下列物质中为含共价键的离子化合物的是( )
A.MgCl2
B.KOH
C.CH2=CH2
D.H2O难度: 中等查看答案及解析
-
下列叙述错误的是( )
A.晶体硅可用于制造太阳能电池
B.氢氟酸保存在棕色玻璃试剂瓶中
C.陶瓷、玻璃、水泥等都是硅酸盐产品
D.硅元素在自然界以SiO2及硅酸盐的形式存在难度: 中等查看答案及解析
-
下列物质之间的转化,不能一步完成的是( )
A.HNO3→NO
B.Fe→FeCl3
C.SiO2→Na2SiO3
D.Al2O3→Al(OH)3难度: 中等查看答案及解析
-
某溶液中存在较多的OHˉ、Clˉ、Na+,该溶液中还可能大量存在的离子是( )
A.Ba2+
B.Mg2+
C.HCO3ˉ
D.NH4+难度: 中等查看答案及解析
-
下列关于氯气的说法错误的是( )
A.密度比空气大
B.有毒
C.黄绿色气体
D.使干燥的有色布条褪色难度: 中等查看答案及解析
-
氮化硅(Si3N4)是一种具有耐高温、耐磨蚀等优异性能的新型陶瓷.工业上可用下列方法制取氮化硅:3SiO2+6C+2N2
Si3N4+6CO.有关该反应说法正确的是( )
A.属于置换反应
B.属于离子反应
C.二氧化硅作氧化剂
D.碳单质作还原剂难度: 中等查看答案及解析
-
2011年是居里夫人获诺贝尔化学奖100周年.居里夫人为了纪念她的祖国波兰,将她发现的一种元素命名为钋(polonium).下列有关钋(
Po)的说法正确的是( )
A.中子数是126
B.质子数是126
C.原子序数是126
D.电子数为126难度: 中等查看答案及解析
-
实验室可利用反应“Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O”制取SO2,下列措施能降低该化学反应速率的是( )
A.适当降低反应温度
B.用铜粉代替铜片
C.加入MnO2作催化剂
D.将浓硫酸改为稀硫酸难度: 中等查看答案及解析
-
判断纯碱中是否混有小苏打,下列实验方案正确的是( )
A.滴加盐酸,观察是否有气体产生
B.溶于水后滴加氯化钙溶液,观察是否有白色沉淀生成
C.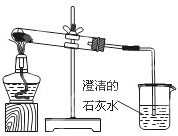
用如图装置进行实验,观察烧杯中是否有白色沉淀
D.溶于水后滴加酚酞试液,观察溶液是否显红色难度: 中等查看答案及解析
-
下列反应中属于放热反应的是( )
A.氧化汞的分解反应
B.铝与氧化铁反应
C.Ba(OH)2•8H2O与NH4Cl反应
D.灼热的炭与CO2反应难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A.铁和稀硝酸反应:Fe+2H+=Fe2++H2↑
B.氯化铁腐蚀印刷线路板:Fe3++Cu=Fe2++Cu2+
C.钠和水反应:2Na+2H2O=2Na++2OH-+H2↑
D.铝和氢氧化钠溶液反应:Al+2OHˉ=AlO2ˉ+H2↑难度: 中等查看答案及解析
-
化学反应的绿色化要求原料物质中所有的原子被安全利用且全部转入期望的产品中.下列符合“化学反应的绿色化学”的是( )
A.制聚乙烯:
B.制硝基苯: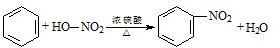
C.制备乙酸乙酯:CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
D.乙醇的催化氧化制乙醛:2CH3CH2OH+O22CH3CHO+2H2O
难度: 中等查看答案及解析
-
下列关于甲烷、乙烯、乙醇、乙酸的说法中,错误的是( )
A.在进行甲烷燃烧实验时,必须先检验其纯度
B.乙烯可以使溴水、酸性高锰酸钾溶液褪色
C.乙醇是重要的有机溶剂,常用来萃取碘水中的碘
D.生活中可以用食醋除去水壶中的水垢难度: 中等查看答案及解析
-
下列实验装置图所示的实验操作,能达到相应实验目的是( )
A.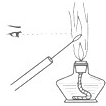
观察K+焰色
B.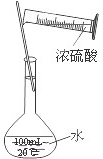
配制稀硫酸
C.
证明氨水易溶于水
D.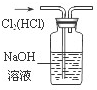
除去Cl2中的HCl难度: 中等查看答案及解析
-
下列化学用语书写正确的是( )
A.乙烯的结构简式:CH2CH2
B.过氧化钠的化学式:NaO2
C.氨分子的电子式:
D.Clˉ离子的结构示意图: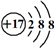
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数,下列说法中正确的是( )
A.0.5mol•L-1Na2CO3溶液中所含Na+数为NA
B.常温常压下,16g臭氧所含氧原子数为NA
C.标准状况下,22.4 L甲烷中含有电子数为NA
D.27g金属铝与足量盐酸反应转移电子数为NA难度: 中等查看答案及解析
-
在下列自然资源的开发利用中,不涉及化学变化的是( )
A.通过石油分馏获得汽油
B.以海带为原料制取碘单质
C.利用海水制取金属镁
D.电解氧化铝获得金属铝难度: 中等查看答案及解析
-
如图为铜锌原电池示意图,下列说法中正确的是( )

A.铜是电池的负极,锌是正极
B.电子由Cu片经导线流向Zn片
C.Cu极附近溶液因产生Cu2+而变蓝
D.电池总反应:Zn+2H+=Zn2++H2↑难度: 中等查看答案及解析
-
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.W与X可形成WX2、WX3两种化合物,则下列说法正确是( )
X Y Z W
A.原子半径:W>Z>X>Y
B.最高价氧化物对应水化物的酸性W>Z
C.气态氢化物的热稳定性:X>Y
D.最高正化合价:Y>Z>X难度: 中等查看答案及解析
-
将足量的铜与一定体积 10mol•L-1的浓硝酸充分反应,得到Cu(NO3)2溶液和NO2、NO混合气体,将集满混合气体的容器倒扣在水中,通入2.24L O2(标准状况)后,所有气体完全被水吸收生成硝酸.发生反应为:4NO2+O2+2H2O=4HNO3;4NO+3O2+2H2O=4HNO3.若向所得Cu(NO3)2溶液中加入5mol•L-1NaOH溶液使Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.40 mL
B.60 mL
C.80 mL
D.100 mL难度: 中等查看答案及解析