-
设计实验方案是科学探究的重要环节,以下化学实验设计中,不能达到实验目的是( )
A. 厨房中用食醋鉴别纯碱和食盐
B. 用稀硫酸除去铜粉中混有的少量铁粉
C. 用稀盐酸检验暴露在空气中的NaOH固体是否变质
D. 用AgNO3溶液鉴别实验室制取二氧化碳的剩余废液中是否存在过量的盐酸
难度: 简单查看答案及解析
-
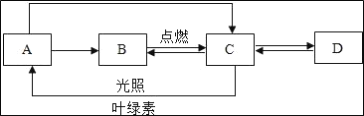
善于梳理化学知识,能使你头脑更聪明.以下有错误的一组( )
化学变化中的能量变化
初中化学中常见的
A
蜡烛燃烧﹣﹣﹣放热反应
碳还原二氧化碳﹣吸热反应
B
三种可燃性气体﹣H2、CO、CH4
构成物质的三种基本微粒﹣分子、原子、离子
化学与安全
化学与能源
C
进入未开发的溶洞探险﹣用火把照明
清理沼气池﹣用火把照明
D
煤、石油、天然气﹣不可再生的化石燃料
风能、地热能、太阳能﹣为充分利用的绿色能源
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列图象能正确反映对应变化关系的是( )
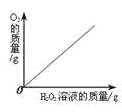
A.向一定量的二氧化锰中加入过氧化氢溶液
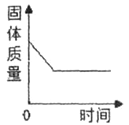
B.将铁钉加入硫酸铜溶液中
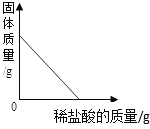
C.向一定量的大理石(杂质不参加反应)中加入足量的稀盐酸
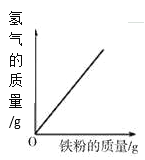
D.向一定质量的稀盐酸中加入足量铁粉
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 大气中二氧化碳含量不断上升,会导致酸雨的形成
B. 把干燥紫色石蕊小花放入盛满干燥的二氧化碳气体的集气瓶中,紫色小花会变红
C. KNO3饱和溶液一定比不饱和溶液溶质质量分数大
D. 焦炭可以通过下列反应还原出铁矿石中的铁:2Fe2O3+3C
4Fe+3CO2↑
难度: 中等查看答案及解析
-
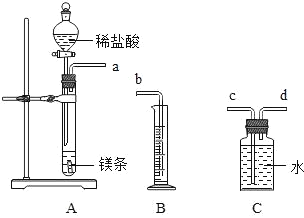
下列四组实验中,不能体现酸的通性的是( )
A.
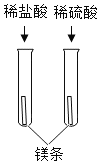 B.
B. 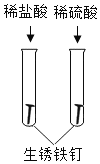
C.
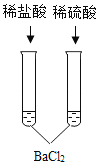 D.
D. 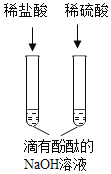
难度: 中等查看答案及解析
-
向盛有10g49%稀硫酸的烧杯中加入5.6克的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法正确的是( )
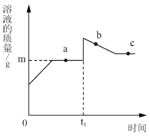
A. 取a点是溶液,加入锌粉,有气体放出
B. b点时,溶液中溶质只有一种
C. c点时,烧杯中固体一定是铜
D. m=12.7
难度: 中等查看答案及解析
-
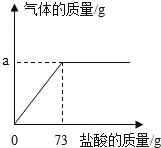
现有盐酸和氯化镁的混合溶液,向其中逐滴滴入氢氧化钠溶液,生成沉淀质量与滴入氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是( )
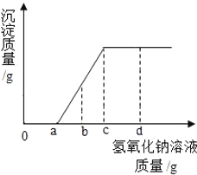
A. 滴加氢氧化钠液质量为a﹣cg时,溶液中发生的反应为:MgC12+2NaOH=2NaCl+Mg(OH)2
B. 滴加氢氧化钠溶液质量至ag时,溶液中溶质质量比原混合溶液中溶质质量大
C. 滴加氢氧化钠溶液质量至bg时,溶液中含三种溶质
D. 滴加氢氧化钠溶液质量至cg时,溶液呈中性
难度: 困难查看答案及解析