-
下列关于古籍中的记载说法不正确的是( )
A. 《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”两个反应互为可逆反应
B. 《天工开物》中“凡石灰,经火焚炼为用”涉及的反应类型是分解反应
C. 《本草纲目》中“以火烧之,紫青烟起,乃真硝石”利用焰色反应区分硝石(KNO3)和朴硝(Na2SO4)
D. 汉朝的《淮南万毕术》《神农本草经》记载“白青(碱式碳酸铜)得铁化为铜”,“石胆能化铁为铜”都是指铜可以采用湿法冶炼。
难度: 简单查看答案及解析
-
阿伏加德罗常数的值为NA.下列说法正确的是( )
A. 16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1 NA
B. 5.6gFe与稀H2SO4完全反应,转移的电子数为0.3NA
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA
D. 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
难度: 中等查看答案及解析
-
下列指定反应的离子方程式正确的是( )
A. CuSO4溶液和氢硫酸反应:Cu2++S2-=CuS↓
B. NaAlO2 溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
C. 向FeBr2溶液中通入等量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
D. 稀硫酸与氢氧化钡溶液反应:H+ + OH-+SO42-+ Ba2+= BaSO4↓ + H2O
难度: 中等查看答案及解析
-
SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O===SO42-+2Fe 2++4H+;
②Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++7H2O。
下列有关说法不正确的是( )
A. SO2发生氧化反应
B. 若有13.44 L SO2(标准状况)参加反应,则最终消耗0.4mol K2Cr2O7
C. 氧化性:SO42- < Fe3+ < Cr2O72-
D. 每0.2 mol K2Cr2O7参加反应,转移电子的数目为1.2NA
难度: 中等查看答案及解析
-
下列实验中,所使用的装置(夹持装置略)、试剂和操作方法有错误的是
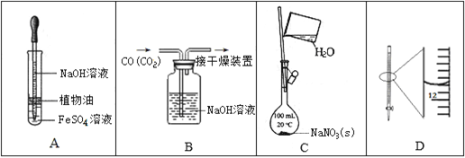
A. 观察Fe(OH)2的生成
B. 除去CO中的CO2
C. 配制一定物质的量浓度的NaNO3溶液
D. 25 mL滴定管读数为11.80 mL
难度: 中等查看答案及解析
-
有以下六种饱和溶液①CaCl2;②Ca(OH)2;③Na2SiO3;④Na2CO3;⑤NaAlO2;分别持续通入CO2,最终不会得到沉淀或析出晶体的是( )
A. ④⑤ B. ③⑤ C. ①④ D. ①②
难度: 中等查看答案及解析
-
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. NaCl
NaHCO3
Na2CO3
B. Cu
CuS
CuCl2
C. Fe2O3
FeCl3(aq)
无水FeCl3
D. MgCO3
MgCl2(aq)
Mg
难度: 中等查看答案及解析
-
下列实验与对应示意图的关系正确的是( )
A
B
C
D
向NaAlO2溶液中逐滴滴加盐酸至过量
向AlCl3溶液中逐滴滴加氨水至过量
向明矾溶液中逐滴滴加
Ba(OH)2溶液至过量
向澄清石灰水中缓缓通入CO2至过量

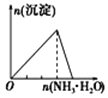
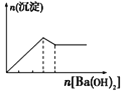
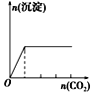
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列有关溶液组成的描述合理的是( )
A. 无色溶液中可能大量存在Al3+、NH4+、Cl-、S2-
B. 弱碱性溶液中可能大量存在Na+、 K+、Cl-、HCO3-
C. pH=1的溶液中可能大量存在Na+、NH4+、SiO32-、I-
D. 0.1 mol·L-1NaAlO2溶液中可能大量存在Na+、H+、 Cl-、SO42-
难度: 中等查看答案及解析
-
现有浓度均为1 mol·L-1的FeCl3、CuCl2、FeCl2的混合溶液100 mL,向该溶液中加入5.6 g铁粉充分反应(溶液的体积变化忽略不计)。下列有关叙述不正确的是( )
A. 反应后的溶液中含有0.2 mol Fe2+和0.1 mol Cu2+
B. 反应后的溶液中含有Fe2+、Cu2+,不含Fe3+
C. 反应后的溶液中Fe2+的浓度增至3 mol·L-1
D. 反应后残留固体为3.2 g
难度: 中等查看答案及解析
-
下列实验方案能达到实验目的的是
实验目的
实验方案
A
证明Mg(OH)2 沉淀可以转化为Fe(OH)3
向2mL1mol/LNaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/LFeCl3
B
比较氯和碳的非金属性强弱
将盐酸滴入碳酸氢钠溶液中
C
配制100mL1.0mol/LCuSO4溶液
将25gCuSO4·5H2O溶于100mL蒸馏水中
D
验证氧化性:Fe3+>I2
将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置,观察下层液体是否变成紫色
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
一定量的铁、铝合金与300mL 2mol/L硝酸完全反应生成3.36LNO(标况)和三价铁盐、铝盐等,再向反应后的溶液中加入3mol/L的NaOH溶液,使铝、铁元素完全沉淀下来,则所加NaOH溶液的体积是( )
A. 450mL B. 150mL C. 200mL D. 无法计算
难度: 中等查看答案及解析
-
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是( )
A. 取a g混合物充分加热,减重b g
B. 取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体
C. 取a g混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b g固体
D. 取a g混合物与足量稀硫酸充分反应,逸出气体直接用碱石灰吸收,增重b g
难度: 中等查看答案及解析
-
下列说法中不正确的有( )
①铝制餐具不宜用来蒸煮或长时间存放酸性、碱性的食物
②Al2O3熔点高,可用于制作耐高温仪器
③SiO2有导电性,可用于制备光导纤维
④二氧化硅既能与氢氟酸反应,又能与烧碱反应,所以它是两性氧化物
⑤金属活动性不同,冶炼方法也有所不同
⑥明矾常作为饮用水的消毒剂
⑦镁铝合金的强度和硬度都比纯铝和纯镁大
⑧除去铜器表面铜绿而不损伤器物,可用稀硝酸
A. ①③⑤⑥ B. ②⑥⑦⑧ C. ③④⑥⑧ D. ④⑤⑦⑧
难度: 中等查看答案及解析
-
含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
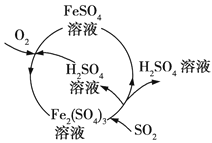
A. 该过程中可得到化工产品H2SO4
B. 该过程中化合价发生改变的元素为Fe和S
C. 该工艺流程是除去煤燃烧时产生的SO2
D. 图中涉及的反应之一为Fe2(SO4)3+SO2 + 2H2O=2FeSO4+2H2SO4
难度: 中等查看答案及解析