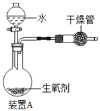
-
下列不利于环境保护的是( )
A. 分类回收生活垃圾,垃圾资源化
B. 过量使用农药化肥,提高粮食产量
C. 预防治理水体污染,保护水资源
D. 加大空气质量监测,改善环境状况
难度: 简单查看答案及解析
-
人们发现建立模型往往需要有一个不断完善,不断修正的过程,经使模型更接近事物的本质。下列原子结构模型建立的过程按时间的顺序正确的是( )
①卢瑟福原子模型 ②汤姆生原子模型 ③道尔顿原子模型 ④玻尔原子模型。
A. ①②③④ B. ③②①④ C. ④③②① D. ③①②④
难度: 中等查看答案及解析
-
下列物质中既含有氧元素的单质,又含有氧元素的化合物的是( )
A. 空气 B. 液氧 C. 高锰酸钾 D. 氧化铜
难度: 中等查看答案及解析
-
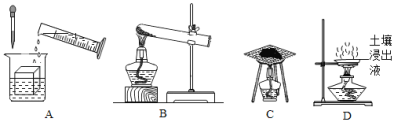
如图是氧气的制取和性质的相关知识网络(反应条件部分省略)。下列说法中不正确的是( )
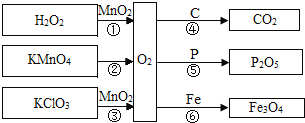
A. 反应④⑤⑥的生成物均为氧化物
B. 反应⑤有大量的白烟产生
C. 反应①②③均属于分解反应
D. C、P、Fe均可以在空气中燃烧
难度: 中等查看答案及解析
-
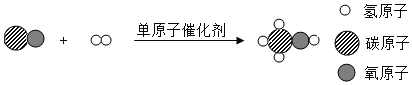
随着计算化学的发展、研究人员通过“晶体结构预测”模型进行演算发现,一定条件下可实现如下反应:2Na+He
Na2He.下列说法正确的是( )
A. 反应物Na和He均由分子构成
B. Na2He中Na化合价为+1价,He为﹣1价
C. Na2He由两个钠元素和一个氦元素组成
D. 该反应为化合反应
难度: 中等查看答案及解析
-
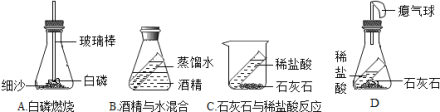
如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。下列实验现象描述,不会出现的是( )
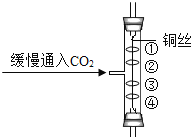
A. ①变红,③不变红 B. ④变红,③不变红
C. ①比④先变红,②、③不变红 D. ④比①先变红,②、③不变红
难度: 简单查看答案及解析
-
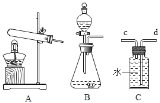
为了测定能使带火星的木条复燃时氧气的最低含量是多少,课外活动小组的同学们将氧气和空气按不同的体积比收集在集气瓶里。收集方法是:在100mL集气瓶里装满水,塞紧胶塞并关闭活塞b,打开活塞a通入氧气,把瓶里的水排入量筒,当量筒内的水达到设定的体积后立即关闭活塞a,然后打开活塞b通入空气,把瓶里的水全部排入量筒。若要收集一瓶含氧气的体积分数约为60%的气体,则通入氧气和空气的体积约是( )
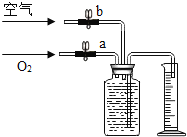
A. 20mL和80mL B. 40mL和60mL
C. 50mL和50mL D. 60mL和40mL
难度: 中等查看答案及解析