-
下列现象的产生与人为排放大气污染物氮氧化物无关的是:
A.光化学烟雾 B.臭氧层空洞 C.酸雨 D.闪电
【解析】闪电是一种自然现象,与氮氧化物无关,答案选D.
难度: 简单查看答案及解析
-
一定条件下硝酸铵受热分解的化学方程式(未配平)为:NH4NO3 - HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为:
A.5∶3 B.5∶4 C.1∶1 D.3∶5
【解析】被氧化化合价升高,即N原子从-3价升高到0价,失去3个电子。被还原,化合价降低,即N原子从+5价降低到0价,得到5个电子。所以根据得失电子守恒可知被氧化与被还原的氮原子数之比为5∶3,即答案是A。
难度: 简单查看答案及解析
-
某溶液中含有NH4+、Mg2+、Fe2+和Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是:
A. 只有NH4+ B.只有 Al3+ C. NH4+和 Al3+ D. Fe2+和NH4+
【解析】在热的强碱性中,NH4+和氢氧化钠反应放出氨气。镁离子和铝离子虽然和氢氧化钠反应被消耗,但加入过量的盐酸后又重新生成。亚铁离子和氢氧化钠反应生成氢氧化亚铁沉淀,但氢氧化亚铁不稳定,可以被氧化生成氢氧化铁沉淀,再加入盐酸,生成铁离子,所以正确的答案是D。
难度: 简单查看答案及解析
-
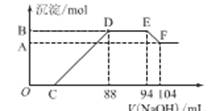
将含amol Na2CO3的溶液逐滴加入到含bmolHCl的溶液中与将含bmolHCl的溶液逐滴加入到含amol Na2CO3的溶液中,正确的描述是:
A. 现象不同,产物种类及物质的量一定相等。
B. 现象相同,产物种类及物质的量有可能相等。
C. 现象不同,产物种类及物质的量不可能相等。
D. 现象不同,产物种类及物质的量有可能相等。
【解析】碳酸钠和盐酸反应,分两步进行,反应式为Na2CO3+HCl=NaHCO3+NaCl、NaHCO3+HCl=NaCl+H2O+CO2↑。若将含amol Na2CO3的溶液逐滴加入到含bmolHCl的溶液中,由于盐酸过量,所以会立即生成CO2气体。若将含bmolHCl的溶液逐滴加入到含amol Na2CO3的溶液中,一开始没有气体生成,只有当碳酸钠全部转化为碳酸氢钠时,再加入盐酸才能生成气体。由于a和b的关系未知,所以选项D是正确的,答案选D。
难度: 简单查看答案及解析
-
将含amol NaOH的溶液逐滴加入到含bmolAlCl3的溶液中与将含bmolAlCl3的溶液逐滴加入到含amol NaOH的溶液中,正确的描述是:
A.现象不同,产物种类及物质的量一定相等。
B. 现象相同,产物种类及物质的量有可能相等。
C. 现象不同,产物种类及物质的量不可能相等。
D. 现象不同,产物种类及物质的量有可能相等。
【解析】若将含amol NaOH的溶液逐滴加入到含bmolAlCl3的溶液中,会立即生成白色沉淀,当氢氧化钠过量时,沉淀再溶解。若将含bmolAlCl3的溶液逐滴加入到含amol NaOH的溶液中,开始氢氧化钠过量,所以不可能生成沉淀,只有当全部转化为NaAlO2时,再加入氯化铝才能产生氢氧化铝沉淀。不论a和b的关系如何,最终的生成物都是相同的,所以正确的答案是A。
难度: 简单查看答案及解析
-
下列有关说法错误的是:
A.利用铝热反应可以冶炼熔点较高的金属
B.用作“钡餐”的物质主要成分是硫酸钡
C.常温下,可以用铁制容器来盛装冷的浓硫酸
D.人造刚玉熔点很高,可用作高级耐火材料,其主要成分是二氧化硅
【解析】刚玉的主要成分是三氧化二铝,D错误。答案是D。
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是:
A.向明矾溶液中加入过量的氢氧化钡溶液:
Al3+ + 2SO42-+2Ba2+ + 4OH-= 2BaSO4↓+ AlO2-+ 2H2O
B. Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-===2Fe2++I2
C. NaHSO3溶液中加入过量的Ba(OH)2溶液:
2HSO3- +Ba2++2OH-===BaSO3↓+2H2O+SO32 -
D. 向含有1molFeBr2溶液中通入标准状况下22.4L的Cl2:2Br-+Cl2 =Br2+2Cl-
【解析】在酸性溶液中,NO3-具有氧化性,且其氧化性大于铁离子的,因此氧化碘离子的是NO3-,而不是铁离子。C中当氢氧化钡过量是亚硫酸钡和氢氧化钠。亚铁离子的还原性强于溴离子的,所以氯气首先氧化亚铁离子,因此正确的答案是A。
难度: 简单查看答案及解析
-
下列各组离子在常温下一定能大量共存的是
A.pH=0的无色溶液中:Cl-、Na+、SO42-、Fe2+
B.在c(H+)=10-2 mol·L-1的溶液中:NH4+、NO3-、K+、Cl-
C.加入铝粉能放出H2的溶液中:Ba2+、NH4+、NO3-、Cl-
D.含有大量Cu2+的溶液中:Al3+、S2-、Br-、Na+
【解析】亚铁离子是浅绿色的,A错误。加入铝粉能放出H2的溶液可以是酸性溶液,也可以是碱性溶液,碱性溶液中NH4+不能大量共存,C不正确。铜离子和硫离子不能大量共存,且硫离子和铝离子也不能大量共存,所以正确的答案是B。
难度: 简单查看答案及解析
-
最近,科学家用一种称为“超酸”的化合物H(CB11H6Cl6)和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-。该反应看起来很陌生,其实在反应类型上可以跟中学化学里某个熟悉的化学反应相类似。该化学反应是:
A.H2O+CH3COOH
H3O++CH3COO-
B.Zn+2HCl = ZnCl2+H2↑
C.CO2+2NH3 = CO(NH2)2+H2O
D.NH3+HCl = NH4Cl
【解析】根据反应的特点可以判断类似于氯化铵的生成,因为氨气获得1个质子生成NH4+,NH4+和氯离子结合生成氯化铵,所以答案是D。
难度: 简单查看答案及解析
-
在检验SO42-的过程中,下列操作中正确的是:
A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在
B.先加入硝酸钡,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有SO42-存在
C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在
D.先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在
【解析】】在检验SO42-时,必须首先排出其他离子的干扰,所以要先加入盐酸,若没有现象,再加入氯化钡溶液来检验。硝酸具有氧化性,因此若含有SO32-,则被氧化生成SO42-,因此无法证明原溶液中是否SO42-,因此正确的答案是C。
难度: 简单查看答案及解析
-
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是:
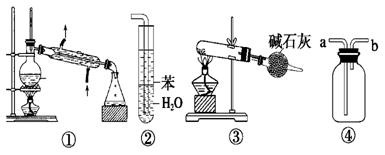
A.装置①常用于分离沸点不同的液体混合物
B.装置②用于吸收氨气,能够防止倒吸
C.以NH4Cl为原料,装置③可制备少量NH3
D.装置④a口进气可收集Cl2、NO等气
【解析】A属于蒸馏,正确。氨气极易溶于水,若导管直接插入水中,容易引起倒吸,导管应插入苯中,B不正确。氯化铵受热分解,生成氨气和氯化氢,但温度降低后,氨气和氯化氢又重新生成氯化铵,C不正确。NO极易被空气氧化,不能通过排气法收集,而是排水法收集,D也不正确。答案是A。
难度: 简单查看答案及解析
-
下列叙述中,正确的是:
A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.晶体中只要有阳离子就会有阴离子
D.电子数相同的阳离子和阴离子一定不具有相同的质子数
【解析】若核外电子排布完全相同,则其化学性质不一定相同,例如钠离子和氟离子等。氢离子、亚铁离子等不具有稀有气体元素原子的核外电子排布。再金属晶体中只有金属阳离子,而没有阴离子。阴离子和阳离子中质子数和电子数一定不相同,所以选项D是正确的,答案选D。
难度: 简单查看答案及解析
-
取四线湿润的蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加69%的硝酸、98.3%的硫酸、新制氯水、浓氨水,四张试纸最后呈现的颜色是:
A.白、红、白、蓝 B.白、黑、白、蓝
C.白、白、白、蓝 D.红、黑、红、蓝
【解析】硝酸具有强氧化性,可以把试纸氧化而褪色。浓硫酸具有脱水性,使试纸炭化。新制氯水具有漂泊性,试纸褪色,氨水溶液显碱性,使石蕊试纸显蓝色。所以正确的答案是B。
难度: 简单查看答案及解析
-
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。下列说法中不正确的是:
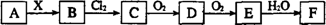
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质:
【解析】若F是硫酸,则E是SO3,D是SO2,C是单质硫,则A可以是Na2S,B是硫化氢,A正确。当X是强碱时,A、B、C、D、E、F可以分别是NH4NO3、NH3、N2、NO、NO2、HNO3,B正确。氯气具有强氧化性,而C又是单质,所以反应一定氧化还原反应。所以选项D是错误的,答案选D。
难度: 简单查看答案及解析
-
下列表达不能通过化合反应得到的是:
A.FeSO4 B.Fe(NO3) 2 C.FeCl2 D.Fe(OH) 2
【解析】铁和硫酸铁化合可以生成硫酸亚铁,同样铁和硝酸铁化合可以生成硝酸亚铁,铁和氯化铁化合生成氯化亚铁,氢氧化亚铁只能通过复分解反应生成,所以答案选D。
难度: 简单查看答案及解析
-
现有CuO和Fe2O3组成的混合物a g,向其中加入2 mol·L—1的硫酸溶液50mL,恰好完全反应。若将a g该混合物在足量H2中加热,使其充分反应,冷却后剩余固体质量:
A.1.6 a g B.(a-1.6) g C.(a-3.2) g D.a g
【解析】硫酸和CuO和Fe2O3反应分别生成硫酸铜和硫酸铁以及水,即硫酸中的氢离子和氧化物中的氧原子结合生成了水,硫酸的物质的量是0.1mol,则氧化物中氧原子的物质的量也是0.1mol,其质量是1.6g,所以混合物中金属原子的质量是(a-1.6)g,所以正确的答案是B。
难度: 简单查看答案及解析
-
Mg、Cu合金8.4g完全溶于浓硝酸中,若反应中硝酸被还原,只产生4480mLNO2和2240mLN2O4,反应后的溶液中加足量的NaOH溶液,生成的沉淀再经灼烧后所得固体质量为:
A.15.2 g, B.11.6g C.13.5g, D.16.6 g
【解析】根据反应过程不难判断,生成的沉淀是氢氧化镁和氢氧化铜,灼烧得到的是氧化镁和氧化铜,因为金属每失去2mol电子,就要结合1mol氧原子。硝酸的还原产物是NO2和N2O4,转移的电子是
,所以根据得失电子守恒可知,金属结合的氧原子是0.2mol,质量是0.2mol×16g/mol=3.2g,所以最终的固体质量是11.6g。即答案是B。
难度: 简单查看答案及解析