-
下列各组物质中全部都属于纯净物的是( )
A.稀有气体、高锰酸钾
B.冰水混合物、红磷点燃后生成的白烟
C.人呼出的气体、食盐水
D.净化后的空气、液态氧难度: 中等查看答案及解析
-
下列词语中,一定包含有化学变化的是( )
A.酒精挥发
B.木已成舟
C.花香四溢
D.火上浇油难度: 中等查看答案及解析
-
下列物质存放在敞口的烧杯中,一段时间后,质量变大且变质的是( )
①浓盐酸 ②浓硫酸 ③烧碱 ④纯碱 ⑤生石灰 ⑥食盐.
A.①⑥
B.③②④⑤
C.②③④
D.③⑤难度: 中等查看答案及解析
-
量筒量取液体时,某同学的操作如下:量筒平放,仰视液体凹液面最低处读数为29mL.倾出一部分液体,又俯视凹液面最低处读数为21mL.这位同学取出液体的体积( )
A.8mL
B.大于8mL
C.小于8mL
D.无法判断难度: 中等查看答案及解析
-
逻辑推理是化学学习常用的思维方法,以下推理正确的是( )
A.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
B.酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸与碱的反应
C.燃烧一般都伴随发光、放热现象,所以有发光、放热的现象就是燃烧
D.氧化物只含有两种元素,所以氧化物中一定有一种元素不是氧元素难度: 中等查看答案及解析
-
下列关于Na、Na+两种粒子的判断,
①核电荷数相同
②核外电子数相等
③电子层结构完全相同
④质量几乎相等
⑤质子数相等
⑥Na+比Na稳定.
其中正确的是( )
A.①④⑤⑥
B.①③⑤⑥
C.①④⑤
D.②③④难度: 中等查看答案及解析
-
根据下列叙述,对其“式”进行判断:①碱式磷酸钙的化学式为Ca4(OH)(PO4)3;②为了方便某些化学计算,质量分数为98%的浓H2SO4可改写为9H2SO4•H2O;③Fe3O4若看做“混合氧化物”时,可改写成FeO•Fe2O3,根据化合价规律和前述写法,则Pb3O4(四氧化三铅)可改写为2PbO•PbO2(Pb的化合价为+2价、+4价).其中错误的是( )
A.仅有①
B.仅有②
C.仅有①③
D.全部难度: 中等查看答案及解析
-
下列除杂质的方法正确( )
物质 杂质 试剂 A CO2 HCl气体 NaOH溶液 B NaNO3溶液 Na2SO4溶液 Ba(OH)2溶液 C 稀盐酸溶液 CuCl2 KOH溶液 D CaCO3 Na2CO3 H2O
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
有五瓶无标签溶液,溶质分别为Na2CO3、AgNO3、BaCl2、HCl、NH4NO3.为鉴别它们,用四支试管分别取其中任意4种,再向这四支试管中分别加入剩下的一种溶液.四个同学的推断分别如下,其中错误的是( )
A.若有三支试管中溶液出现沉淀,则最后加入的是AgNO3溶液
B.若有一支试管中溶液产生气体,则最后加入的是盐酸
C.若有二支试管中溶液产生沉淀,另两支无现象,则最后加入的是BaCl2溶液
D.若四支试管中均无明显现象,则最后加入的是NH4NO3溶液难度: 中等查看答案及解析
-
2010年上海世博会中国馆-“东方之冠”给人强烈的视觉冲击,它的主体结构为四根巨型钢筋混凝上制成的陔心筒.其中钢属于( )

A.金属材料
B.合成材料
C.天然材料
D.复合材料难度: 中等查看答案及解析
-
最近,科学家推出了一种廉价环保的新能源--甲醚,它完全燃烧时发生如下反应:X+3O2
2CO2+3H2O,则X(甲醚)的化学式为( )
A.C3H6O2
B.C2H6O
C.C2H4O
D.CH4O难度: 中等查看答案及解析
-
等质量的甲、乙、丙三种金属,分别与足量的溶质质量分数相同的稀硫酸完全反应后,都生成+2价的硫酸盐,其产生氢气的体积与反应时间的关系如图所示,则下列说法正确的是( )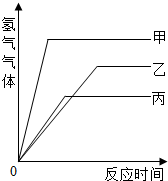
A.三种金属的活动性大小为甲>乙>丙
B.反应时消耗硫酸的质量一定相同
C.三种金属的相对原子质量是甲>乙>丙
D.反应速率最快的是甲,最慢的是乙难度: 中等查看答案及解析
-
如图中E、F为中学常见的两种单质,G、H、I、R为中学常见的四种不同化合物,它们之间有如下关系:由此推知,X可能为下列物质中的( )
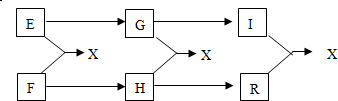
A.CuCl2
B.CaO
C.HCl
D.CO2难度: 中等查看答案及解析
-
在天平左右托盘上,各放一含有20g溶质质量分数为18.25%盐酸的烧杯,将天平调整平衡,然后在左盘的烧杯中加入5g铁,在右盘上的烧杯中加入5g锌,充分反应后,天平将( )
A.仍然平衡
B.向右盘倾斜
C.向左盘倾斜
D.无法判断难度: 中等查看答案及解析
-
某同学预配制溶质质量分数为8%的食盐水80克,在用托盘天平称量时,他把食盐和砝码的位置放颠倒了(1克以下用游码),则实际上他所配制的食盐水的溶质质量分数为( )
A.8.5%
B.7%
C.14%
D.8%难度: 中等查看答案及解析
-
在一定温度下,某固态溶质(不含结晶水)的水溶液甲,经历如下变化:溶液甲
溶液乙
溶液丙,下列结论正确的是( )
A.溶液甲可能是饱和溶液
B.溶液乙和溶液丙中的溶质质量分数不可能相等
C.溶液乙一定是不饱和溶液
D.溶液丙若再蒸发5g水,析出的晶体可能大于2g难度: 中等查看答案及解析