-
关于钠的叙述中,正确的是( )
A. 钠是银白色金属,硬度很大
B. 将金属钠放在坩埚里用酒精灯加热,金属钠剧烈燃烧,产生黄色火焰,生成淡黄色固体氧化钠
C. 金属钠在空气中燃烧,生成过氧化钠
D. 金属钠的熔点很高
难度: 中等查看答案及解析
-
用铝箔包裹0.1mol金属钠,用针在铝箔上扎一些小孔,用镊子夹住,放入水中,待完全反应后,收集到的气体在标准状况下的体积为
A. 等于1.12L B. 等于0.56L C. 大于1.12L D. 小于1.12L
难度: 中等查看答案及解析
-
下列各组物质相互反应后,没有碱生成的是 ( )
A. Na2O2溶于水 B. 红热的铁和水蒸气
C. 金属钠投入水中 D. Na2O投入水中
难度: 中等查看答案及解析
-
离子方程式BaCO3+2H+===CO2↑+H2O+Ba2+中的H+不能代表的物质是( )
①HCl ②H2SO4 ③HNO3 ④NaHSO4 ⑤CH3COOH
A. ①③ B. ①④⑤
C. ②④⑤ D. ①⑤
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A. 钠和冷水反应 Na+2H2O=Na++2OH-+H2↑
B. 金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-+H2↑
C. 金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑
D. 铁跟稀硫酸反应:Fe+2H+=Fe3++H2↑
难度: 中等查看答案及解析
-
日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是
A. 铜铸塑像上出现铜绿[Cu2(OH )2CO3] B. 铁制菜刀生锈
C. 大理石雕像被酸雨腐蚀毁坏 D. 铝锅表面生成致密的氧化膜
难度: 简单查看答案及解析
-
地壳中含量最多的金属元素和非金属元素组成的化合物的化学式是( )
A. CuO B. Al2O3 C. Fe2O3 D. SiO2
难度: 简单查看答案及解析
-
关于Na2CO3和NaHCO3性质的说法正确的是( )
A. 在水中的溶解性:NaHCO3>Na2CO3 B. 热稳定性:NaHCO3<Na2CO3
C. 与酸反应的速率:NaHCO3<Na2CO3 D. 只可能让NaHCO3转化成Na2CO3
难度: 中等查看答案及解析
-
铝、氧化铝、氢氧化铝和可溶性铝盐与过量强碱溶液的反应,其生成物有一定的规律,下列说法中正确的是
A.都有H2O生成 B.都有H2生成
C.都有AlO2-生成 D.都有Al3+生成
难度: 中等查看答案及解析
-
向物质的量浓度均为1 mol·L-1的AlCl3和盐酸的混合溶液中逐滴滴入NaOH溶液,下图[n表示Al(OH)3的物质的量、V表示NaOH溶液的体积]能正确表示这个反应过程的是( )
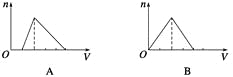
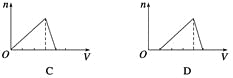
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
能与Fe3+反应,且能证明Fe3+具有氧化性的是①SCN-②Fe ③Fe2+④Cu ⑤Zn ⑥OH-
A. ①②③ B. ②④⑤ C. ①③⑥ D. ①②⑤
难度: 中等查看答案及解析
-
在反应H2S+H2SO4(浓)=S↓+SO2↑+2H2O中,若有32g硫生成则转移电子的物质的量为
A. 6mol B. 2mol C. 3mol D. 4mol
难度: 中等查看答案及解析
-
现有下列几个离子反应:
① Cr2O
+14H++6Cl-===2Cr3++3Cl2↑+7H2O
② 2Fe2++Br2===2Fe3++2Br- ③ 2Br-+Cl2=== Br2+2Cl-
④ 2Fe3++SO2+2H2O===2Fe2++SO
+4H+
下列有关性质的比较中正确的是( )。
A. 氧化性:Cr2O
>Cl2>Fe3+ B. 氧化性:Cl2>Br2>Cr2O
C. 还原性:SO2<Fe2+<Br- D. 还原性:Cl->Cr3+>Fe2+
难度: 中等查看答案及解析
-
在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
A. Fe3+、K+、Cl-、MnO4- B. Ag+、Na+、NO3-、Cl-
C. Zn2+、Al3+、SO42-、Cl- D. Ba2+、NH4+、Cl-、HCO3-
难度: 简单查看答案及解析
-
下列说法正确的是
A.绿色食品是不含任何化学物质的食品
B.灼烧某物质时,用眼直接观察到火焰呈黄色,则可判断该物质不含钾元素
C.向新制的FeSO4溶液中滴入适量的NaOH溶液,放置片刻,整个反应过程的颜色变化是:浅绿色溶液→白色沉淀→灰绿色沉淀→红褐色沉淀
D.称取等质量的两份铝粉,分别加入过量的稀盐酸和过量的NaOH溶液.则放出氢气的体积(同温同压下)不相等
难度: 中等查看答案及解析

