-
下列粒子半径的比较中,正确的是( )
A.Na+>Na
B.Cl->Cl
C.Ca2+>Cl-
D.Mg>Na难度: 中等查看答案及解析
-
下列有关苯酚的实验事实中,能说明侧链对苯环性质有影响的是( )
A.苯酚与浓溴水反应生成三溴苯酚
B.苯酚能和NaOH溶液反应
C.苯酚燃烧产生带浓烟的火焰
D.1mol苯酚与3mol H2发生加成反应难度: 中等查看答案及解析
-
1,5-戊二醛(简称GA),是一种重要的饱和直链二元醛.2%的GA溶液具有广谱、高效、无刺激性、无腐蚀等特点,对禽流感、猪流感等疾病有良好的防治作用.根据上述信息,判断下列说法正确的是( )
A.戊二醛分子式是C5H10O2,符合此分子式的二元醛有4种
B.戊二醛不能在加热条件下和新制的氢氧化铜悬浊液反应
C.戊二醛不能使酸性高锰酸钾溶液褪色
D.2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用难度: 中等查看答案及解析
-
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是( )
A.蒸馏可用于分离提纯液态有机混合物
B.燃烧法是研究确定有机物成分的一种有效方法
C.核磁共振氢普通常用于分析有机物的相对分子质量
D.对有机物分子红外光谱图的研究有助于确定有机物分子中的基团难度: 中等查看答案及解析
-
2010年下半年,我国接连发生多起煤矿爆炸事故,造成重大人员伤亡和财产损失.煤矿发生爆炸事故的元凶是煤矿坑道气中含有的甲烷.下列关于甲烷的叙述中错误的是( )
A.“抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸
B.甲烷分子是一种呈正四面体型的分子
C.甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业
D.甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子难度: 中等查看答案及解析
-
下列化合物中,含有离子键和非极性共价键的是( )
A.H2O2
B.K2O2
C.CaCl2
D.FeCl2难度: 中等查看答案及解析
-
以下分子或离子的结构为正四面体构型的是( )
①CH4 ②③CH3Cl ④P4 ⑤H2S.
A.①②③
B.①②④
C.①②⑤
D.①④⑤难度: 中等查看答案及解析
-
固体乙醇晶体中不存在的作用力是( )
A.极性键
B.非极性键
C.离子键
D.氢键难度: 中等查看答案及解析
-
与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的化合物是( )
A.MgBr2
B.Na2S
C.KCl
D.K2S难度: 中等查看答案及解析
-
下列属于酚类化合物的是( )
A.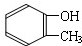
B.
C.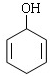
D.
难度: 中等查看答案及解析
-
合成结构简式为
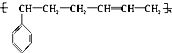 的高聚物,其单体应是( )
的高聚物,其单体应是( )
①苯乙烯 ②丁烯 ③13-丁二烯 ④丙炔 ⑤苯丙烯.
A.①②
B.④⑤
C.③⑤
D.①③难度: 中等查看答案及解析
-
下列分子式只能表示一种物质的是( )
A.C3H4Cl2
B.C3H8
C.C2H6O
D.C3H6难度: 中等查看答案及解析
-
下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是( )
A.CH3Cl
B.
C.
D.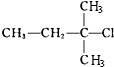
难度: 中等查看答案及解析
-
物质的下列性质不能用键能来解释的是( )
A.氮气的化学性质没有氯气活泼
B.HF比HCl稳定
C.金刚石的熔点比晶体硅高
D.常温下溴呈液态,碘呈固态难度: 中等查看答案及解析
-
HgCl2的稀溶液可用作手术刀的消毒剂,已知HgCl2的熔点是277℃,熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力,则下列关于HgCl2的叙述中正确的是( )
①HgCl2属于共价化合物
②HgCl2属于离子化合物
③HgCl2属于非电解质
④HgCl2属于弱电解质.
A.①③
B.①④
C.②③
D.②④难度: 中等查看答案及解析
-
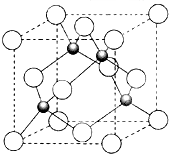
如图,在氯化钠晶体中,与每个Na+等距离且最近的几个Cl-所围成的空间几何构型为( )
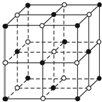
A.十二面体
B.正八面体
C.正六面体
D.正四面体难度: 中等查看答案及解析
-
绿色化学提倡化工生产应提高原子利用率.原子利用率表示目标产物的质量与生成物总质量之比.在下列制备环氧乙烷反应中,原子利用率最高的是( )
A.CH2=CH2+(过氧乙酸)→
+CH3COOH
B.CH2=CH2++O2→+CaCl2+H2O
C.2CH2=CH2++O22
D.3+HOCH2CH2-O-CH2CH2OH+2H2O
难度: 中等查看答案及解析
-
下列各化合物的命名中正确的是( )
A.CH2=CH-CH=CH2 1,3-二丁烯
B.CH3-O-CH3 乙醚
C.3-丁醇
D.2-甲基丁烷
难度: 中等查看答案及解析
-
下列各对物质中,互为同系物的是( )
A.CH3-CH=CH2与
B.OH与
CH2OH
C.甲苯和二甲苯
D.CH2═CH-CH═CH2和CH3-CH2-CH2-C≡CH难度: 中等查看答案及解析
-
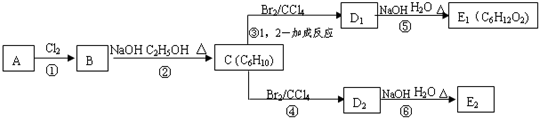
某种烃与H2 1:1加成后的产物如图所示,该烃的结构式可能有则该烯烃的结构( )
A.2种
B.3种
C.4种
D.6种难度: 中等查看答案及解析
-
下列说法正确的是( )
A.用乙醇或CCl4提取碘水中的碘单质
B.NaCl和SiC晶体熔化时,克服粒子间作用力类型相同
C.24Mg32S晶体中电子总数与中子总数之比为1:1
D.H2S与SiF4分子中各原子最外层都满足8电子结构难度: 中等查看答案及解析
-
有机物中碳原子和氢原子个数比为3:4,不能与溴水反应却能使KMnO4酸性溶液褪色.其蒸汽密度是相同状况下甲烷密度的7.5倍.在铁存在时与溴反应,能生成两种一溴代物,该有机物可能是( )
A.CH≡C-CH3
B.CH2=CHCH3
C.CH3C2H5
D.CH3难度: 中等查看答案及解析
-
由乙烯和乙醇蒸气组成的混和气体中,若碳元素的质量百分含量为60%,则氧元素的质量百分含量为( )
A.15.6%
B.26.7%
C.30%
D.无法确定难度: 中等查看答案及解析
-
通常情况下,原子核外p能级、d能级等原子轨道上电子排布为“全空”、“半满”、“全满”的时候一般更加稳定,称为洪特规则的特例.下列事实能作为这个规则证据的是C( )
A.元素氦(He)的第一电离能远大于元素氢(H)的第一电离能
B.26Fe2+容易失电子转变成26Fe3+,表现出较强的还原性
C.基态铜(Cu)原子的电子排布式为[Ar]3d104s1而不是[Ar]3d94s2
D.某种激发态碳(C)原子排布式为1s22s12p3而不是1s22s22p2难度: 中等查看答案及解析
-
下列各组表述中,两个微粒一定不属于同种元素原子的是( )
A.3p能级有一个空轨道的基态原子和核外电子排布为1s22s22p63s23p2的原子
B.M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p63d64s2的原子
C.最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p5的原子
D.2p能级有一个未成对电子的基态原子和原子的价电子排布为2s22p5的原子难度: 中等查看答案及解析

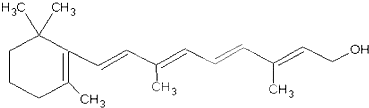
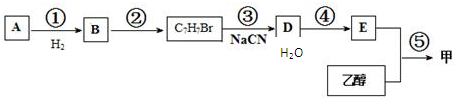
 ,请写出设计合成实验时所涉及的有机反应类型:______.
,请写出设计合成实验时所涉及的有机反应类型:______.