-
1,5-戊二醛(简称GA),是一种重要的饱和直链二元醛.2%的GA溶液具有广谱、高效、无刺激性、无腐蚀等特点,对禽流感、猪流感等疾病有良好的防治作用.根据上述信息,判断下列说法正确的是( )
A.戊二醛分子式是C5H10O2,符合此分子式的二元醛有4种
B.戊二醛不能在加热条件下和新制的氢氧化铜悬浊液反应
C.戊二醛不能使酸性高锰酸钾溶液褪色
D.2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用高二化学选择题中等难度题查看答案及解析
-
1,5-戊二醛(简称GA),是一种重要的饱和直链二元醛。2%的GA溶液具有广谱、高效、无刺激、无腐蚀等特点,对禽流感、口蹄疫、猪瘟等疾病有良好的防治作用。根据上述信息,判断下列说法中正确的是 ( )
A、戊二醛分子式为C5H10O2,符合此分子式的二元醛有4种
B、戊二醛不能在加热条件下和新制备的氢氧化铜反应
C.戊二醛不能使酸性KMnO4溶液褪色
D.对有机物分子红外光谱图的研究有助于确定有机物分子中的基团
高二化学选择题困难题查看答案及解析
-
1,5-戊二醛(简称GA),是一种重要的饱和直链二元醛。2%的GA溶液具有广谱、高效、无刺激、无腐蚀等特点,对禽流感、口蹄疫、猪瘟等疾病有良好的防治作用。根据上述信息,判断下列说法中正确的是( )
A.戊二醛分子式为C5H10O2,符合此分子式的二元醛有4种
B.戊二醛不能在加热条件下和新制备的氢氧化铜反应
C.戊二醛不能使酸性KMnO4溶液褪色
D.2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用
高二化学选择题简单题查看答案及解析
-
1,5-戊二醛(简称GA),是一种重要的饱和直链二元醛。2%的GA溶液具有广谱、高效、无刺激、无腐蚀等特点,对禽流感、口蹄疫、猪瘟等疾病有良好的防治作用。根据上述信息,判断下列说法中正确的是
A、戊二醛分子式为C5H10O2,符合此分子式的二元醛有4种
B、戊二醛不能在加热条件下和新制备的氢氧化铜反应
C.戊二醛不能使酸性KMnO4溶液褪色
D.2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用
高二化学选择题简单题查看答案及解析
-
1,5-戊二醛(简称GA)是一种重要的饱和直链二元醛。2%的GA溶液对禽流感、口蹄疫等疾病有良好的防治作用。根据上述信息,判断下列说法中正确的是 ( )
A.戊二醛的分子式为C5H8O2,符合此分子式的二元醛有5种
B.1mol的戊二醛与足量的银氨溶液反应,最多可得2mol单质银
C.戊二醛不能使酸性高锰酸钾溶液褪色
D.戊二醛经催化氧化可以得到的戊二酸有4种同分异构体
高二化学选择题简单题查看答案及解析
-
1,5-戊二醛(简称GA)是一种重要的饱和直链二元醛。2%的GA溶液对禽流感、口蹄疫等疾病有良好的防治作用。根据上述信息,判断下列说法中正确的是 ( )
A.戊二醛的分子式为C5H8O2,符合此分子式的二元醛有5种
B.1mol的戊二醛与足量的银氨溶液反应,最多可得2mol单质银
C.戊二醛不能使酸性高锰酸钾溶液褪色
D.戊二醛经催化氧化可以得到的戊二酸有4种同分异构体
高二化学选择题简单题查看答案及解析
-
(2014•南昌模拟)ClO2为一种黄绿色气体,是目前国际上公认的高效,广谱,快速安全的杀菌剂.制备ClO2的新工艺是电解法.
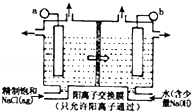
(1)如图表示用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,写出阳极ClO2产生的电极方程式: ;图中b电极为 ;(填“阳极”或“阴极”)
(2)电解一段时间,当阴极产生标准状况下气体112ml时,停止电解,则通过阳离子交换膜的阳离子物质的量为 mol,阴极区pH (填“变大”、“变小”或“不变”)
(3)ClO2对污水中Fe2+,Mn2+,S2﹣,CN﹣等有明显去除效果,某工厂中污水含CN﹣(a mg/L),现将ClO2把CN﹣氧化成两种无毒气体,写出该反应的离子方程式: .
高二化学填空题困难题查看答案及解析
-
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂,目前已开发出用电解法制取ClO2的新工艺.
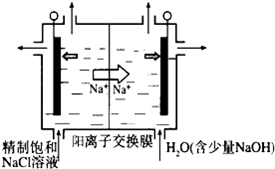
(1)①如图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极产生ClO2的电极反应式:__________________.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为____mol;用平衡移动原理解释阴极区pH增大的原因___________。
(2)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.某工厂污水中含CN-amg/L,现用ClO2将CN-氧化,只生成两种气体,其离子反应方程式为______;处理100m3这种污水,至少需要ClO2______mol.
(3)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-。电池工作时正极反应式为_________________。
高二化学填空题困难题查看答案及解析
-
ClO2为一种黄绿色气体,是目前国际上公认的高效、广谱、快速安全的杀菌剂,制备ClO2的新工艺是电解法。

(1)如图表示用石墨做电极,在一定条件下电解饱和食盐水制取ClO2,写出阳极产生ClO2的电极方程式:__________________________________;图中b电极为_____________(填“阳极”或“阴极”)。
(2)电解一段时间,当阴极产生标准状况下气体112 mL时,停止电解,则通过阳离子交换膜的阳离子物质的量为________mol,阴极区pH________(填“变大”“变小”或“不变”)。
(3)ClO2对污水中Fe2+、Mn2+、S2-、CN-等有明显去除效果,某工厂中污水含CN-(a mol·L-1),现将ClO2把CN-氧化成两种无毒气体,写出该反应的离子方程式:_____________________。
高二化学填空题困难题查看答案及解析
-
(10分)FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是 。FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3。
①若酸性FeCl2 废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:_____ClO3-+______Fe2++______ =_____Cl-+_____Fe3++______
(3)FeCl3 在溶液中分三步水解:Fe3++H2O
Fe(OH)2++H+ K1
Fe(OH)2++H2O
Fe(OH)2++H+ K2 Fe(OH)++H2O
Fe(OH)3+H+ K3
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O
Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
高二化学填空题困难题查看答案及解析