-
地壳中含量最多的元素是
A.H B.O C.Si D.Al
难度: 简单查看答案及解析
-
属于溶液的是
A.豆浆 B.牛奶 C.矿泉水 D.蒸馏水
难度: 简单查看答案及解析
-
菠菜中含铁质,对缺铁性贫血有较好的辅助治疗作用。这里的铁质指的是
A.元素 B.分子 C.原子 D.单质
难度: 简单查看答案及解析
-
测得常见果汁的近似pH,其中酸性最强的是
A.柿子pH=8.5 B.菠萝pH=5.1 C.苹果pH=4.1 D.杨梅pH=2.5
难度: 简单查看答案及解析
-
关于“水”参与的变化,属于化学变化的是
A.配食盐水 B.小河流淌 C.冰川融化 D.酸雨形成
难度: 简单查看答案及解析
-
表示两个氢分子的是
A.2H B.2H2 C.H D.H2
难度: 简单查看答案及解析
-
有关物质用途说法错误的是
A.草木灰可用作氮肥 B.氧气可供给呼吸
C.干冰可用于人工降雨 D.金刚石可切割玻璃
难度: 简单查看答案及解析
-
关于甲烷的说法正确的是
A.具有助燃性 B.氢元素以化合态存在
C.摩尔质量为16 D.碳元素质量分数为20%
难度: 简单查看答案及解析
-
化学反应方程式书写正确的是
A.2H2O
2H2+O2 B.6HCl+2Fe
2FeCl3+3H2↑
C.CaCO3
CaO+CO2↑ D.2KClO3
2KCl+3O2↑
难度: 简单查看答案及解析
-
一氧化碳冶炼氧化铁的过程中,一氧化碳作
A.催化剂 B.氧化剂 C.还原剂 D.燃料
难度: 简单查看答案及解析
-
实验室中的操作类似“海水晒盐”原理的是
A.溶解 B.蒸发 C.过滤 D.搅拌
难度: 简单查看答案及解析
-
某纯净物不含氢元素,它不可能是
A.酸 B.盐 C.单质 D.氧化物
难度: 简单查看答案及解析
-
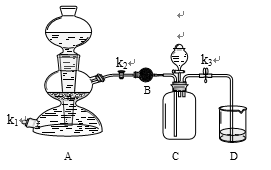
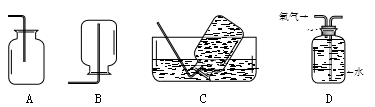
集气瓶可以完成多种实验,以下实验正确的是
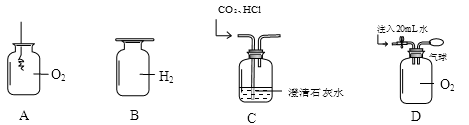
A.铁丝在O2中燃烧 B.储存H2
C.除去CO2 中HCl气体 D.气球收集20mL O2
难度: 简单查看答案及解析
-
室温时,将1g蔗糖放入100g水中,充分溶解,形成溶液。蔗糖分子发生变化的是
A.大小 B.个数 C.种类 D.间隔
难度: 简单查看答案及解析
-
利用中和反应原理的是
①熟石灰除去土壤中的硫酸 ②用稀硫酸除去铁锈
③氢氧化镁治疗胃酸过多 ④实验室制取二氧化碳
A.①③ B.③④ C.①②④ D.①③④
难度: 简单查看答案及解析
-
实验现象与结论对应正确的是
A.某固体中加入稀硫酸,产生气泡,该固体为活泼金属
B.某溶液中滴加酚酞试剂,不变色,该溶液为酸性溶液
C.某溶液进行焰色反应,火焰呈黄色,该溶液中含有钠元素
D.某溶液中滴加氯化钡和稀硝酸,产生白色沉淀,该溶液中含有硫酸盐
难度: 中等查看答案及解析
-
金属X与AgNO3溶液反应的化学方程式为:X+2AgNO3→X(NO3)2+2Ag。有关说法错误的是
A.X可能会与盐酸反应 B.X可能是铝
C.该反应属于置换反应 D.反应前后溶液质量发生变化
难度: 简单查看答案及解析
-
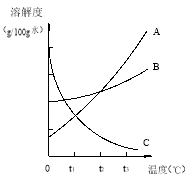
20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到四只各盛有50g水的烧杯中,充分溶解后的情况如下表所示,该温度下有关说法正确的是
物质
甲
乙
丙
丁
未溶解固体的质量 (g)
4.2
2
0
9.2
A.甲的溶解度是8.4g/100g水 B.再加入4mL水,乙中不溶固体全部溶解
C.丙溶液可能是饱和溶液 D.丁溶液的溶质质量分数最大
难度: 简单查看答案及解析
-
14gX在一定量的Y中恰好完全反应,生成44gM和18gN,变化的部分微观示意如图所示,有关说法正确的是
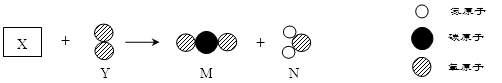
A.反应消耗3molY B.X可能含有三种元素
C.M属于有机物 D.X和N的物质的量的比为1:2
难度: 中等查看答案及解析
-
将某氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量。根据实验事实绘制如图所示曲线。其中说法正确的是
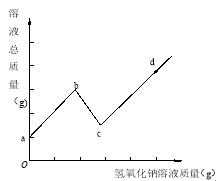
A.a至b段有蓝色沉淀生成
B.a至d段硫酸钠质量不断增大
C.c至d段,溶液pH不断减小
D.c点比a点所含的溶质种类少
难度: 中等查看答案及解析