-
实验室中的操作类似“海水晒盐”原理的是
A.溶解 B.蒸发 C.过滤 D.搅拌
九年级化学选择题简单题查看答案及解析
-
氯化钠是重要的化工原料,氯碱工业生产的一种流程如图:
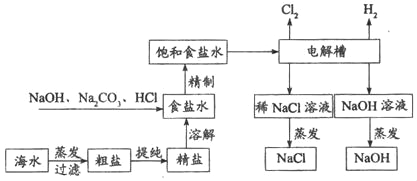
(1)从“海水叶粗盐叶精盐”的过程包括溶解、过滤、蒸发等实验操作,实验室中上述3种操作都需要使用的仪器是_____(填名称),该仪器在蒸发操作中的作用是_____。
(2)“食盐水”中常含有NaCl,MgCl2,CaCl2等物质,“精制”过程中加入NaOH的目的是_____。
(3)20℃时,“饱和食盐水”的溶质质量分数为26.47%,则该温度下,氯化钠的溶解度为_____(计算结果精确到0.1)。
(4)写出“电解槽”中发生反应的化学方程式:_____。
(5)流程中可以循环使用的物质有_____(填化学式)。
(6)氯碱工业生产的碱样品中常含有Na2CO3和NaCl等杂质,碱样品中含有Na2CO3的原因是_____;检验碱样品中是否含有Na2CO3,下列试剂中可选择使用的是_____(填字母)。
A 酚酞试液 B 石蕊试液 C 硝酸铵溶液 D 澄清石灰水
(7)用“离子交换膜法”生产的碱样品质量主要标准如下表所示:
等级
氢氧化钠含量
碳酸钠含量
优等品
≥99.0%
≤0.5%
一等品
≥98.5%
≤0.8%
合格品
≥98.0%
≤1.0%
化学兴趣B组设计并完成了如下实验来判断碱样品的等级(不考虑其他杂质参加反应)。称取20.3 g碱样品,加入足量的水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤、干燥,得到碳酸钡固体0.197 g;向滤液中加入2滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5.0%的稀盐酸365 g。
①该碱样品中碳酸钠的含量(质量分数)为_____(计算结果精确到0.01% )。
②列式计算该碱样品中氢氧化钠的含量_____(计算结果精确到0.01% )。
③该碱样品的等级为_____。
九年级化学流程题困难题查看答案及解析
-
人类利用海水可提取粗盐,进一步制得精盐,请回答:
(1)粗盐中含有的难溶性杂质,在实验室里可以通过溶解、过滤、蒸发等操作将其除去,其中过滤操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是___________________________(填序号)
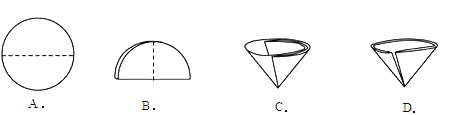
(2)在蒸发操作中玻璃棒的作用是___________________________(填“受热均匀”或“加快溶解”)。
(3)用氯化钠固体配制100g溶质质量分数为6%的氯化钠溶液,其正确的实验步骤顺序是___________________________(填字母)。
A.称量及量取
B.计算
C.溶解
D.装瓶贴标签
(4)溶液配制过程中除用到托盘天平、药匙、量筒、玻璃棒和胶头滴管外,还需要的仪器是___________________________。
(5)将已配制好的100g质量分数为6%的氯化钠溶液转化为质量分数为16%的氯化钠溶液,需要再加NaCl的质量是___________________________g( 计算结果精确至0.1)。
九年级化学填空题中等难度题查看答案及解析
-
下列实验操作中,不能达到实验目的是( )
实验目的 实验操作 A 鉴别海水与蒸馏水 加入硝酸银,看是否产生白色沉淀 B 提纯粗盐(含少量泥沙) 将粗盐加适量水溶解、过滤、蒸发结晶 C 除去氯化钙溶液中少量盐酸 加入过量的碳酸钙粉末、充分反应后过滤 D 分离硫酸钠和硫酸铜的混合溶液 加入过量氢氧化钠溶液后过滤,将滤渣溶于稀硫酸
A.A
B.B
C.C
D.D九年级化学选择题中等难度题查看答案及解析
-
海水晒盐可获得粗盐,其中含杂质Na2SO4、MgCl2、CaCl2、泥沙,实验室里可以分步提纯得到氯化钠。
(1)粗盐经过溶解、过滤、蒸发操作可获得精盐。加水溶解后,除去泥沙的操作步骤中玻璃棒的作用是什么?____
(2)为了进一步除去Na2SO4、MgCl2、CaCl2并得到氯化钠,有下列所加试剂和操作:①加过量的Na2CO3溶液 ②过滤③加过量的NaOH溶液 ④加适量的稀盐酸 ⑤加过量的BaCl2溶液 ⑥蒸发。写出能达到实验目的操作顺序______。
(3)在完成(2)中加入试剂和实验操作顺序时,你认为应该考虑的因素是什么?______
九年级化学实验题困难题查看答案及解析
-
氯化钠是重要的化工原料,氯碱工业生产的一种流程如图:
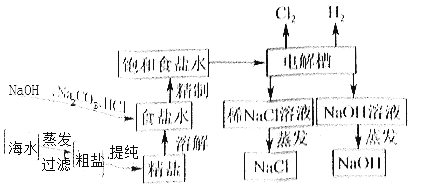
(1)从“海水→粗盐→精盐”的过程包括溶解、过滤、蒸发等实验操作,实验室中上述3种操作都需要使用的仪器是__(填名称)。
(2)“食盐水”中常含有NaCl、MgCl2、CaCl2等物质,“精制”过程中加入NaOH的目的是__。
(3)写出“电解槽“中发生反应的化学方程式__,流程中可以循环使用的物质有__(填化学式)。
(4)氯碱工业生产的碱样品中常含有Na2CO3和NaCl等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示
等级
氢氧化钠含量
碳酸钠含量
优等品
≥99.0%
≤0.5%
一等品
≥98.5%
≤0.8%
合格品
≥98.0%
≤1.0%
①你认为碱样品中含有Na2CO3的原因是__,检验碱样品中是否含有Na2CO3,下列试剂中可选择使用的是__。
a.酚酞 b.稀盐酸c。澄清石灰水
②李老师设计和完成了如下实验来判断碱样品的等级。
称取20.3g碱样品,加足量水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤,干燥得到碳酸钡(BaCO3)固体0.197g;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸365g。该碱样品的等级是__(不考虑其他杂质参加反应)。
九年级化学流程题中等难度题查看答案及解析
-
氯化钠是重要的化工原料,氯碱工业生产的一种流程如图:
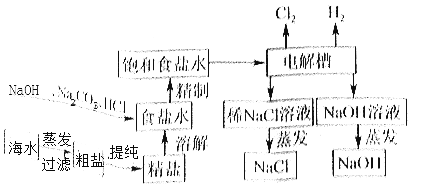
(1)从“海水→粗盐→精盐”的过程包括溶解、过滤、蒸发等实验操作,实验室中上述3种操作都需要使用的仪器是__(填名称)。
(2)“食盐水”中常含有NaCl、MgCl2、CaCl2等物质,“精制”过程中加入NaOH的目的是__。
(3)写出“电解槽“中发生反应的化学方程式__,流程中可以循环使用的物质有__(填化学式)。
(4)氯碱工业生产的碱样品中常含有Na2CO3和NaCl等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示
等级
氢氧化钠含量
碳酸钠含量
优等品
≥99.0%
≤0.5%
一等品
≥98.5%
≤0.8%
合格品
≥98.0%
≤1.0%
①你认为碱样品中含有Na2CO3的原因是__,检验碱样品中是否含有Na2CO3,下列试剂中可选择使用的是__。
a.酚酞 b.稀盐酸c。澄清石灰水
②李老师设计和完成了如下实验来判断碱样品的等级。
称取20.3g碱样品,加足量水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤,干燥得到碳酸钡(BaCO3)固体0.197g;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸365g。该碱样品的等级是__(不考虑其他杂质参加反应)。
九年级化学流程题中等难度题查看答案及解析
-
海洋是巨大的资源宝库,人类正在运用各种方法开发、提取海洋资源。
(1)海水晒盐得粗盐,粗盐提纯的实验步骤为:溶解、过滤、蒸发结晶。三步操作中均用到的一种玻璃仪器是__________,蒸发操作中该仪器的作用是_______________。
(2)从海水中得到金属镁。用苦卤制取金属镁的流程图如图所示:
①步骤1发生反应的化学方程式为_____________。
②验证苦卤中MgCl2已完全转化为Mg(OH)2沉淀的方法是______________。
(3)海水制碱,流程图如图所示:
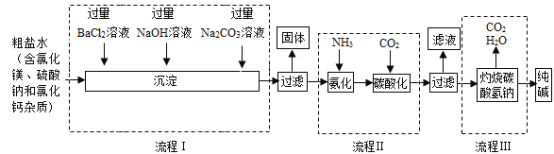
①该厂最终得到的产品有___________(填物质名称)。
②流程中加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,除掉的离子依次是_________(填离子符号,注意顺序)。
③写出流程Ⅱ中发生反应的化学方程式____________________。
九年级化学流程题中等难度题查看答案及解析
-
下列实验中, 实验原理和主要操作方法都不能达到实验目的的是
实验目的
实验原理
主要操作方法
A
除去粗盐中的泥沙
各成分的溶解性差异
先加足量水溶解,过滤,蒸发结晶
B
分离酒精与水的混合物
各成分的沸点差异
蒸馏
C
除去银粉中的锌粉
金属活动性差异
加入过量的稀盐酸,充分反应后过滤洗涤、干燥
D
鉴别稀盐酸和稀硫酸
都含氢离子有相似的化学性质
加入碳酸钠溶液,观察产生气泡快慢
A.A B.B C.C D.D
九年级化学单选题中等难度题查看答案及解析
-
用海水晒盐得到的是粗盐.提纯含有少量泥沙的粗盐,下列操作顺序正确的是( )
A.溶解、蒸发、过滤
B.过滤、蒸发、溶解
C.过滤、溶解、蒸发
D.溶解、过滤、蒸发九年级化学选择题中等难度题查看答案及解析