-
一定温度下,在固定容积的密闭容器中发生下列反应:2HI(g)
H2(g)+I2(g)。若HI浓度由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么HI浓度由0.07 mol·L-1降到0.05 mol·L-1时所需反应的时间为
A.等于5 s B.大于10 s C.等于10 s D.小于10 s
难度: 中等查看答案及解析
-
煤气是生活中常用的燃料,制取水煤气的反应为C(s)+H2O(g)
CO(g)+H2(g)。该反应在一容积可变的密闭容器中进行时,改变下列条件会对反应速率产生影响的是
①增加少量的碳 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使体系体积增大
A.①② B.②③ C.②④ D.①④
难度: 中等查看答案及解析
-
将1 mol A2和1 mol B2通入一容积不变的密闭容器中,在一定温度和催化剂作用下,发生反应:2A2(g)+B2(g)
2A2B(g)。反应达到平衡时A2B为0.3 mol。若此时移走0.5 mol A2和0.5 mol B2,则重新 达到平衡后,A2B的物质的量
A.小于0.15 mol B.等于0.3 mol
C.等于0.15 mol D.大于0.15 mol,小于0.3 mol
难度: 中等查看答案及解析
-
在25 ℃时,密闭容器中X、Y、Z三种气体的浓度变化情况如图,下列说法错误的是
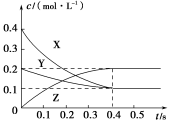
A.反应可表示为3X+Y
2Z
B.从反应开始到0.4 s时,以Y表示的化学反应速率为0.25 mol·L-1·s-1
C.增大压强使平衡向生成Z的方向移动,正逆反应速率均增大
D.升高温度,平衡常数一定增大
难度: 中等查看答案及解析
-
CO(g)+H2O(g)
H2(g)+CO2(g) ΔH<0,在其他条件不变的情况下
A.加入催化剂,加快了反应速率,反应的ΔH也随之改变
B.温度降低,正、逆反应速率都减小,反应放出的热量不变
C.恒容时充入稀有气体或充入H2,正、逆反应速率都减小
D.改变压强,反应速率发生改变,反应放出的热量不变
难度: 中等查看答案及解析
-
COCl2俗名称作光气,是有毒气体。在一定条件下,可发生的化学反应为: COCl2(g)
CO(g)+Cl2(g) ΔH<0下列有关说法不正确的是
A.在一定条件下,使用催化剂能加快反应速率
B.当反应达平衡时,恒温恒压条件下通入Ar,COCl2的转化率不变
C.单位时间内生成CO和消耗Cl2的物质的量比为1∶1时,反应达到平衡状态
D.平衡时,其他条件不变,升高温度可使该反应的平衡常数减小
难度: 中等查看答案及解析
-
在0.1mol·L-1CH3COOH溶液中存在如下电离平衡: CH3COOH
CH3COO-+H+,对于该平衡,下列叙述正确的是
A.加入水时,平衡向生成CH3COOH的方向移动
B.加入少量NaOH固体,平衡向电离的方向移动
C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向电离的方向移动
难度: 中等查看答案及解析
-
常温下0.1 mol·L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是
A.加入适量的氢氧化钠固体 B.将溶液稀释到原体积的 10倍
C.加入等体积0.2 mol·L-1氨水 D.降低溶液的温度
难度: 中等查看答案及解析
-
用食用白醋(醋酸浓度约为1 mol/L)进行下列实验,能证明醋酸为弱电解质的是
A.白醋中滴入石蕊试液呈红色 B.白醋加入豆浆中有沉淀产生
C.蛋壳浸泡在白醋中有气体放出 D.pH试纸显示醋酸的pH为2~3
难度: 中等查看答案及解析
-
欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少
A.通入二氧化碳气体 B.加入氢氧化钠固体
C.通入氯化氢气体 D.加入饱和石灰水溶液
难度: 中等查看答案及解析
-
一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g)
2NH3(g) ΔH<0,反应过程如图:下列说法正确的是
A.t1 min时正、逆反应速率相等。
B.X曲线表示NH3的物质的量随时间变化的关系
C.0~8 min,H2的平均反应速率v(H2)=
mol·L-1·min-1
D.10~12 min,升高温度使反应速率加快,平衡正向移动
难度: 中等查看答案及解析
-
可逆反应mA(g)+nB
pC(g)+qD中,A和C都是无色气体,达到平衡后,下列叙述正确的是
A.若增加B的量,平衡体系颜色加深,说明B必是气体
B.增大压强,平衡不移动,说明m+n一定等于p+q
C.升高温度,A的转化率减小,说明正反应是吸热反应
D.若B是气体,增大A的量,A、B的转化率都增大
难度: 中等查看答案及解析
-
在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)
Ni(CO)4(g),已知该反应在25 ℃和80 ℃时的平衡常数分别为5×104、2。下列说法正确的是
A.恒温恒容下,向容器中再充入少量Ni(CO)4(g),达新平衡时,Ni(CO)4的百分含量将增大
B.在80 ℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v(正)<v(逆)
C.恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动
D.上述生成Ni(CO)4(g)的反应为吸热反应
难度: 中等查看答案及解析
-
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应
A.强酸溶液产生较多的氢气 B.两者产生等量的氢气
C.无法比较两者产生氢气的量 D.弱酸溶液产生较多的氢气
难度: 中等查看答案及解析
-
水的电离平衡曲线如图所示,下列说法正确的是
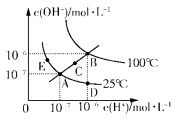
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到D点,可采用在水中加入少量酸的方法
C.若从A点到C点,可采用温度不变时在水中加入适量NaOH固体的方法
D.若处在B点时,将pH=2的硫酸与pH=12的KOH等体积混合后,溶液显中性
难度: 中等查看答案及解析