-
室温下,同种规格的铝片分别与下列物质混合,产生氢气速率最大的是
A. 0.1 mol/L的盐酸15mL B. 0.15 mol/L的硫酸溶液8mL
C. 0.4 mol/L的硝酸12mL D. 18 mol/L的浓硫酸15mL
难度: 中等查看答案及解析
-
下列说法中,错误的是
A. 人类目前所直接利用的能量大部分是由化学反应产生的
B. 煤、石油、天然气是当今世界最重要的三种化石燃料
C. 化学变化中的能量变化主要是由化学键变化引起的
D. 化学反应中能量变化的大小与反应物的质量多少无关
难度: 中等查看答案及解析
-
化学用语在化学学习中有着重要的作用.下列有关化学用语使用正确的是
A.CO2的电子式
B.Cl-的结构示意图
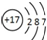
C.HCl的电子式
D.质量数为37的氯原子
难度: 中等查看答案及解析
-
下列反应中,反应物总能量低于生成物总能量,且属于氧化还原反应的是
A. Ba(OH)2·8H2O与NH4Cl反应 B. 灼热的炭与CO2反应
C. 铝与稀盐酸 D. 铝粉与氧化铁粉末反应
难度: 中等查看答案及解析
-
不具有放射性的同位素称为稳定同位素,稳定同位素分析法近20年来在植物生理学、生态学和环境科学研究中获得广泛应用。如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物。下列有关说法正确的是 ( )。
A. 34S原子核内中子数为16
B. 1H216O和1H218O的相对分子质量不同
C. 13C和15N原子核内的质子数相差2
D. 2H+结合OH-的能力比1H+的更强
难度: 中等查看答案及解析
-
下图中横坐标均表示11~17号元素顺序排列的原子序数。根据图像变化趋势判断,纵坐标表示其最高化合价的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列说法中错误的是
A. 在周期表中,原子的核外电子层数等于该元素所在的周期数
B. 元素周期表中从IIIB族到IIB族10个纵行的元素都是金属元素
C. 室温时,零族元素的单质都是气体
D. 位于IA的元素与位于VIIA的元素组成的化合物都是离子化合物
难度: 简单查看答案及解析
-
运用元素周期律分析下面的推断,其中不正确的是
A. 锂(Li)与水反应不如钠与水反应剧烈
B. 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸
C. 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂
D. HIO4的酸性比HBrO4的酸性强
难度: 中等查看答案及解析
-
下列关于能量转换的认识中不正确的是
A. 白炽灯工作时,电能全部转化为光能
B. 普通干电池工作时将化学能转变为电能
C. 化学反应中的能量变化,通常主要表现为热量的变化
D. 火力发电是通过化石燃料燃烧,使化学能经过一系列能量转化最终转变为电能
难度: 简单查看答案及解析
-
下列判断错误的是
A. 碘升华——分子间作用力被破坏
B. HCl气体溶于水——共价键被破坏
C. NaCl晶体溶于水——离子键被破坏
D. 氢氧化钠熔化——离子键和共价键被破坏
难度: 简单查看答案及解析
-
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是( )
A. Y元素最高价氧化物对应的水化物化学式H2YO4
B. 原子半径由小到大的顺序为:X<Z<Y
C. Y、Z两种元素气态氢化物中,Z的气态氢化物最稳定
D. X与W形成的两种化合物中,阴、阳离子物质的量之比均为1︰2
难度: 中等查看答案及解析
-
X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-离子具有相同的电子层结构。下列说法正确的是
A. 原子最外层电子数:X>Y>Z B. 原子序数:X>Y>Z
C. 离子半径:X2->Y+>Z- D. 氢化物的稳定性:X>Z
难度: 简单查看答案及解析
-
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )

A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的酸性均减弱
D.产生气泡的速度甲比乙慢
难度: 中等查看答案及解析
-
如图所示,电流表G的指针发生偏转,同时A极质量增加,B极质量减少,C为电解质溶液。则A、B、C分别可能为
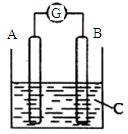
A.A是Zn,B是Cu,C是稀硫酸
B.A是Cu,B是Zn,C是稀硫酸
C.A是Fe,B是Ag,C是AgNO3稀溶液
D.A是Ag,B是Fe,C是AgNO3稀溶液
难度: 中等查看答案及解析
-
下列关于化学反应的限度的叙述中,正确的是
A. 任何化学反应的限度都相同
B. 可以通过改变温度控制化学反应的限度
C. 可以通过延长化学反应的时间改变化学反应的限度
D. 当一个化学反应在一定条件下达到最大限度时,反应速率也最大
难度: 简单查看答案及解析
-
下列金属冶炼的反应原理,错误的是( )。
A. 2NaCl(熔融)
2Na+Cl2↑ B. Al2O3+3H2
2Al+3H2O
C. Fe3O4+4CO
3Fe+4CO2↑ D. 2HgO
2Hg+O2↑
难度: 简单查看答案及解析
-
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法错误的是
X
Y
W
Z
T
A. X、Y、Z三种元素最低价氢化物的沸点依次升高
B. 物质W3X4中,每个原子最外层均达到8电子稳定结构
C. X、Y和氢形成的化合物中可能既有离子键、又有共价键
D. T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
难度: 简单查看答案及解析
-
恒温下,在体积恒定的密闭容器中发生可逆反应:2SO2 (g)+ O2(g)
2SO3(g),下列不能用来判断该反应达到平衡状态的是
A. 容器中压强不再变化 B. SO2的体积分数不再变化
C. 容器中混合物的密度不再变化 D. 容器中各物质的浓度不再变化
难度: 简单查看答案及解析
-
某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,下列有关说法错误的是

A. 该反应的化学方程式为3X+Y
2Z
B. 2 min时,反应达最大限度,但化学反应仍在进行
C. 反应开始至2 min,Z的反应速率为0.05 mol•L﹣1•min﹣1
D. 反应达到平衡时,压强是开始时的0.8倍
难度: 中等查看答案及解析
-
在一定温度下,10mL 0.40mol/L H2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
t/min
0
2
4
6
8
10
V(O2)/mL
0.0
9.9
17.2
22.4
26.5
29.9
下列叙述不正确的是(溶液体积变化忽略不计)
A. 0~6 min的平均反应速率:v(H2O2)≈ 3.3×10﹣2 mol/(L•min)
B. 6~10 min的平均反应速率:v(H2O2)< 3.3×10﹣2 mol/(L•min)
C. 反应到6 min时,H2O2分解了50%
D. 反应到6 min时,c(H2O2)=0.30 mol/L
难度: 简单查看答案及解析