-
造成大气污染的SO2主要来源于 ( )
A. 火山喷发 B. 自然界中游离态硫缓慢氧化
C. 煤、石油等含硫燃料的大量燃烧、硫矿石的冶炼及硫酸工业等产生的工业废气 D. 汽车尾气
难度: 简单查看答案及解析
-
常温下能用铁罐或铝罐贮存的是( )
A. 浓H2SO4 B. 浓HCl C. 稀H2SO4 D. 稀HNO3
难度: 简单查看答案及解析
-
将蔗糖用少量水湿润,然后在不断搅拌下加入浓硫酸,可看到蔗糖颜色变黑,体积逐渐膨胀,最后变成多孔的疏松固体,且产生刺激性气味的气体,上述过程中( )
A. 体现浓硫酸的吸水性 B. 体现了浓硫酸的脱水性
C. 体现了浓硫酸的吸水性和脱水性 D. 体现了浓硫酸的吸水性、脱水性和强氧化性
难度: 简单查看答案及解析
-
下列离子方程式正确是( )
A. 碳酸氢钠与过量的氢氧化钙溶液反应:HCO3- +OH- +Ca2+ =CaCO3↓+H2O
B. 过氧化钠与水的反应:2 O22- + 2H2O = 4 OH- + O2↑
C. 碳酸钙加入醋酸CO32-+2CH3COOH=CO2↑+2CH3COO-+H2O
D. 铁与稀盐酸的反应:2Fe+6H+=2Fe3++3H2↑
难度: 简单查看答案及解析
-
下列各组中的离子,因发生氧化还原反应而不能大量共存同一溶液中的是:( )
A. Fe2+、SO42-、Fe3+ 、Cl- B. S2-、Cu2+、Na+、Cl-
C. H+、SO42-、Cu2+、OH- D. Fe2+、H+、Mg2+、NO3-
难度: 中等查看答案及解析
-
下列变化不可能通过一步反应直接完成的是 ( )
A. Al(OH)3 → Al2O3 B. SiO2 → H2SiO3
C. Al → AlO2- D. Si→ Na2SiO3
难度: 中等查看答案及解析
-
证明某溶液含有Fe2+的实验方法是 ( )
A. 先滴加氯水,再滴加KSCN溶液后显红色
B. 先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C. 滴加NaOH溶液,产生白色沉淀
D. 只需滴加KSCN溶液
难度: 中等查看答案及解析
-
将Fe、Cu、FeCl2、FeCl3、CuCl2盛于同一容器中充分反应,如Fe有剩余,则容器中只能有的金属或金属离子是 ( )
A. Cu、Fe3+ B. Fe2+、Fe3+ C. Cu、Cu2+、Fe D. Cu、Fe2+、Fe
难度: 中等查看答案及解析
-
100ml某混合液中HNO3的物质的量浓度为0.2mol/L, H2SO4 的物质的量浓度为0.1mol/L,向其中加入1.92g Cu,微热,完全反应后溶液中Cu2+的物质的量浓度为( )
A. 0.3 mol/L B. 0.15 mol/L
C. 0.25 mol/L D. 无法计算
难度: 中等查看答案及解析
-
向MgSO4和Al2(SO4)3的混合溶液中, 逐滴加入NaOH溶液。下列图象中(横坐标表示NaOH溶液的体积, 纵坐标表示沉淀质量), 能正确表示上述反应的是 ( )
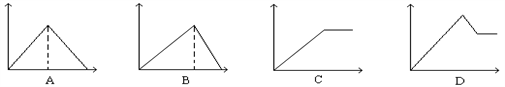
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
把a g 铝铁合金粉末溶于足量盐酸中,再加入过量氢氧化钠溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则此合金中铝的质量分数为( )
A. 70% B. 30% C. 52.4% D. 22.2%
难度: 中等查看答案及解析
-
4.6g金属钠在干燥空气中被氧化后,得到7.0g固体,由此可判断其产物是 ( )
A. 只有Na2O B. 只有Na2O2 C. Na2O2和Na2O D. 无法确定
难度: 中等查看答案及解析
-
在Na2O2与CO2的反应中,被氧化元素与被还原元素的质量比是 ( )
A. 1:1 B. 1:2 C. 2:1 D. 8:53
难度: 简单查看答案及解析
-
向25mL 18.4mo1·L-1 H2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量是( )
A. 小于0.23 mol B. 等于0.23 mol
C. 0.23mol~0.46mol之间 D. 等于0.46mol
难度: 简单查看答案及解析
-
下列反应中,SO2作为氧化剂而发生反应的是( )
A. 2SO2+O2 = 2SO3 B. SO2 + H2O = H2SO3
C. SO2 + 2H2S = 3S↓ + 2H2O D. SO2 + Cl2 + 2H2O = H2SO4 + 2HCl
难度: 简单查看答案及解析
-
下列物质能使品红溶液褪色的是( )
①干燥的Cl2 ②Na2O2 ③O3 ④活性炭 ⑤SO2
A. 除①外其他都可以 B. 只有①②③
C. 只有①④⑤ D. 全部都可以
难度: 简单查看答案及解析
-
在反应Cl2+2NaOH =NaCl +NaClO+H2O的变化中,当产生58.5gNaCl时,转移电子总数是:( )
A. 1.204×1024个 B. 6.02×1023个 C. 4.816×1023个 D. 2.408×1023个
难度: 简单查看答案及解析
-
用MnO2和浓盐酸反应制取氯气时,当有4mole-转移时,生成的氯气在标况下的体积为:( )
A. 22.4L B. 11.2L C. 44.8L D. 89.6L
难度: 简单查看答案及解析
-
加热10.0g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45g,求混合物中碳酸钠的质量分数。( )
A. 58% B. 42% C. 36% D. 64%
难度: 简单查看答案及解析
-
由锌、铁、铝、镁四种金属中的两种组成的混和物10克,与足量的盐酸反应产生的氢气在标准状况下为11.2升,则混和物中一定含有的金属是( )
A. 锌 B. 铁 C. 铝 D. 镁
难度: 困难查看答案及解析
-
金属钠长期置于空气中,最后变为: ( )
A. Na2O B. Na2O2 C. NaOH D. Na2CO3
难度: 简单查看答案及解析
-
1体积的CO2和O2的混合气体通过足量的Na2O2后所得气体的体积变为原来的3/4,则CO2在原混合气体中所占体积分数为:( )
A. 25% B. 40% C. 50% D. 75%
难度: 中等查看答案及解析
-
金属钠分别与下列物质反应时,既有沉淀又有气体生成的是:( )
A. 氯化钡溶液 B. 硫酸钾溶液 C. 氯化铁溶液 D. 硝酸铵溶液
难度: 简单查看答案及解析
-
焰色反应是:( )
A. 单质的性质 B. 化合物的性质 C. 元素的性质 D. 离子的性质
难度: 简单查看答案及解析
-
将8gFe2O3投入150mL的稀硫酸中,再投入7g铁粉,共收集到1.68L氢气(标准状况下),同时固体均无剩余,向溶液中滴入KSCN溶液,未见颜色变化。为了中和多余的硫酸,且使Fe2+全部转化为Fe(OH)2沉淀,共消耗4mol/L的NaOH溶液150mL,则原硫酸的物质的量浓度为( )mol/L。
A. 1 B. 2 C. 3 D. 4
难度: 困难查看答案及解析