-
下列离子方程式书写正确的是( )
A.氧化铁溶于氢碘酸:Fe2O3+6H+═2Fe3+3H2O
B.等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O
C.过氧化钠固体与水反应:2O22一+2H2O═4OH一+O2↑
D.硫化钠水溶液呈碱性的原因:S2-+2H2O⇌H2S↑+2OH-难度: 中等查看答案及解析
-
现代无机化学对硫一氮化合物的研究是最为活跃的领域之一.其中图是已经合成的最著名的硫一氮化合物的分子结构.下列说法错误的是( )
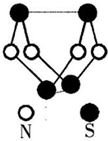
A.该物质的分子式为S4N4
B.该物质与化合物s2N2互为同素异形体
C.该物质的分子结构中含有极性键
D.该物质中所含化学键S-N键能小于N2中N≡N键能难度: 中等查看答案及解析
-
用M表示阿伏加德罗常数的数值,下列说法中一定正确的是( )
A.1 L l mol•L-1的FeCl3溶液中含有NA个Fe3+
B.4.8g镁与足量盐酸反应时,转移0.2 NA个电子
C.钠与水反应生成1.12 L H2,反应中转移的电子数为0.1NA
D.常温常压下,22g氧气和26g臭氧混合气体所含氧原子总数为3NA难度: 中等查看答案及解析
-
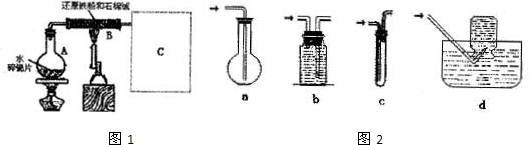
如图所示,利用培养皿进行实验.实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面.
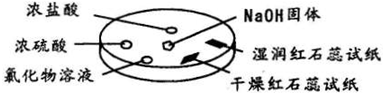
下表中对实验现象所做的解释不正确的是( )选项 实验现象 解释 A 浓盐酸附近产生白烟 NH3与HCl反应产生了NH4Cl固体 B 浓硫酸附近无白烟 NH3与浓硫酸不发生反应 C 干燥红色石蕊试纸不变色,湿润红色石蕊试纸变蓝 NH3与水反应生成了NH3.H2O,电离出OH一使红色石蕊试纸变蓝 D 氯化物溶液变浑浊 可能是AICl3与NH3反应生成Al(OH)3
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
某溶液中含有NH4+、H+、SO42-和OH-,对该溶液的描述一定正确的是( )
A.该溶液可能呈酸性,也可能呈碱性或中性
B.只能是硫酸铵和硫酸的混合溶液
C.离子浓度由大到小的顺序是:c(NH4+)>c(SO42-)>c(H+)>c(OH-)
D.离子浓度存在下列关系:c(NH4+)+c(H+)=c(OH-)+c(SO42-)难度: 中等查看答案及解析
-
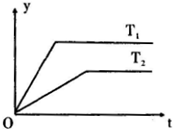
在一密闭容器中充人4mol SO2和一定量O2,发生反应:2SO2(g)+O2(g)⇌2SO3(g)△H=一196.6kJ•mol-1.则下列说法正确的是( )
A.为提高反应速率和SO2的转化率选择更高效的催化剂
B.增大压强有利于SO2转化,平衡常数也会增大
C.当放出353.6 kJ热量时,SO2的转化率接近90%
D.图中纵坐标y为SO3的含量难度: 中等查看答案及解析
-
用铜片、银片设计成如图所示的原电池.以下有关该原电池的叙述正确的是( )
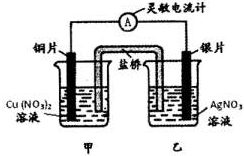
A.电子通过盐桥从乙池流向甲池
B.铜导线替换盐桥,原电池仍继续工作
C.开始时,银片上发生的反应是:Ag-e Ag+
D.将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同难度: 中等查看答案及解析
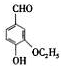 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.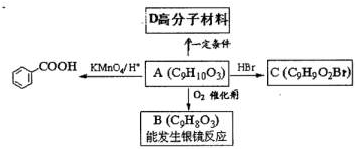
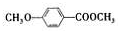 )是一种医药中间体.某兴趣小组提出用茴香醛(
)是一种医药中间体.某兴趣小组提出用茴香醛( 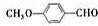 )为基本原料通过2步合成E.指出该流程中所涉及的化学反应类型______,______.
)为基本原料通过2步合成E.指出该流程中所涉及的化学反应类型______,______.