-
下列微粒中,能表示2个氢原子的是
A. 2H B. 2H+ C. H2O D. 2H2
难度: 简单查看答案及解析
-
下列过程中发生化学变化的是
A. 拧干衣服 B. 食物腐败 C. 写粉笔字 D. 粉碎废纸
难度: 简单查看答案及解析
-
下列物质由离子构成的是
A. 氧气 B. 氯化钠 C. 铁 D. 水
难度: 简单查看答案及解析
-
将自然界中的水进行净化处理,其中净化程度最高的方法是
A. 吸附 B. 沉降 C. 蒸馏 D. 过滤
难度: 简单查看答案及解析
-
下列物质的化学式书写不正确的是
A. 氧化钙——CaO2 B. 氢氧化钠——NaOH
C. 氯化钾——KCl D. 二氧化碳——CO2
难度: 中等查看答案及解析
-
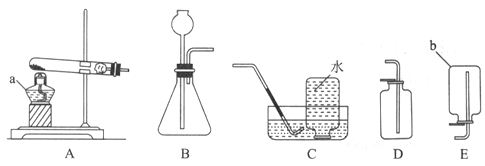
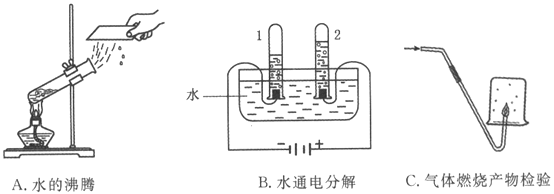
下列实验基本操作正确的是

A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列有关物质燃烧现象的叙述中,正确的是
A. 铁丝在氧气中燃烧:火星四射,生成红色固体
B. 硫粉在空气中燃烧:产生淡蓝色火焰,生成一种刺激性气味的气体
C. 木炭在空气中燃烧:发出耀眼的白光
D. 红磷在空气中燃烧:发出白光,生成大量的白色烟雾
难度: 中等查看答案及解析
-
在空气中含量较多且化学性质不活泼的气体是
A. 氮气 B. 二氧化碳 C. 氧气 D. 水蒸气
难度: 简单查看答案及解析
-
下图为海水中富含的钠元素和氯元素在元素周期表中的部分信息。下列有关说法不正确的是

A. 氯是一种非金属元素 B. 钠的相对原子质量是22.99
C. 钠原子的中子数为11 D. 氯元素的原子序数为17
难度: 简单查看答案及解析
-
下列对催化剂描述正确的是
A. 任何化学反应都需要催化剂 B. 催化剂在反应前后本身的质量发生了变化
C. 二氧化锰可作为各种化学反应的催化剂 D. 某些化学反应可以有多种催化剂
难度: 简单查看答案及解析
-
雾霾是一种大气污染现象,治理雾霾势在必行。下列不属于雾霾治理措施的是
A. 外出时佩戴防雾霾口罩 B. 提倡绿色出行,发展公共交通
C. 植树绿化,美化环境 D. 使用清洁能源
难度: 简单查看答案及解析
-
下列关于水的说法不正确的是
A. 水从液态变成气态时,分子间隔变大
B. 爱护水资源就要节约用水和防止水体污染
C. 地球上可利用的淡水资源丰富,不用节约用水
D. 如果将水样蒸干后有固体残留,这种水样中一定含有杂质
难度: 简单查看答案及解析
-
为证明人体呼出的气体中二氧化碳含量明显高于空气中二氧化碳的含量,采用如下图装置进行实验。下列说法不正确的是
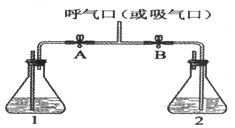
A. 瓶1和瓶2中所装试剂均为相同的澄清石灰水
B. 吸气时,应将A打开、B关闭,呼气时,则相反
C. 呼气时,瓶2试剂中出现气泡,液体始终不变浑浊
D. 通过瓶1和瓶2中的不同现象,证明人体呼出的气体中二氧化碳含量明显高于空气中二氧化碳的含量
难度: 简单查看答案及解析