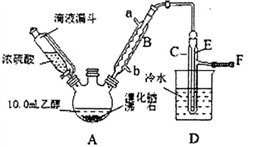
-
下列各原子或离子的电子排布式正确的是
A. K ls22s22p63s23p63d1 B. Cr ls22s22p63s23p63d44s2
C. As [Ar]4s24p3 D. Zn2- [Ar] 3d10
难度: 简单查看答案及解析
-
下列说法不正确的是
A. 同一原子中, ls、2s、3s电子的能量逐渐增多
B. 同一原子中,2p、3p、4p能级的轨道数依次增多
C. 任一原子的p能级电子云轮廓图形状均呈哑铃形
D. 任一能层的能级数等于该能层序数
难度: 简单查看答案及解析
-
下列有关微粒性质的比较中不正确的是
A. 离子半径:O2->Na+>Mg2+ B. 原子的未成对电子数:Mn>Ge>Br
C. 元素的第一电离能:O>N>C D. 元素的电负性:F>N>Si
难度: 简单查看答案及解析
-
若某原子在处于能量最低状态时,价电子层排布为4d25s2,则下列说法正确的是
A. 该元素原子最外层共有4个电子
B. 该元素原子核外第N层上共有10个不同运动状态的电子
C. 该元素处于第五周期IVA族
D. 该元素原子第四电子层上有4个空轨道
难度: 中等查看答案及解析
-
下列说法不正确的是
A. 医药中常用酒精来消毒,是因为酒精能使细菌蛋白质变性
B. 日常生活中的饮料、糖果和糕点等常使用酯类作香料
C. 石油的裂化和裂解是获得芳香烃的主要途径
D. 淀粉和纤维素水解的最终产物都是葡萄糖
难度: 简单查看答案及解析
-
下列有关物质分子结构特征的描述,正确的是
A. 乙炔易与溴的四氯化碳溶液发生反应,且lmol乙炔完全加成消耗2molBr2,证明乙炔分子里含有一个碳碳三键
B. 苯分子的结构中存在碳碳单键和碳碳双键交替出现的结构
C.
 和
和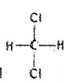 属于同一种物质,不能用来解释甲烷是一种正四面体结构
属于同一种物质,不能用来解释甲烷是一种正四面体结构D. lmolCH3CH2OH与Na完全反应只生成0.5molH2,不能说明乙醇分子中有一个氢原子与其它氢原子不同
难度: 简单查看答案及解析
-
下列有机物的命名,正确的是
A.
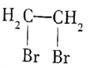 二溴乙烷
二溴乙烷B.
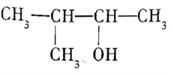 2-甲基-3-丁醇
2-甲基-3-丁醇C. (CH3)3CCH2CH(CH3)2 2,2,3-三甲基戊烷
D.
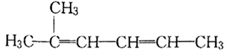 2-甲基-2,4-己二烯
2-甲基-2,4-己二烯难度: 简单查看答案及解析
-
某化合物的结构(键线式)及球棍模型如下:

该有机分子的核磁共振氢谱图如下(单位是ppm):

化学位移5
下列关于该有机物的叙述正确的是
A. 该有机物属于芳香族化合物
B. 键线式中的Et代表的基团为-CH3
C. 该有机物不同化学环境的氢原子有8种
D. 该有机物在氢氧化钠醇溶液加热的情况下能发生消去反应
难度: 中等查看答案及解析
-
有机物A经氧化后得B(化学式为C2H3O2Br),而A经水解得D,0.1molD和2molB反应得到一种含溴的酯(C6H8O4Br2)。由此推断A的结构简式为
A. Br-CH2CH2OH B.
 C.
C.  D. HOCH2CH2OH
D. HOCH2CH2OH难度: 中等查看答案及解析
-
下列说法正确的是
A. 总质量一定的油脂,无论以何种比例组合,完全水解后生成甘油的量不变
B. 用甘氨酸(
 )和丙氨酸(
)和丙氨酸(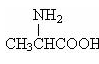 )缩合最多可形成4种二肽
)缩合最多可形成4种二肽C. 用碳酸钠溶液不能区分乙醇、乙酸、苯和硝基苯四种有机物
D. 苯酚和苯甲醇互为同系物,均能使酸性高锰酸钾溶液褪色
难度: 简单查看答案及解析
-
同一条件下,下列关系不正确的是
A. 在水中的溶解度:丙三醇>HOCH2CH2CH2OH>CH3CH2CH2OH > CH2CH2COOCH
B. 密度:CCl4>CHCl3>H2O>苯
C. 熔点:2,2—二甲基戊烷>2, 3—二甲基丁烷>戊烷>丙烷
D. 与金属钠反应的剧烈程度:乙酸>苯酚>乙醇>水
难度: 中等查看答案及解析
-
下列实验的失败原因可能是因为缺少必要的实验步骤造成的是
①验证某RX是氯代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再加入硝酸银溶液未出现白色沉淀
②将乙醇和乙酸混合,再加入稀硫酸共热制乙酸乙酯
③向苯酚浓溶液中加入少许稀溴水,未见白色沉淀
④做醛的还原性实验时,当加入新制的氢氧化铜悬浊液后,未出现红色沉淀
⑤检验淀粉己经水解,将淀粉与少量稀硫酸加热一段时间后,加入银氨溶液后未析出银镜
A. ③④⑤ B. ①③④ C. ①④⑤ D. ②④⑤
难度: 简单查看答案及解析
-
CPAE是蜂胶的主要活性成分,它可由咖啡酸合成,其合成过程如下。下列说法不正确的是
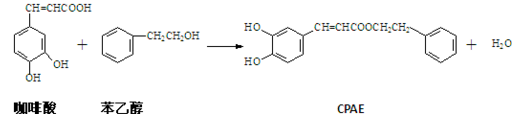
A. 咖啡酸的分子式为C9H8O4
B. 咖啡酸可发生加聚反应,并且所得聚合分子中含有3种官能团
C. 1 mol CPAE与足量的NaOH溶液反应,最多消耗3molNaOH
D. 1 mol CPAE与足量H2反应,最多消耗7 mol H2
难度: 简单查看答案及解析
-
某气态不饱和链烃CxHy在一定条件下与H2加成为CxHy+m,取CxHy和H2混合气体共120mL进行实验,发现随混合气体中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温间压下测定)由此可知m的数值为
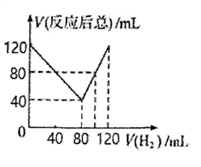
A. 1 B. 2 C. 3 D. 4
难度: 中等查看答案及解析
-
分子式为C4H7BrO2且能与碳酸氢钠反应生成气体的有机物数目,与下列各选项有机物数目相同的是(不含立体异构)
A. 分子式为C4H8O2的酯 B. 分子式为C5H10的烯烃
C. 甲苯的一氯代物 D. 立体烷(
 )的二氯代物
)的二氯代物难度: 简单查看答案及解析
-
如下流程中a、b、c、d、e、f是六种有机物,其中a是烃类,其余是烃的衍生物。下列有关说法正确的是
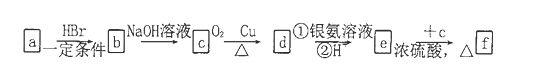
A. 若a为单烯烃,则d与f的最简式一定相同
B. 若d的相对分子质量是44,则a是乙炔
C. 若a为苯乙烯(
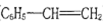 ),则f的分子式是C16H32O2
),则f的分子式是C16H32O2D. 若a的相对分子质量是42,则d是乙醛
难度: 中等查看答案及解析
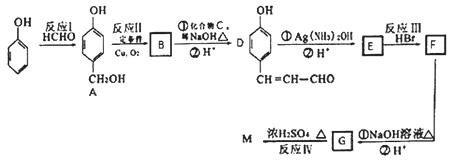
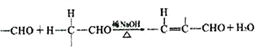
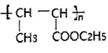 的合成路线:(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)________。
的合成路线:(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)________。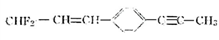 分子结构中最多有________个原子共面。
分子结构中最多有________个原子共面。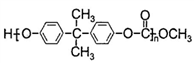 的透光率良好,可制作车、船、飞机的挡风玻璃,以及眼镜镜片、光盘、唱片等。合成聚碳酸酯是用绿色化学原料碳酸二甲酯(
的透光率良好,可制作车、船、飞机的挡风玻璃,以及眼镜镜片、光盘、唱片等。合成聚碳酸酯是用绿色化学原料碳酸二甲酯( )与________(写出该有机物的结构简式)缩合聚合而成。
)与________(写出该有机物的结构简式)缩合聚合而成。