-
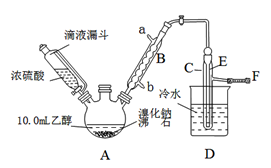
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):
H2SO4(浓)+NaBr  NaHSO4+HBr↑
NaHSO4+HBr↑
CH3CH2OH+HBr CH3CH2Br+H2O。有关数据见下表:
CH3CH2Br+H2O。有关数据见下表:
| 乙醇 | 溴乙烷 | 溴 |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度/(g·cm-3) | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(1)A装置的名称是______________。
(2)实验中用滴液漏斗代替分液漏斗的优点为_______________________。
(3)给A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应,写出此反应的化学方程式________________________。
(4)给A加热的目的是________________________,F接橡皮管导入稀NaOH溶液,其目的主要是___________________。
(5)图中C中的导管E的末端须在水面以下,其目的是______________________。
(6)粗产品洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的无水硫酸镁固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0 g。从乙醇的角度考虑,本实验所得溴乙烷的产率是________________。
-
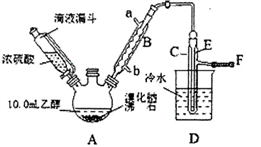
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其实验的装置如下(反应需要加热,图中省去了加热装罝):
| 乙醇 | 溴乙烷 | 溴 |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度/(g • cm-3) | 0.79 | 1.44 | 3. 1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(1)A装置的名称是________。
(2)沸石的作用是________。
(3)己知H2SO4(浓)+NaBr NaHSO4+HBr↑,写出A中生成溴乙烷的化学方程式________。
NaHSO4+HBr↑,写出A中生成溴乙烷的化学方程式________。
(4)C中收集到的粗产品混有杂质的主要成份是________;为了除去这些杂质,最好选择下列____(选填序号)溶液来洗涤所得粗产品。
A.氢氧化钠 B.碘化钠 C.亚硫酸钠 D.碳酸氢钠
(5)粗产品洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的M固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0g。
①M固体的名称为________;
②在上述提纯过程中每次分液时,产品均从分液漏斗的________(填“上口”或“下口”)放出;
③从乙醇的角度考虑,本实验所得溴乙烷的产率是_________。
(6)该实验装罝的主要缺陷是________。
-
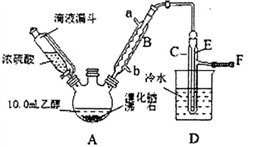
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其实验的装置如下(反应需要加热,图中省去了加热装罝):
| 乙醇 | 溴乙烷 | 溴 |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度/(g • cm-3) | 0.79 | 1.44 | 3. 1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(1)A装置的名称是________。
(2)沸石的作用是________。
(3)己知H2SO4(浓)+NaBr NaHSO4+HBr↑,写出A中生成溴乙烷的化学方程式________。
NaHSO4+HBr↑,写出A中生成溴乙烷的化学方程式________。
(4)C中收集到的粗产品混有杂质的主要成份是________;为了除去这些杂质,最好选择下列____(选填序号)溶液来洗涤所得粗产品。
A.氢氧化钠 B.碘化钠 C.亚硫酸钠 D.碳酸氢钠
(5)粗产品洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的M固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0g。
①M固体的名称为________;
②在上述提纯过程中每次分液时,产品均从分液漏斗的________(填“上口”或“下口”)放出;
③从乙醇的角度考虑,本实验所得溴乙烷的产率是_________。
(6)该实验装罝的主要缺陷是________。
-
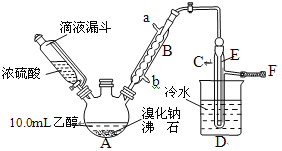
实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):
H3PO4(浓)+NaBr NaH2PO4+HBr、CH3CH2OH+HBr
NaH2PO4+HBr、CH3CH2OH+HBr CH3CH2Br+H2O
CH3CH2Br+H2O
有关数据见下表:
| 乙醇 | 溴乙烷 | 溴 |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度g/mL | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(1)A中放入沸石的作用是___。
(2)仪器B的名称为___,B中进水口为___(填“a”或“b”)口。
(3)实验中用滴液漏斗代替分液漏斗的优点为:___。
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?___(用化学方程式表示)。
(5)将C中的馏出液转入三角烧瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是___。
-
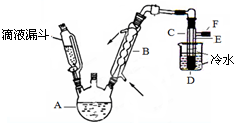
下图是实验室用乙醇、硫酸、溴化钠混合反应来制备溴乙烷的装置。反应需要加热,图中省去了加热装置。乙醇、溴乙烷、溴的有关性状参数见下表。
| 乙醇 | 溴乙烷 | 溴 |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g.cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
| 水溶性 | 易溶 | 难溶 | 微溶 |
(1)加热A中三种反应物的混合物时,发生反应的化学方程式为: 。
(2)若选用较浓的硫酸作为反应物,得到的产品则会呈棕黄色,这说明反应过程中有 生成。为去除颜色,最好选择下列的 溶液来洗涤产品。
A.四氯化碳 B.硫酸钠 C.碘化亚铁 D.亚硫酸钠
产品选择上述溶液洗涤后,还需再用蒸馏水洗涤一次。洗涤液与产品分离的方法是 (填方法名称)。
(3)装置中,B和D两部分的作用分别是:B ;D 。
-
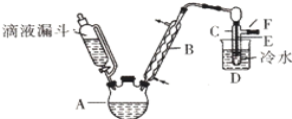
(14分)下图是实验室用乙醇与浓硫酸和溴化钠反应来制备溴乙烷的装置,反应需要加热,图中省去了加热装置。有关数据见下表:
乙醇、溴乙烷、溴有关参数:
| 乙醇 | 溴乙烷 | 溴 |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(1)制备操作中,加入的浓硫酸必需进行稀释,其目的是 (选填序号)。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(2)已知加热温度较低时NaBr与硫酸反应生成NaHSO4,写出加热时A中发生的主要反应的化学方程式 。
(3)仪器B的名称 ,冷却水应从B的 (填“上”或“下”)口流进。
(4)反应生成的溴乙烷应在 中(填“A”或“C”中)。
(5)若用浓的硫酸进行实验时,得到的溴乙烷呈棕黄色,最好选择下列 (选填序号)溶液来洗涤产品。
a.氢氧化钠 b.亚硫酸钠 c.碘化亚铁 d.碳酸氢钠
洗涤产品时所需要的玻璃仪器有 。
-
某兴趣小组在实验室用乙醇、浓硫酸和溴化钠和水混合反应来制备溴乙烷,并探究溴乙烷的性质。有关数据见下表:
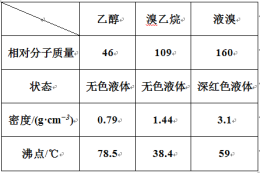
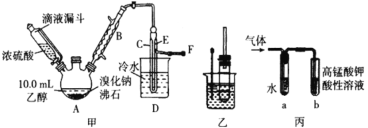
I. 溴乙烷的制备
反应原理如下,实验装置如上图(加热装置、夹持装置均省略):
H2SO4+NaBr  NaHSO4+HBr↑ CH3CH2OH+HBr
NaHSO4+HBr↑ CH3CH2OH+HBr  CH3CH2Br+H2O
CH3CH2Br+H2O
(1) 图甲中A 仪器的名称_____,图中B 冷凝管的作用为_____。
(2) 若图甲中A 加热温度过高或浓硫酸的浓度过大,均会使 C 中收集到的粗产品呈橙色,原因是A 中发生了副反应生成了_____;F 连接导管通入稀NaOH 溶液中,其目的主要是吸收_____等尾气防止污染空气
II. 溴乙烷性质的探究
用如图实验装置验证溴乙烷的性质:
(3) 在乙中试管内加入 10mL6mol·L -1NaOH 溶液和 2mL 溴乙烷,振荡、静置,液体分层,水浴加热。该过程中的化学方程式为_______。
(4) 若将乙中试管里的 NaOH 溶液换成NaOH 乙醇溶液,为证明产物为乙烯,将生成的气体通入如图丙装置。a 试管中的水的作用是_______;若无 a 试管,将生成的气体直接通入 b 试管中,则 b中的试剂可以为 _____。
-
某兴趣小组在实验室用乙醇、浓硫酸和溴化钠和水混合反应来制备溴乙烷,并探究溴乙烷的性质。有关数据见下表:
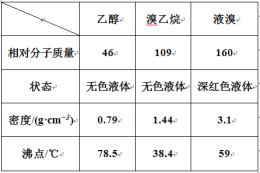
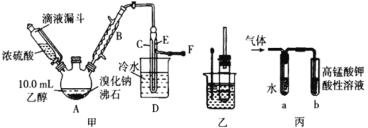
I. 溴乙烷的制备
反应原理如下,实验装置如上图(加热装置、夹持装置均省略):
H2SO4+NaBr  NaHSO4+HBr↑ CH3CH2OH+HBr
NaHSO4+HBr↑ CH3CH2OH+HBr  CH3CH2Br+H2O
CH3CH2Br+H2O
(1) 图甲中A 仪器的名称_____,图中B 冷凝管的作用为_____。
(2) 若图甲中A 加热温度过高或浓硫酸的浓度过大,均会使 C 中收集到的粗产品呈橙色,原因是A 中发生了副反应生成了_____;F 连接导管通入稀NaOH 溶液中,其目的主要是吸收_____等尾气防止污染空气
II. 溴乙烷性质的探究
用如图实验装置验证溴乙烷的性质:
(3) 在乙中试管内加入 10mL6mol·L -1NaOH 溶液和 2mL 溴乙烷,振荡、静置,液体分层,水浴加热。该过程中的化学方程式为_______。
(4) 若将乙中试管里的 NaOH 溶液换成NaOH 乙醇溶液,为证明产物为乙烯,将生成的气体通入如图丙装置。a 试管中的水的作用是_______;若无 a 试管,将生成的气体直接通入 b 试管中,则 b中的试剂可以为 _____。
-
某兴趣小组在实验室用乙醇、浓硫酸和溴化钠和水混合反应来制备溴乙烷,并探究溴乙烷的性质。有关数据见下表:
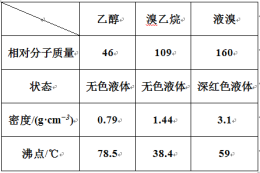
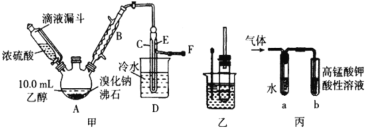
I. 溴乙烷的制备
反应原理如下,实验装置如上图(加热装置、夹持装置均省略):
H2SO4+NaBr  NaHSO4+HBr↑ CH3CH2OH+HBr
NaHSO4+HBr↑ CH3CH2OH+HBr  CH3CH2Br+H2O
CH3CH2Br+H2O
(1) 图甲中A 仪器的名称_____,图中B 冷凝管的作用为_____。
(2) 若图甲中A 加热温度过高或浓硫酸的浓度过大,均会使 C 中收集到的粗产品呈橙色,原因是A 中发生了副反应生成了_____;F 连接导管通入稀NaOH 溶液中,其目的主要是吸收_____等尾气防止污染空气
II. 溴乙烷性质的探究
用如图实验装置验证溴乙烷的性质:
(3) 在乙中试管内加入 10mL6mol·L -1NaOH 溶液和 2mL 溴乙烷,振荡、静置,液体分层,水浴加热。该过程中的化学方程式为_______。
(4) 若将乙中试管里的 NaOH 溶液换成NaOH 乙醇溶液,为证明产物为乙烯,将生成的气体通入如图丙装置。a 试管中的水的作用是_______;若无 a 试管,将生成的气体直接通入 b 试管中,则 b中的试剂可以为 _____。
-
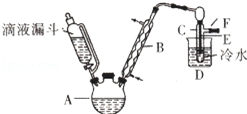
已知:R﹣OH+HX→R﹣X+H2O如图是实验室用乙醇与浓硫酸和溴化钠反应制备溴乙烷的装置,图中省去了加热装置.有关数据见表:
乙醇、溴乙烷、溴有关参数
| 乙醇 | 溴乙烷 | 溴 |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm﹣3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(1)制备操作中,加入的浓硫酸必需进行稀释,其目的是 。
a减少副产物烯和醚的生成 b.减少Br2的生成 c减少HBr的挥发 d.水是反应的催化剂
(2)加热的目的是 (从速率和限度两方面回答);应采取的加热方式是 。
(3)为除去产品中的一种主要杂质,最好选择下列溶液来洗涤产品_______。
A.氢氧化钠 B.碘化钠 C.亚硫酸钠
(4)第(3)步的实验所需要的主要玻璃仪器是 。

NaHSO4+HBr↑,写出A中生成溴乙烷的化学方程式________。











