-
关于1 mol H2O的叙述正确的是
A.含有1 mol 氢气
B.质量为18 g/mol
C.在标准状况下的体积为22.4 L
D.含有水分子的个数约为6.02×1023
难度: 中等查看答案及解析
-
如图装置所示,铜片上发生的反应为
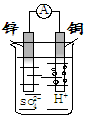
A.Zn2+ + 2eˉ = Zn
B. 2H+ + 2eˉ = H2↑
C. Zn - 2eˉ= Zn2+
D.Cu2+ + 2eˉ = Cu
难度: 中等查看答案及解析
-
下图是产生和收集气体的实验装置,该装置适合于
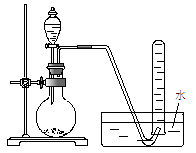
A.用H2O2溶液和MnO2反应制取O2
B.用浓盐酸和MnO2反应制取C12
C.用稀硫酸与石灰石反应制取CO2
D.用NH4C1和Ca(OH)2反应制取NH3
难度: 中等查看答案及解析
-
钢轨的野外焊接可用铝热反应。下列对铝热反应中电子转移方向和数目的表示正确的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
短周期主族元素W、R、X、Y、Z的原子序数依次增大,且分别占有三个不同的周期。W与X同主族,R与Z同主族,R最外层电子数是其内层电子数的3倍,Y是地壳中含量最多的金属元素。下列说法正确的是
A.W、X是金属元素
B.原子半径:R<Y<Z
C.简单气态氢化物的热稳定性:Z>R
D.X、Y、Z的最高价氧化物对应的水化物能相互反应
难度: 中等查看答案及解析
-
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL废液加入足量的AgNO3溶液,生成沉淀 8.61g。(2)另取10mL废液放入铜片充分反应,铜片质量减少了0.256g。下列关于原废液组成的判断正确的是
A.c(Cu2+) = c(Fe 2+)
B.c(Fe 2+)+ c(Cu2+)+ c(Fe 3+)= c(Clˉ)
C.c(Cu2+)+c(Fe 3+) = 1.4 mol / L
D.c(Fe 3+) + c(Fe 2+) = 6 mol / L
难度: 中等查看答案及解析
-
第二届青奥会“幸福之门”火炬用铝合金材料制造。铝合金属于

A.盐 B.氧化物 C.纯净物 D.混合物
难度: 简单查看答案及解析
-
医疗上给病人输液补充能量,常用的糖是
A.葡萄糖 B.麦芽糖 C.淀粉 D.纤维素
难度: 简单查看答案及解析
-
下列物质中,不与盐酸反应,但可与氢氧化钠溶液反应的是
A.Al(OH)3 B.Al2O3 C.SiO2 D.Al
难度: 中等查看答案及解析
-
下列属于共价化合物的是
A.NaCl B.CaO C.CO2 D.NaOH
难度: 中等查看答案及解析
-
某溶液中存在大量的H+、Clˉ、Fe3+,该溶液中还可能大量存在的离子是
A.OHˉ B.Ag+ C.CO
D.SO
难度: 中等查看答案及解析
-
下列物质不属于高分子化合物的是
A.淀粉 B.纤维素 C.乙酸 D.聚乙烯
难度: 简单查看答案及解析
-
今年5月7日某公司丢失铱-192放射源的事件再次敲响核安全的警钟。下列关于铱-192 (
Ir)的说法正确的是
A.原子序数为77 B.电子数为115 C.中子数为192 D.质量数为77
难度: 简单查看答案及解析
-
下列关于化学反应与能量的说法正确的是
A.中和反应是吸热反应
B.燃烧是放热反应
C.化学键断裂放出能量
D.反应物总能量与生成物总能量一定相等
难度: 简单查看答案及解析
-
煤燃烧的烟气中含有CO和SO2气体,下列关于这两种气体的说法正确的是
A.两者都易溶于水
B.两者都是有毒气体
C.两者都能使品红溶液褪色
D.两者都是形成酸雨的主要原因
难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是
A.向Ba(OH)2溶液中滴入稀硫酸:H+ + OHˉ= H2O
B.向AlCl3溶液中滴入氨水:Al3++3OHˉ= Al(OH)3↓
C.向NaHCO3溶液中滴入稀盐酸:H++HCO
= CO2↑+H2O
D.向Fe2(SO4)3溶液中加入铁粉:Fe3++Fe = 2Fe2+
难度: 中等查看答案及解析
-
下列用品的有效成分正确的是
A
B
C
D
用品




有效成分
KAl(SO4)2·12H2O
Na2CO3
C6H12O6
NaClO
难度: 中等查看答案及解析
-
下列各组物质互为同分异构体的是
A.O2和O3 B.CH3CH2CH2CH3和CH(CH3)3
C.12C和13C D.CH4和CH3CH3
难度: 中等查看答案及解析
-
可用下图所示玻璃试剂瓶(带玻璃塞)长期盛放的试剂是
A.浓硫酸 B.饱和碳酸钠溶液
C.氢氟酸 D.氢氧化钠溶液
难度: 简单查看答案及解析
-
下列实验操作不能用于物质分离的是

A B C D
难度: 中等查看答案及解析
-
下列有关表示正确的是
A.氯离子的结构示意图:

B.氯化氢分子的电子式:
C.乙烯分子的结构式:CH2=CH2
D.苯分子的比例模型:
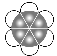
难度: 中等查看答案及解析
-
用下列方法制取氢气,反应速率最大的是
A.10℃时,粉末状锌与2 mol·L-1硫酸溶液反应
B.30℃时,粉末状锌与2mol·L-1硫酸溶液反应
C.10℃时,块状锌与2 mol·L-1硫酸溶液反应
D.30℃时,块状锌与2 mol·L-1硫酸溶液反应
难度: 中等查看答案及解析
-
下列有机反应中,不属于取代反应的是
A.CH3COOH+CH3CH2OH
CH3COOCH2CH33+H2O
B.2CH3CH2OH+O2
2CH3CHO+2H2O
C.CH4+Cl2
CH3Cl+HCl
D.
+Br2
+HBr
难度: 中等查看答案及解析