-
在盛装浓硫酸试剂瓶的标签上印有的警示标记是 ( )

难度: 中等查看答案及解析
-
下列化学用语正确的是( )
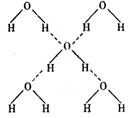
A .Na2S 的电子式:
B.Clˉ的结构示意图:
C.I—131 : 78 53I D.乙烯的结构式:CH2=CH2
难度: 中等查看答案及解析
-
用 NA 表示阿伏加德罗常数的值,下列说法正确的是( )
A.在 lmol/ L 的 AlCl3溶液中,A13+的个数小于 NA
B.1 mol 碳烯(:CH2)中含有电子数为8NA
C.标准状况下, lL 己烷的分子数为
D.1 mol C4Hl0分子中含有的共价键数无法确定
难度: 中等查看答案及解析
-
用量最大、用途最广的合金是( )
A.铁合金 B.铝合金 C.铜合金 D.钦合金
难度: 中等查看答案及解析
-
下列关系不正确的是( )
A.离子半径:Clˉ> F ˉ> Na+ > Al3+
B.熔点:石英>食盐>冰>干冰
C.结合氢离子的能力:SO42ˉ> SO32ˉ> CO32ˉ
D.热稳定性: HF > HCI > H2S > PH3
难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中可能大量共存的是 ( )
A.滴人甲基橙显红色的溶液中: Na+、NO3ˉ、 Iˉ、SO32ˉ
B.水电离出的 c(H+)= 10ˉ12 mol/L 的溶液中:K+、 AlO2ˉ、 CH3COOˉ、SiO32ˉ
C.
=10ˉ12 的溶液中: K+、ClOˉ、S2ˉ、 Clˉ
D.c(Fe 3+) = 0.1 mol/L 的溶液中: K+、ClOˉ 、SO42ˉ、 SCNˉ
难度: 中等查看答案及解析
-
能区别 NaCl 、 AgCl 、CuSO4、 MgCl2 四种固体的试剂是 ( )
A.蒸馏水 B.蒸馏水、硝酸
C.蒸馏水、氨水 D.蒸馏水、 BaC12 溶液
难度: 中等查看答案及解析
-
关于甲醛(CH2O)分子,下列说法不正确的是 ( )
①分子中碳原子采用。 SP2杂化; ②分子中所有原子处于同一平面上;
③分子中每个原子都达到 8 电子稳定结构;④分子的立体构型为四面体
A.① ② B.② ③ C.③ ④ D.① ④
难度: 中等查看答案及解析
-
下列解释原理的表达式中,不正确的是 ( )
A.镁的冶炼:
B.用热的纯碱溶液清洗油污:
C.用Na2CO3溶液处理水垢中的CaCO4:

D.用氢氟酸刻蚀玻璃:4HF+SiO2=SiF4↑+2H2O
难度: 中等查看答案及解析
-
在常温下,将一定体积的某 NaOH 溶液分成两等分,与pH 均为2的一元酸 HA、HB恰好中和,消耗两种酸溶液的体积分别为V1、V2(V1≠V2)。则下列叙述中正确的是( )
A.若 Vl>V2,则说明 HA 的酸性比 HB的酸性强
B.中和后得到的两种溶液的 pH 均为 7
C.分别将两种酸溶液稀释10 倍后溶液的 pH 均为3
D.分别往等体积的两种酸溶液中加人足量锌粉,充分反应后产生的 H2的体积相等
难度: 中等查看答案及解析
-
用下列实验装置完成对应的实验(部分仪器略去),能达到实验目的的是( )
A
B
C
D
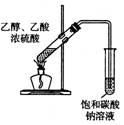
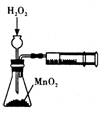
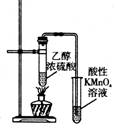
制取乙酸乙酯
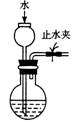
检查装置的气密性
定量测定 H2O2的分解速率
证明 CH3CH2OH 发生消去反应生成了乙烯
难度: 中等查看答案及解析
-
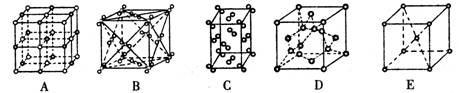
在核电荷数为26的元素Fe的原子核外3d、4s 轨道内,下列电子排布图正确的是( )
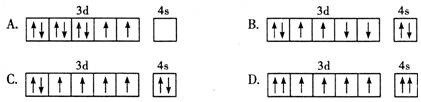
难度: 中等查看答案及解析
-
Al、Fe、Cu 都是重要的金属元素。下列说法正确的是 ( )
A.三种金属单质在常温下均可溶于浓硫酸
B.三种金属单质放置在空气中均只能生成氧化物
C.电解AlCl3、FeCl3、CuCl2 的混合溶液时阴极上依次析出Cu、Fe、Al.
D.制备AlCl3、FeCl3、CuCl2 三种固体物质,均不能采用将溶液直接蒸干的方法
难度: 中等查看答案及解析
-
右图曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,

下列叙述正确的是( )
A.盐酸的物质的量浓度为 1 mol/L
B.P 点时反应恰好完全中和,溶液呈中性
C.曲线 a 是盐酸滴定氢氧化钠的滴定曲线
D.酚酞不能用做本实验的指示剂
难度: 中等查看答案及解析
-
铁氧磁体法处理
的废水的原理可概述为:向
的酸性废水中加人FeSO4·7H2O ,将
还原为Cr3+,调节溶液的 pH,使溶液中的铁、铬元素转化为组成相当于FeⅡ[FeⅢ XCrⅢ 2-X]O4(铁氧磁体、罗马数字表示元素的价态)的沉淀。处理含 1 mol
的废水至少需要加人amol FeSO4·7H2O 。下列结论正确的是 ( )
A.x= 0.5 , a= 8 B.x = 0.5 , a=10 C .x = 1.5 , a= 8 D.x = 1.5 , a= 10
难度: 中等查看答案及解析