-
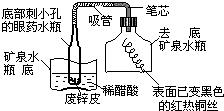
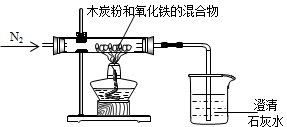
酒后驾车是一种非常严重的违章行为,交警常用“司机饮酒检测仪”检查司机呼出的气体以判断他是否饮酒,司机呼出的乙醇分子能在硫酸存在的条件下,使红色的三氧化铬变为绿色的硫酸铬,请计算出硫酸铬[Cr2(SO4)3]中的Cr元素的化合价为( )
A.+3
B.+5
C.+6
D.+7难度: 中等查看答案及解析
-
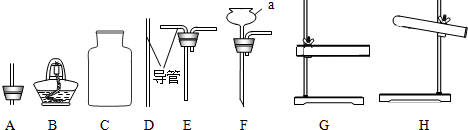
实验室制取气体选择收集方法时,对气体的下列性质不必考虑的是( )
A.颜色
B.密度
C.溶解性
D.是否与水反应难度: 中等查看答案及解析
-
下列各组离子在水溶液中能大量共存的是( )
A.Fe2+、Ca2+、CO32-、OH-
B.Na+、SO42-、Cl-、OH-
C.Ba2+、H+、Cl-、OH-
D.Ag+、NH4+、NO3-、OH-难度: 中等查看答案及解析
-
能证明分子在化学变化中可分的是( )
A.打开汽水瓶,有气体逸出
B.10mL水与10mL酒精混合,体积小于20mL
C.加热氧化汞得银白色汞与氧气
D.水蒸发为水蒸气难度: 中等查看答案及解析
-
实验室中有饱和食盐水和蒸馏水各一瓶,为了区分它们,某学习小组的同学设计了以下四种方案.你认为不能把两者区分开来的是( )
A.进行导电性试验,能导电的是饱和食盐水
B.压强计来测定同深度处的压强,压强较大的是饱和食盐水
C.再加入少量食盐晶体,晶体不能继续溶解的是饱和食盐水
D.通过显微镜观察,能看到钠离子的是饱和食盐水难度: 中等查看答案及解析
-
人类探测月球发现,月球土壤中含有较丰富的质子数为2,中子数为l的氦原子.则氦原子中的电子数为( )
A.1
B.2
C.3
D.4难度: 中等查看答案及解析
-
荣获2009年诺贝尔化学奖的是英国剑桥大学科学家文卡特拉曼•拉马克里希南、美国科学家托马斯•施泰茨和以色列科学家阿达•约纳特因,他们在对“核糖体结构和功能的研究”上作出了杰出的贡献.核糖体是进行蛋白质合成的重要细胞器,蛋白质是一类非常复杂的化合物,由碳、氢、氧、氮、硫等元素组成,蛋白质在酸、碱或酶的作用下能发生水解反应生成氨基酸,氨基酸分子中含有氨基(-NH2,具有碱的性质)和羧基(-COOH,具有酸的性质).氨基酸分子具有的性质是( )
A.只能与硫酸反应,不能与氢氧化钠反应
B.只能与氢氧化钠反应,不能与硫酸反应
C.既能与硫酸反应,又能与氢氧化钠反应
D.既不能与硫酸反应,又不能与氢氧化钠反应难度: 中等查看答案及解析
-
我们在实验室看到的浓硝酸往往呈黄色,这是由于硝酸的化学性质不稳定、分解生成NO2的缘故.纯净的硝酸或浓硝酸在常温下见光或受热就会分解,有关反应为:见光或受热4HNO3═2H2O+4NO2↑+O2↑.为防止硝酸的分解,下列贮存硝酸的方法中你认为合理的是( )
A.无色试剂瓶
B.棕色试剂瓶
C.无色试剂瓶并置于阴凉处
D.棕色试剂瓶并置于阴凉处难度: 中等查看答案及解析
-
在25℃时,向足量的饱和碳酸钠溶液中加入1.06克无水碳酸钠,搅拌后静置,最终析出晶体的质量( )
A.等于1.06克
B.大于1.06克而小于2.86克
C.等于2.86克
D.大于2.86克难度: 中等查看答案及解析
-
实验室使用大理石和盐酸反应制取的CO2是不纯净的,为证明该气体中含有多种物质,所用的试剂及使用顺序正确的是
( )
A.无水硫酸铜、硝酸银溶液、石灰水
B.浓硫酸、氢氧化钠溶液、石灰水
C.硝酸银溶液、石灰水、无水硫酸铜
D.氯化钙、石蕊试液、水难度: 中等查看答案及解析
-
下列解释不科学的是( )
A.在溶洞中,当溶有Ca(HCO3)2的水液发生分解,析出固体(在洞顶或洞底),日久天长便形成了钟乳石
B.长期盛放NaOH溶液的试剂瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气压小于瓶外大气压的缘故
C.“通风橱”是利用排风扇将橱内废气直接排放到室外的装置,它是一种不完善的防污设施
D.高压氧舱可治疗煤气中毒,原因是和血红蛋白结合的CO跟氧气反应生成无毒的CO2难度: 中等查看答案及解析
-
1.6g某物质在氧气中完全燃烧生成4.4g二氧化碳和3.6g水,关于该物质的组成有下列论断:
①一定含C、H;②一定不含O;③可能含O;④一定含O;⑤分子中C、H的原子个数比为1:2;⑥分子中C、H的原子个数比为1:4.其中正确的是( )
A.①②⑥
B.①②⑤
C.①③⑥
D.①④⑤难度: 中等查看答案及解析
-
托盘天平调零后,在左盘衬纸上置氧化铜粉末,右盘衬纸上置1个5g砝码,游码标尺示数如图,此时天平平衡.则被称量的氧化铜质量为( )
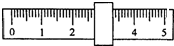
A.8.3 g
B.7.7 g
C.3.3 g
D.2.7 g难度: 中等查看答案及解析
-
下列所示的图象能反映相对应实验的是( )
A.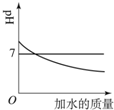 向pH=12的Ca(OH)2溶液中不断加水稀释
向pH=12的Ca(OH)2溶液中不断加水稀释
B.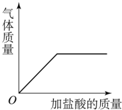 向碳酸钙固体中逐滴加入稀盐酸至过量
向碳酸钙固体中逐滴加入稀盐酸至过量
C.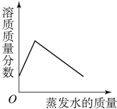 在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
D.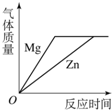 将足量的金属镁片和锌片分别和等质量的相同质量分数的稀硫酸混合
将足量的金属镁片和锌片分别和等质量的相同质量分数的稀硫酸混合 难度: 中等查看答案及解析
-
冬天,人们常用甘油溶液护肤,使皮肤保持湿润.质量分数为80%的甘油溶液护肤效果最佳.配制80%的甘油溶液500g,所需甘油的质量为( )
A.80 g
B.40 g
C.100 g
D.400 g难度: 中等查看答案及解析