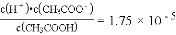-
用标准浓度的NaOH溶液滴定未知浓度的盐酸时下列情况会使盐酸物质的量浓度偏低的是( )
A. 碱式滴定管用蒸馏水洗净后,直接注入标准浓度的NaOH溶液
B. 碱式滴定管尖端有气泡,滴定后气泡消失
C. 记录消耗的碱液,滴定前平视,滴定后俯视凹液面
D. 锥形瓶用蒸馏水洗净后,直接装入未知浓度的盐酸
难度: 中等查看答案及解析
-
将纯水加热至较高温度,下列叙述正确的是
A、水的离子积变大,pH变小,呈酸性
B、水的离子积不变,pH不变,呈中性
C、水的离子积变小,pH变大,呈碱性
D、水的离子积变大,pH变小,呈中性
难度: 简单查看答案及解析
-
“84”消毒夜在日常生活中被广泛使用。该消毒液无色,pH大于7,对某些有色物质有漂白作用。你认为它可能的有效成分是( )
A. SO2 B. Na2CO3 C. KMnO4 D. NaClO
难度: 简单查看答案及解析
-
准确移取20.00 mL某待测HCl溶液于锥形瓶中,用0.100 0 mol·L-1NaOH溶液滴定。 下列说法正确的是( )
A. 滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B. 随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C. 用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D. 滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
难度: 中等查看答案及解析
-
下列有关滴定操作的顺序正确的是( )
①检查滴定管是否漏水 ②用蒸馏水洗涤玻璃仪器
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管
④装标准溶液和待测液并调整液面(记录初读数)
⑤取一定体积的待测液于锥形瓶中 ⑥滴定操作
A. ①③②④⑤⑥ B. ①②③④⑤⑥ C. ②③①④⑤⑥ D. ④⑤①②③⑥
难度: 简单查看答案及解析
-
关于pH的测定下列说法正确的是
A. pH试纸在使用之前应用蒸馏水润湿
B. 用广泛pH试纸测得某盐酸的pH=2.3
C. 利用酸碱指示剂可以测溶液的pH
D. pH计是精确测定溶液pH的仪器
难度: 简单查看答案及解析
-
对滴有酚酞试液的下列溶液,操作后颜色变深的是
A. 明矾溶液加热 B. CH3COONa溶液加热
C. 氨水中加入少量NH4Cl固体 D. 小苏打溶液中加入少量NaCl固体
难度: 中等查看答案及解析
-
下图曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,下列叙述正确的是( )
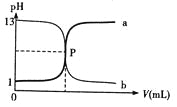
A. 盐酸的物质的量浓度为 1 mol/L
B. P 点时反应恰好完全中和,溶液呈中性
C. 曲线 a 是盐酸滴定氢氧化钠的滴定曲线
D. 酚酞不能用做本实验的指示剂
难度: 困难查看答案及解析
-
下列事实不属于盐类水解应用的是
A. 明矾净水
B. 使用热的纯碱溶液去除油污
C. 实验室配制FeCl3溶液时加入少量稀盐酸
D. 向FeCl3溶液中加入NaOH溶液产生红褐色沉淀
难度: 中等查看答案及解析
-
在以下各种情形下, 下列电离方程式的书写正确的是( )
A. 熔融状态下的NaHSO4电离:NaHSO4
Na++H++SO42-
B. H2CO3的电离:H2CO3
2H++CO32-
C. Fe(OH)3的电离:Fe(OH)3
Fe3++3OH-
D. 水溶液中NaHSO4的电离:NaHSO4
Na++HSO4-
难度: 中等查看答案及解析
-
60 mL 0.5 mol/L的氢氧化钠溶液和40 mL 0.4 mol/L的硫酸相混合后,溶液的pH约为( )
A. 0.5 B. 1.7 C. 2 D. 13.2
难度: 简单查看答案及解析
-
H2S水溶液中存在电离平衡H2S
H++HS-和HS-
H++S2-。若向H2S溶液中
A. 加水,平衡向右移动,溶液中氢离子浓度增大
B. 通入过量SO2气体,平衡向左移动,溶液pH值增大
C. 滴加新制氯水,平衡向左移动,溶液pH值减小
D. 加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 强电解质一定是离子化合物,弱电解质一定是共价化合物
B. 强电解质一定是易溶化合物,弱电解质一定是难溶化合物
C. SO3溶于水后水溶液导电性很强,所以SO3是强电解质
D. 属于共价化合物的电解质在熔化状态下一般不导电
难度: 简单查看答案及解析
-
下列关于室温下氨水的叙述,正确的是( )
A. 同pH同体积的氨水和NaOH溶液,能分别与同浓度同体积的盐酸恰好完全中和
B. 加水稀释0.10 mol•L-1的氨水,溶液中n(OH-)减小
C. 若温度不变,在氨水中加入少量NH4Cl固体,氨水的电离度和电离平衡常数均变小
D. 氨水中的离子浓度关系满足:c(OH-)=c(H+)+c(NH4+)
难度: 困难查看答案及解析
-
将0.1 mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时都会引起( )
A. CH3COOH电离程度变大 B. 溶液pH减小 C. 溶液的导电能力减弱 D. 溶液中c(H+)减小
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 在一定温度下AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数;
B. AgCl的Ksp= 1.8×10-10mol2·L-2,在任何含AgCl固体的溶液中,c(Ag+) = c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10mol2·L-2;
C. 温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液;
D. 向饱和AgCl水溶液中加入盐酸,Ksp值变大。
难度: 中等查看答案及解析
-
把下列物质的水溶液加热蒸干后,能得到原溶质的是
A. NaHCO3 B. FeCl3 C. KCl D. Al(NO3)3
难度: 简单查看答案及解析
-
下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
A 相同浓度的两溶液中c(H+)相同
B 100mL 0.1mol/L的两溶液能中和等物质的量的氢氧化钠
C pH=3的两溶液稀释100倍,pH都为5
D 两溶液中分别加人少量对应的钠盐,c(H+)均明显减小
难度: 简单查看答案及解析
-
向三份0.1
, 溶液中分别加入少量
、
、
固体(忽略溶液体积变化),则
浓度的变化依次为( )。
A. 减小、增大、减小 B. 增大、减小、减小
C. 减小、增大、增大 D. 增大、减小、增大
难度: 简单查看答案及解析
-
下列有关盐类水解的说法中,不正确的是( )。
A. 盐类的水解过程破坏了纯水的电离平衡
B. 盐类的水解是酸碱中和反应的逆反应
C. 盐类水解后的溶液不一定显中性
D.
溶液中,
是
的两倍
难度: 简单查看答案及解析
-
在一定条件下,
溶液中存在水解平衡:
。下列说法正确的是
A. 稀释溶液,促进
的水解,
增大
B. 通入
,平衡向正反应方向移动
C. 升高温度,
减小
D. 加入
固体,溶液
减小
难度: 中等查看答案及解析
-
下列有关离子水解的方程式中正确的是( )。
A.
溶液:
B.
溶液:
C.
溶液:
D.
溶液:
难度: 简单查看答案及解析
-
对H2O的电离平衡不产生影响的粒子是( )
A.
B. 26Fe3+ C.
D.
难度: 中等查看答案及解析
-
某酸式盐NaHY的水溶液c(OH-)>c(H+),下列叙述正确的是
A. H2Y的电离方程式:H2Y
2H++Y2-
B. HY-的水解方程式:HY-+ H2O
H3O++ Y2-
C. 该酸式盐溶液中离子浓度关系:c(Na+)>c(HY-)>c(OH-)>c(H+)
D. 该酸式盐溶液中离子浓度关系:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
难度: 困难查看答案及解析
-
在25℃时,在浓度为1 mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的溶液中,测得其c(NH4+)分别为a、b、c(单位为mol/L),下列判断正确的是( )
A. a=b=c B. a > b >c C. a > c >b D. c > a > b
难度: 中等查看答案及解析