-
用水壶烧开水,水沸腾后壶盖被顶起,说明( )
A. 分子间空隙增大 B. 分子的质量很小
C. 分子的体积变大 D. 分子是由原子构成的
难度: 简单查看答案及解析
-
为了减轻大气污染,自2018年2月1日起,扬州市禁止燃放烟花爆竹,下列标识中属于“禁止燃放烟花爆竹”的是( )
A.
 B.
B. 
C.
 D.
D. 
难度: 简单查看答案及解析
-
下列过程仅包含物理变化的是
A.光合作用 B.干冰升华 C.煤的燃烧 D.金属锈蚀
难度: 简单查看答案及解析
-
下列物质由离子构成的是
A.A1 B.H2O C.CO2 D.NaCl
难度: 简单查看答案及解析
-
可用装有 K2Cr2O7 的仪器检查司机是否酒驾。K2Cr2O7 中 Cr 元素的化合价为
A.+ 2 价 B.+5 价 C.+6 价 D.+7 价
难度: 简单查看答案及解析
-
下列实验现象的描述正确的是
A.木炭在空气中燃烧,生成黑色物质
B.红磷燃烧,生成大量白色烟雾
C.铁丝在氧气中燃烧,火星四射,放出大量的热,生成黑色固体
D.铜在空气中加热,固体由黑色变成红色
难度: 简单查看答案及解析
-
下列物质中含有自由移动的氯离子的是
A. 氯化钠晶体 B. 氯化氢气体 C. 氯酸钾溶液 D. 食盐水
难度: 简单查看答案及解析
-
下列有关溶液的叙述正确的是
A. 均一、稳定的液体一定是溶液 B. 洗涤剂去油污是乳化现象
C. 豆浆、牛奶都是溶液 D. 溶液都是无色的
难度: 中等查看答案及解析
-
下列有关实验操作中不正确的是
A.
检查装置气密性 B.
 液体加热 C.
液体加热 C. 倾倒液体 D.
倾倒液体 D.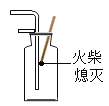 氧气验满
氧气验满难度: 中等查看答案及解析
-
下列化学方程式书写正确的是
A.4Fe + 3O2 = 2Fe2O3
B.2Fe+6HCl = 2FeCl3+3H2↑
C.Cu + FeSO4 = Fe + CuSO4
D.H2O2 = H2↑ + O2↑
难度: 简单查看答案及解析
-
下列各组物质,仅用水无法鉴别的是
A.CuSO4、NaCl B.CaCl2、NaCl C.CaCO3、NaCl D.NH4NO3、NaCl
难度: 中等查看答案及解析
-
科学家用滤纸和二氧化钛(TiO2)制得纳米纸,在纳米纸上铺一层萘胺(C10H9N)又制得一种试纸,可用于检测食品中亚硝酸盐浓度的高低。下列说法正确的是
A.这种试纸是一种新型化合物
B.萘胺中氢元素的质量分数最小
C.二氧化钛中钛元素的化合价为﹢2
D.萘胺中碳、氢元素的质量比为10︰9
难度: 中等查看答案及解析
-
化学知识有助于我们正确认识、理智选择、科学生活。下列说法不正确的是
A.用铁矿石和焦炭在高炉内炼钢
B.常用“加铁酱油”有助于预防贫血
C.重要图书档案着火用液态二氧化碳灭火器扑灭
D.室外发生火灾时,用湿毛巾捂住口鼻,并及时逃离现场
难度: 简单查看答案及解析
-
逻辑推理是化学学习常用的思维方法。下列推理正确的是
A.氧化物中都含有氧元素,所以含有氧元素的化合物都是氧化物
B.在同一化合物中,若金属元素显正价,则非金属元素一定显负价
C.铁和铜都是金属,铁与稀硫酸反应产生氢气,则铜也能与稀盐酸反应产生氢气
D.点燃可燃性气体前需要检验纯度,所以点燃一氧化碳前也需要检验纯度
难度: 简单查看答案及解析
-
某物质和二氧化碳反应后只生成碳酸钠和氧气,则该物质中 ( )
A.只含氧元素 B.一定含钠元素和氧元素
C.只含钠元素 D.一定含钠元素,可能含氧元素
难度: 简单查看答案及解析
-
等质量的同一种稀硫酸分别和金属 X、Y 反应,产生气体的质量与金属质量变化的图像。下列说法不正确的是
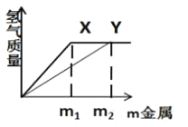
A.金属 X 比金属 Y 活泼
B.m1 时,产生气体的质量:X>Y
C.m2 时,消耗金属的质量:X<Y
D.m2 时,消耗稀硫酸的质量:X=Y
难度: 困难查看答案及解析