-
逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
A. 因为CO和CO2的组成元素相同,所以它们的化学性质相同
B. 中和反应的产物是盐和水,有盐和水生成的反应都是中和反应
C. 化合物含有不同种元素,不同种元素组成的纯净物一定是化合物
D. 因为碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液
难度: 简单查看答案及解析
-
坚持人与自然和谐共生,建设生态文明是中华民族永续发展的千年大计,下列做法不利于保护环境的是( )
A. 大力植树造林,增加植被面积 B. 实施雨污分流,构建海绵城市
C. 大量施用化肥,提高粮食产量 D. 垃圾分类回收,循环利用资源
难度: 简单查看答案及解析
-
食醋是厨房中常用的调味品,它的主要成分是乙酸(CH3COOH)。下列有关乙酸的说法中,正确的是
A. 乙酸是由乙酸分子构成
B. 乙酸是由2个碳原子、4个氢原子、2个氧原子构成
C. 乙酸中共含有8个原子
D. 乙酸分子是由碳、氢,氧三种元素组成
难度: 简单查看答案及解析
-
下列工艺制品的制造过程无需发生化学变化的是( )
A.
 玻璃花瓶 B.
玻璃花瓶 B.  青铜鼎
青铜鼎C.
 青花瓷器 D.
青花瓷器 D.  汉白玉雕塑
汉白玉雕塑难度: 简单查看答案及解析
-
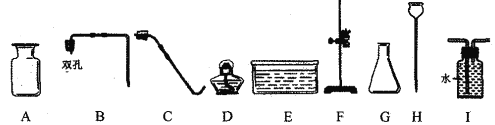
如图所示的实验操作正确的是
A.
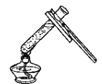 加热液体 B.
加热液体 B. 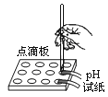 测定溶液pH
测定溶液pHC.
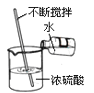 稀释浓硫酸 D.
稀释浓硫酸 D. 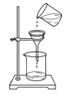 过滤
过滤难度: 简单查看答案及解析
-
在点燃条件下,A与B反应生成C和D,反应前后分子种类变化的微观示意图如图示:
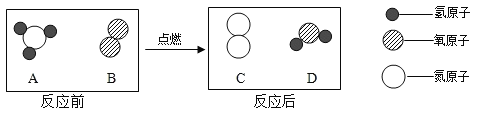
A. 该反应的本质是原子的重新组合
B. 该反应中,分子个数发生了改变
C. 该反应属于置换反应
D. 该反应中,参加反应的A与B的分子数比为1:1
难度: 简单查看答案及解析
-
下列排序正确的是( )
A. 地壳中元素的含量
B. 硫元素的化合价:
C. 溶液的pH:
D. 溶解时放出的热量
难度: 简单查看答案及解析
-
稀NaOH溶液与稀盐酸反应过程中温度和pH的变化如图所示。下列说法正确的是( )
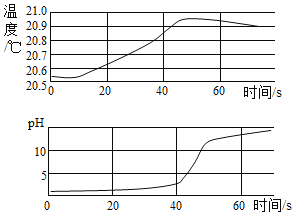
A. 该实验是将稀盐酸滴入稀NaOH溶液
B. 稀NaOH溶液与稀盐酸反应为吸热反应
C. 在40s到50s某时刻,两溶液恰好完全反应
D. 在温度达到最高值前,溶液中只有
和
两种离子
难度: 简单查看答案及解析
-
如图是a、b、c三种物质的落溶解度曲线,说法错误的是( )
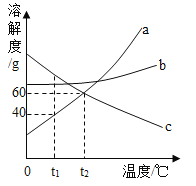
A. t2℃时,a、c两种物质的溶解度相同
B. 升高温度可使饱和的c溶液变为不饱和溶液
C. t1℃时,三种物质的溶解度大小的顺序是c>b>a
D. 将t2℃时a、b、c的饱和溶液同时降温至t1℃后,析出晶体最多的物质是a
难度: 简单查看答案及解析
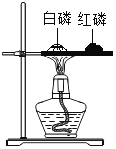 比较红磷、白磷着火点
比较红磷、白磷着火点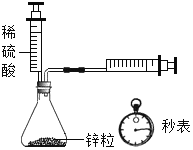 测定锌和稀硫酸反应速率
测定锌和稀硫酸反应速率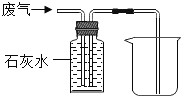 除去废气中的CO,并收集
除去废气中的CO,并收集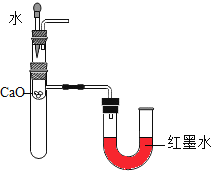 验证CaO和水反应是放热反应
验证CaO和水反应是放热反应