-
下列说法错误的是
A. 蔗糖、果糖和麦芽糖均为双糖
B. 植物油硬化过程中发生了加成反应
C. 加热能杀死流感病毒是因为蛋白质受热变性
D. 加工后具有吸水性的植物纤维可用作食品干燥剂
难度: 中等查看答案及解析
-
已知C6H14有多种同分异构体,则其同分异构体中沸点最高的分子的一氯取代物的种数是
A.2 B.3 C.4 D.5
难度: 简单查看答案及解析
-
以溴乙烷为原料,用下述六种反应的类型:(1)氧化(2)消去(3)加成(4)酯化(5)水解(6)加聚来合成乙二酸乙二酯的正确顺序
A. (1)(5)(2)(3)(4) B. (1)(2)(3)(4)(5)
C. (2)(3)(5)(1)(4) D. (2)(3)(5)(1)(6)
难度: 困难查看答案及解析
-
下列物质既能发生消去反应生成相应的烯烃,不能氧化生成相应醛的是
A. CH3 OH B. CH3CH2CH2OH
C.
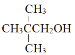 D.
D. 难度: 中等查看答案及解析
-
已知化合物B3N3H6(硼氮苯)与苯的分子结构相似,分别为
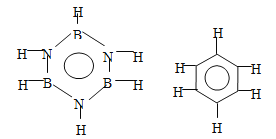
则硼氮苯的二氯取代物(B3N3H4Cl2)的同分异构体的数目为 ( )
A. 2 B. 3 C. 4 D. 5
难度: 简单查看答案及解析
-
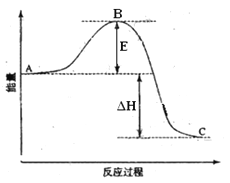
已知氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1 mol氢气的化学键消耗的能量为Q1 kJ,破坏1 mol氯气的化学键消耗的能量为Q2kJ ,形成1 mol氯化氢的化学键释放的能量为Q3kJ,下列关系式正确的是
A. Q1 + Q2 > Q3 B. Q1 + Q2 < Q3 C. Q1 + Q2 > 2Q3 D. Q1 + Q2 < 2Q3
难度: 简单查看答案及解析
-
下列热化学方程式中△H代表燃烧热的是
A. C6H12O6 (s) + 6O2 (g) = 6CO2 (g) + 6H2O (l);△H1
B. H2(g) + 1/2O2 (g) = H2O (g) ;△H2
C. CH4 (g) + 3/2O2 (g) = 2H2O (l) + CO (g);△H3
D. 2CO (g) + O2 (g) = 2CO2 (g);△H4
难度: 简单查看答案及解析
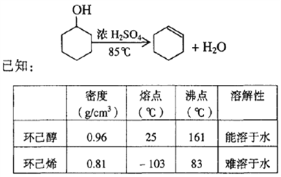
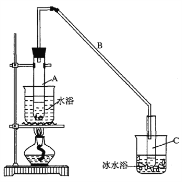
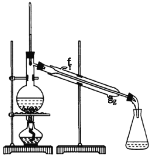
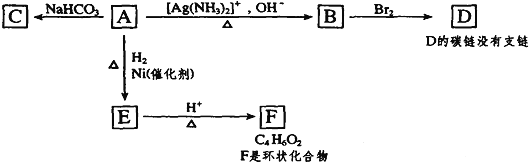
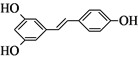 )属二苯乙烯类多酚化合物,具有抗氧化、抗癌和预防心血管疾病的作用。某课题组提出了如下合成路线:
)属二苯乙烯类多酚化合物,具有抗氧化、抗癌和预防心血管疾病的作用。某课题组提出了如下合成路线: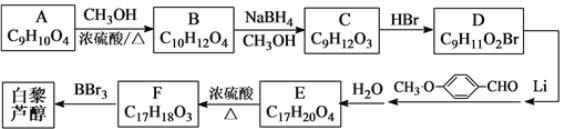
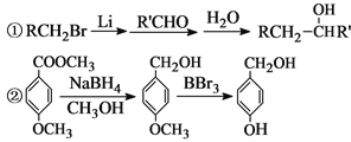 。
。 有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:_____________________________________________________。
有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:_____________________________________________________。