-
(7分)2SO2(g) + O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99 kJ·mol-1。
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99 kJ·mol-1。
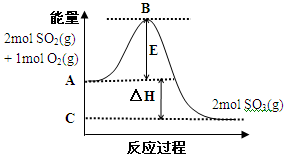
请回答下列问题:
 (1)已知图中C 点表示2mol SO3(g)的总能量,则A点表示: ;E所代表的能量是 ;E的大小对该反应的反应热 影响。(填“有”或“无”)。
(1)已知图中C 点表示2mol SO3(g)的总能量,则A点表示: ;E所代表的能量是 ;E的大小对该反应的反应热 影响。(填“有”或“无”)。
 (2)图中△H= kJ·mol-1。
(2)图中△H= kJ·mol-1。
-
(10分)2SO2(g) + O2(g) = 2SO3 (g)反应过程的能量变化如图所示。已知1mol SO2 (g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。请回答下列问题:
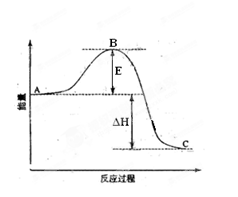
(1)图中A、C分别表示,E的大小对该反应的反应热
(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点________(填“升高”或“降低”),△H________(填“变大”、“变小”或“不变”),
 (2)图中△H=KJ·mol-1;
(2)图中△H=KJ·mol-1;
-
2SO2(g)+O2(g)⇌2SO3(g),反应过程的能量变化如图所示.
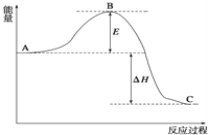
已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ/mol.
请回答下列问题:
(1)E的大小对该反应的反应热 ______ 影响?(填“有”或“无”).该反应通常用V2O5作催化剂,加V2O5会使图中B点 ______ (填“升高”或“降低”);
(2)图中△H= ______ kJ/mol;
(3)如果反应速率υ(SO2)为0.05mol/(L•min),则υ(O2)= ______ mol/(L•min);
(4)1molSO2(g)氧化为1mol SO3(g)的反应热△H1 ______ 1mol SO3(g)还原为1mol SO2(g)的反应热△H2(填“>、<或=”) 。
(5)已知单质硫的燃烧热为296kJ/mol,计算由S(s)生成3mol SO3(l)的△H= _________________
-
已知2SO2(g)十O2(g) 2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
(1)1mol SO2(g)氧化为1mol SO3(g)放出的热量为99.00kJ·mol-1,写出该反应的热化学方程式 。
(2)①在图中标出该反应的活化能E和反应热△H;
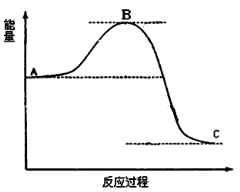
②该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低,请在图中画图表示出来,并进行必要的标注。
(3)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 。
A.容器中气体总压强不变
B.容器中混合气体的密度不变
C.每生成1mol SO3的同时生成1molSO2
D.SO2、O2、SO3的物质的量之比为2∶1∶2
(4)在400℃,常压下,向体积为2L的密闭容器中充入2mol SO2(g)和1.92mol O2(g),充分反应后,达平衡时测得还有0.04molL-1 SO2剩余,求该反应在平衡时O2 的转化率及SO3的物质的量浓度(要求写出三段式计算过程)。
-
(10分)2SO2(g)+ O2 (g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH = - 99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH = - 99 kJ·mol-1
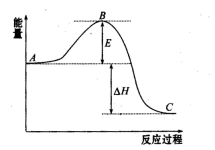
请回答下列问题:
(1)图中A表示_____________________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________。
(2)图中ΔH = __________ kJ·mol-1。
(3)如果反应速率v(SO2)为0.06 mol·L-1·min-1,则v(O2)为__________ mol·L-1·min-1。
(4)已知S(s) + O2(g) = SO2(g) ΔH = - 296 kJ·mol-1,则由S(s)生成5 mol SO3(g)的ΔH= kJ·mol-1。
-
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=﹣99kJ•mol﹣1.请回答下列问题:
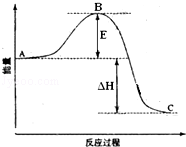
(1)图中A、C分别表示 ,E的大小对该反应的反应热 (填“有”或“无”)影响.该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”还是“降低”),△H (填“变大”、“变小”或“不变”),理由是
(2)图中△H= KJ•mol﹣1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5.写出该催化循环机理的化学方程式 、 .
-
(16分) 2SO2(g) + O2(g) = 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH= —99kJ·mol-1.请回答下列问题:
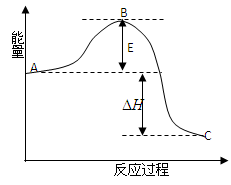
(1)图中A、C分别表示________、________,E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是________;
 (2)图中△H=________KJ·mol-1;
(2)图中△H=________KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自 身被还原为四价钒氧化物;四价钒氧化物再被氧气氧化。写出该催化循环机理的化学方程式
________、________;
 (4)已知单质硫的燃烧热为296 KJ·mol-1,写出硫的燃烧热方程式:________
(4)已知单质硫的燃烧热为296 KJ·mol-1,写出硫的燃烧热方程式:________
计算由S(s)生成2molSO3(g)的△H________KJ·mol-1。
-
(14分)2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。、
2SO3(g)反应过程的能量变化如图所示。、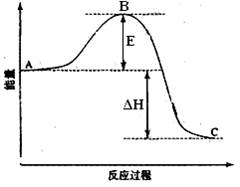
已知1mol SO2(g)氧化为1mol SO3的ΔH= -99kJ·mol—1.请回答下列问题:(1)图中A、C分别表示________、
________,E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________ ,并说明理由________;
(2)图中△H=________;
(3)如果反应速率v(SO2)为0.05 mol·L—1·min—1,则v(O2)=________mol·L—1·min—1
(4)已知单质硫的燃烧热为296 KJ·mol—1,计算由S(s)生成3 molSO3(g)的△H________(要有计算过程)。
-
 (8分)2SO2(g)+O2(g)
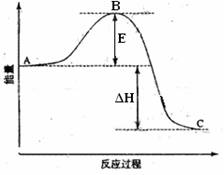
(8分)2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的
ΔH= —99kJ·mol—1.请回答下列问题:
(1)图中A、C分别表示________、 ________, E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是;
(2)图中△H=KJ·mol—1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式________,
________。
-
2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
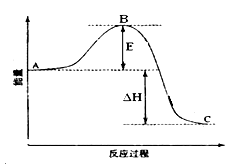
已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。
请回答下列问题:
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热 (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”还是“降低”),△H (填“变大”、“变小”或“不变”)。
(2)图中△H= kJ·mol-1;
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= - 24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= - 47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:








 (8分)2SO2(g)+O2(g)
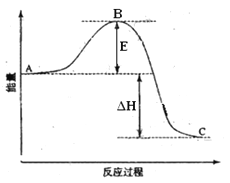
(8分)2SO2(g)+O2(g) 