-
下列变化中,需加氧化剂才能实现的是
A. H2O→H2 B. FeCl3→FeCl2 C. C→CO2 D. CaO→Ca(OH)2
难度: 简单查看答案及解析
-
根据物质的组成进行分类,O2属于
A. 单质 B. 氧化物 C. 化合物 D. 混合物
难度: 简单查看答案及解析
-
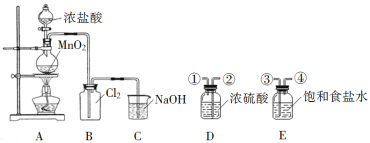
仪器的名称为“锥形瓶”的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列物质中,易溶于水的是
A. KNO3 B. BaCO3 C. AgCl D. CuO
难度: 简单查看答案及解析
-
下列属于非电解质的是
A. 氨水 B. 蔗糖 C. 氢氧化钾 D. 铜
难度: 简单查看答案及解析
-
Na2O+H2O=2NaOH的反应类型属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
难度: 简单查看答案及解析
-
下列物质溶于水后溶液显酸性的是
A. NaCl B. Na2O C. NH3 D. Cl2
难度: 简单查看答案及解析
-
下列属于电解质的是
A. 氯化钠 B. 酒精 C. 氯气 D. 铁
难度: 简单查看答案及解析
-
下列金属元素的单质或化合物在火焰上灼烧时,焰色为紫色的是
A. 钠 B. 钾 C. 镁 D. 铁
难度: 简单查看答案及解析
-
在化学反应2KI+Cl2=2KCl+I2中,作还原剂的是
A. KI B. Cl2 C. KCl D. I2
难度: 简单查看答案及解析
-
下列物质中,不能与金属钠反应的是
A. 氯气 B. 水 C. 盐酸 D. 煤油
难度: 简单查看答案及解析
-
下列物质溶于水后不能电离的是
A. 葡萄糖(C6H12O6) B. 氯化氢(HCl)
C. 氯化钠(NaCl) D. 氢氧化钡[Ba(OH)2]
难度: 简单查看答案及解析
-
NaH与水反应的方程式为:NaH+H2O=NaOH+H2↑,在该反应中H2O
A. 失去电子 B. 被氧化
C. 发生氧化反应 D. 是氧化剂
难度: 中等查看答案及解析
-
石灰石是许多工业的原料之一,但制取下列物质不需用石灰石的是
A. 制漂白粉 B. 炼铁 C. 制生石灰 D. 制烧碱
难度: 中等查看答案及解析
-
下列离子方程式正确的是
A. Zn与稀H2SO4反应:Zn+H+=Zn2++H2↑
B. Na2CO3溶液与足量盐酸反应:CO32-+2H+=H2O+CO2↑
C. Cl2与NaOH溶液反应:Cl2+2OH-=2Cl-+H2O
D. MgC12溶液与过量氨水反应:Mg2++2OH-=Mg(OH)2↓
难度: 中等查看答案及解析
-
下列关于氯水的说法中,不正确的是
A. 氯水是指液态的氯 B. 新制氯水呈黄绿色
C. 新制氯水具有漂白作用 D. 新制氯水应避光保存
难度: 中等查看答案及解析
-
下列说法正确的是
A. 可用蒸发结晶的方法从碘水中提取碘单质
B. 碘化银可用于人工降雨
C. 酒精在实验台上着火可用水作灭火剂
D. 氢气还原氧化铜要先加热再通氢气
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A. 钠与水反应:Na+2H2O=Na++2OH-+H2↑
B. 氯气通入溴化钠溶液中:Cl2+2Br-=2Cl-+Br2
C. 硫酸铜溶液与氢氧化钡溶液混合:SO42-+Ba2+=BaSO4↓
D. CaCO3与稀盐酸反应:CO32-+2H+=CO2↑+H2O
难度: 简单查看答案及解析
-
下列说法不正确的是
A. 胶体属于纯净物
B. 可用丁达尔效应区分胶体与溶液
C. 氢氧化铁胶体能吸附水中的悬浮颗粒并沉降而用于净水
D. 胶体分散质粒子的直径在10-9~10-7m之间
难度: 简单查看答案及解析
-
下列各组离子中,能在强酸性溶液中大量共存的是
A. Na+、K+、SO42-、OH- B. Na+、K+、Cl-、HCO3-
C. Na+、Cu2+、CO32-、Br- D. Na+、Mg2+、NO3-、Cl-
难度: 中等查看答案及解析
-
下列说法正确的是
A. 铜在自然界中主要以单质的形式存在
B. 工业上常用电解饱和食盐水的方法制备金属钠
C. 工业上常用焦炭在高温下直接将氧化铁还原炼铁
D. 在海水中加入石灰乳可得氢氧化镁沉淀,这是从海水中富集镁的基本方法
难度: 简单查看答案及解析
-
将一小粒金属钠投入到盛有冷水的小烧杯中,以下描述合理的是
A. 无明显现象 B. 烧杯内溶液颜色逐渐变红
C. 金属钠浮于液面上,四处游动 D. 金属钠沉入烧杯底部,并产生气泡
难度: 简单查看答案及解析
-
用NA代表阿伏加德罗常数的值,下列说法正确的是
A. 常温常压下,11. 2 L 二氧化硫气体中含有0. 5NA个SO2分子
B. 标准状况下,22. 4 L CCl4中含有NA个分子
C. 1 mol Na与一定量的O2反应生成Na2O和Na2O2,转移的电子数为NA个
D. 将NA个HCl气体分子溶于1 L水中得到1 mol·L-1的盐酸
难度: 简单查看答案及解析
-
下列除去杂质(括号的物质为杂质)的方法中,错误的是
A. FeCl3溶液(FeCl2):通入适量Cl2
B. CO(CO2):通过NaOH溶液洗气后干燥
C. MnO2(KCl):加水溶解后过滤、洗涤、烘干
D. CO2(HCl):通过饱和Na2CO3溶液洗气后干燥
难度: 中等查看答案及解析
-
下列操作对应的现象不符合事实的是
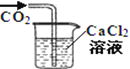

A.将二氧化碳气体通入CaCl2溶液,不会产生白色沉淀
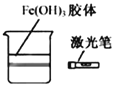
B.用激光笔照射Fe(OH)3胶体,产生“丁达尔效应”
C.将湿润的有色布条放入盛有干燥氯气的瓶中,布条不褪色
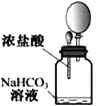
D.将滴管中的浓盐酸加入碳酸氢钠溶液,气球体积由小变大
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
某兴趣小组进行碘的提取实验:首先将海带灼烧成灰,用水浸泡得到含碘离子的水溶液,再用硫酸酸化、加氯水氧化得到少量碘水,最后以CCl4为溶剂将碘单质从中提取出来。下列说法正确的是
A. 灼烧的目的是为了使海带灰化,除去有机物,以便于碘离子的浸出
B. 灼烧时用到的仪器是烧杯、酒精灯、玻璃棒
C. 海带灰浸取液中的碘离子可用淀粉溶液检验
D. CCl4溶剂还可用苯、酒精代替
难度: 简单查看答案及解析
-
从海水中提取镁的工业流程如图所示,下列说法不正确的是
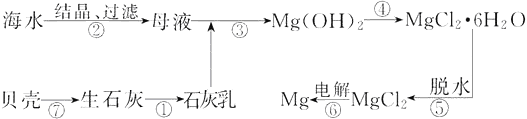
A. 用此法提取镁的优点之一是原料来源丰富
B. 在实验室进行②的操作需用到坩埚、坩埚钳、玻璃棒、酒精灯
C. 步骤⑥电解MgCl2时,副产物Cl2可以循环利用
D. 上述工艺流程中的反应未涉及置换反应
难度: 中等查看答案及解析
-
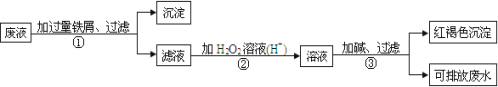
某无色透明溶液可能含有K+、NH4+、Cu2+、Ba2+、Clˉ、CO32ˉ、SO42ˉ中的几种离子。现取等体积的三份该溶液分别进行如下实验:
(1)取第一份溶液加入AgNO3溶液,有白色沉淀产生。
(2)取第二份溶液加入过量的BaCl2溶液,所得沉淀经过滤、洗涤、干燥、称重得6. 63 g;在沉淀中加入过量稀盐酸,仍有4. 66 g沉淀。
(3)取第三份溶液加入过量浓NaOH溶液,加热使气体全部逸出,收集到能使湿润的红色石蕊试纸变蓝色的气体0. 672 L(标准状况)。
根据上述实验,下列推断正确的是
A. 该溶液一定含有K+、NH4+、CO32ˉ、SO42ˉ B. 该溶液一定含有Clˉ
C. Cu2+一定不存在,Ba2+可能存在 D. 还需通过焰色反应检验是否含有K+
难度: 中等查看答案及解析