-
空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
难度: 简单查看答案及解析
-
能使气体物质溶解度增大的操作是
A. 增加溶剂 B. 振荡溶液 C. 增大压强 D. 升高温度
难度: 中等查看答案及解析
-
属于化学变化的是
A.木炭燃烧 B.酒精挥发 C.矿石粉碎 D.铁丝弯曲
难度: 简单查看答案及解析
-
氢元素的符号是
A.He B.H C.H2 D.2H
难度: 简单查看答案及解析
-
澄清石灰水属于
A.溶液 B.纯净物 C.乳浊液 D.悬浊液
难度: 简单查看答案及解析
-
保持水化学性质的微粒是
A.氢原子 B.氧分子 C.水分子 D.水原子
难度: 简单查看答案及解析
-
活性炭能净水,主要是因为它具有
A.还原性 B.吸附性 C.稳定性 D.可燃性
难度: 简单查看答案及解析
-
下列实验操作正确的是
A.
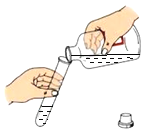 液体的倾倒 B.
液体的倾倒 B.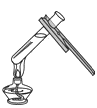 液体的加热
液体的加热C.
量取一定量的液体 D.
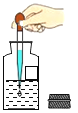 用滴管取液体
用滴管取液体难度: 简单查看答案及解析
-
关于分子、原子说法正确的是
A.分子可分,原子不可再分 B.分子的质量大于原子
C.温度越高,分子运动速率越快 D.温度升高,分子体积增大
难度: 简单查看答案及解析
-
关于“胆矾”说法错误的是
A.颜色:蓝色 B.类别:化合物
C.化学式:CuSO4∙5H2O D.作用:检验水
难度: 简单查看答案及解析
-
化学方程式与事实相符且正确的是
A.4Fe+3O2
2Fe2O3 B.CuO+C
Cu+CO↑
C.CuSO4+2NaOH=Na2SO4+Cu(OH)2↓ D.CO2+Ca(OH)2=CaCO3+H2O
难度: 简单查看答案及解析
-
城市污水经深度净化处理后的水统称“中水”,因为水质介于自来水(上水)与排入管道的污水(下水)之间,故名为“中水”,说法正确的是
A.“中水”是一种饮用水
B.利用“中水”有利于节约水资源
C.“中水”中水分子的构成与蒸馏水中水分子的构成不同
D.将生活污水净化处理成“中水”的过程中要过滤、吸附和蒸馏
难度: 简单查看答案及解析
-
2019 年锂电池的研究荣获了诺贝尔化学奖,“锂-空气”电池是锂电池的一种,它在无水电解质中反应的原理:2Li+O2
Li2O2,说法错误的是
A.充电时,反应为分解反应 B.充电时,氧元素由游离态变为化合态
C.放电时,反应为化合反应 D.放电时,发生的是氧化反应
难度: 简单查看答案及解析
-
下图白球代表氢原子,黑球代表氦原子,表示等质量氢气与氦气的混合气体是
A.
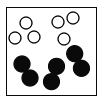 B.
B.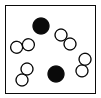 C.
C.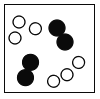 D.
D.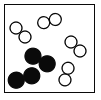
难度: 简单查看答案及解析
-
不能用如图装置进行的实验是
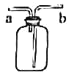
A.排空气法收集氢气,氢气从 a 端通入
B.排水法收集氧气,瓶内装满水,氧气从 a 端通入
C.检验二氧化碳,瓶内装有一定量澄清石灰水,气体从 b 端通入
D.收集并测量氧气的体积,瓶内装满水,a 端接量筒,氧气从 b 端通入
难度: 简单查看答案及解析
-
有关叙述错误的是
A.CO2的摩尔质量为44g/mol
B.1molCO和1molN2的质量相等
C.1molMnO2中含有1mol 氧分子
D.1molH2和1molO2所含的原子个数一样多
难度: 简单查看答案及解析
-
实验现象描述正确的是
A.在空气中点燃镁条,发出耀眼的白光,生成白色氧化镁
B.将红热的铁丝放在空气中,剧烈燃烧,火星四射,生成黑色固体
C.硫在氧气中燃烧产生明亮的蓝紫色火焰,生成无色无味的气体
D.木炭在氧气中燃烧,发出白光,放出热量,产生能使澄清石灰石变浑浊的气体
难度: 简单查看答案及解析
-
推理错误的是
选项
化学反应
影响化学反应的因素
A
镁能与二氧化碳反应,铁不能与二氧化碳反应
反应物的性质
B
通常木炭充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳
反应温度
C
硫在氧气中比在空气中燃烧更剧烈
反应物的浓度
D
加热氯酸钾反应速率较慢,加入二氧化锰后速度加快
催化剂
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
说法正确的是
A.含有一种元素的纯净物是单质
B.由不同种元素组成的物质是化合物
C.物质与氧气发生反应时都需要点燃
D.能生成多种物质的反应是分解反应
难度: 简单查看答案及解析
-
工业中合成SO3的反应:2SO2+O2
2SO3。一定条件下,在一密闭容器内投入 SO2、O2、SO3、V2O5四种物质,在不同时刻测得各物质的质量(单位为 g)如下表所示。说法错误的是
甲
乙
丙
丁
t1
100
5
80
5
t2
60
55
a
b
t3
40
c
d
5
A.丁物质一定是V2O5
B.d=15
C.丙物质是O2
D.t3时,生成乙75g
难度: 中等查看答案及解析
-
图像不能正确反应其变化过程的是
A.
镁在装有空气的密闭容器内燃烧
B.
 电解水生成气体的体积
电解水生成气体的体积C.
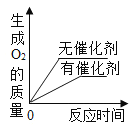 比较氯酸钾中有无二氧化锰的反应情况
比较氯酸钾中有无二氧化锰的反应情况D.
 向氢氧化钠溶液中不断加水
向氢氧化钠溶液中不断加水难度: 中等查看答案及解析
-
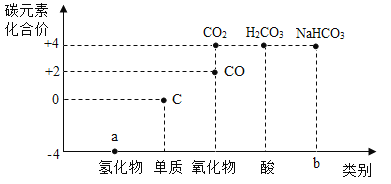
类推是化学学习中常用的思维方法。类推结果正确的是
A.溶液一定是均一稳定的,则均一稳定的液体一定是溶液
B.燃烧一定都伴随发光发热,则有发光发热现象的一定是燃烧
C.化合物中元素都有一定的化合价,则同种元素在一种化合物中化合价一定相同
D.纯净物只含一种物质,则只含一种物质的一定是纯净物
难度: 中等查看答案及解析
-
t℃时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成图中的斜线。说法正确的是
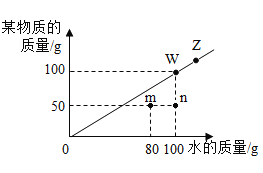
A.t℃时该物质的溶解度为 50g/100g水
B.图中 4 个点表示的溶液中只有 z 是饱和溶液
C.点z向点w移动的一种方法是恒温蒸发一定量的水
D.将m点表示的溶液中变为饱和溶液的一种方法是再加入20g溶质
难度: 中等查看答案及解析
-
某碳酸钙和氧化钙组成的混合物中,钙元素的质量分数为50%,将40g该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是( )
A.8.8g B.12g C.15.7g D.20g
难度: 困难查看答案及解析