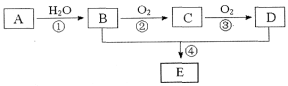
-
下列过程没有发生化学反应的是
A.用含硅胶、铁粉的透气小袋与食品一起密封包装
B.用热碱水清除炊具上残留的油污
C.用浸泡过高锰酸钾溶液的硅藻土保存水果
D.用活性炭去除冰箱中的异味
难度: 中等查看答案及解析
-
许多国家十分重视海水资源的综合利用。不需要化学变化就能够从海水中获得的物质是
A.氯、溴、碘 B. 钠、镁、铝 C. 食盐、淡水 D. 烧碱、氢气
难度: 中等查看答案及解析
-
下列化学用语中表达正确的是
A.四氯化碳的电子式
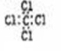 B.C2 H4的结构简式:CH2CH2
B.C2 H4的结构简式:CH2CH2C.环已烷的结构简
D.次氯酸的结构式:H-Cl-O
难度: 中等查看答案及解析
-
下列说法不正确的是
A.钠与乙醇反应,钠块沉在乙醇液面下面
B.除去乙酸乙酯中残留的乙酸,可用饱和Na2CO3溶液洗涤后分液
C.伴有能量变化的物质变化都是化学变化
D.化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变
难度: 中等查看答案及解析
-
下列冶炼金属的反应原理,错误的是
A.2NaCl (熔融)
2Na+Cl2 ↑ B.MgO + H2
Mg + H2O
C.Fe3O4 + 4CO
3Fe + 4CO2 D.Fe+CuSO4=FeSO4+Cu
难度: 中等查看答案及解析
-
糖类、脂肪和蛋白质是维持人体生命活动必需的三大营养物质。以下叙述正确的是
A.糖类、油脂、蛋白质都是高分子化合物
B.淀粉水解的最终产物是葡萄糖
C.油脂的水解反应称为皂化反应
D.加热会使蛋白质变性,因此食用生鸡蛋所获得营养价值更高
难度: 中等查看答案及解析
-
“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应物中原子全部转化为欲制的产物,即原子利用率为100%。以下反应最符合“绿色化学”原子经济性要求的是
A.乙烯发生加聚反应制得聚乙烯高分子材料 B.用甲烷与氯气制备一氯甲烷
C.用苯和液溴为原料制取溴苯 D.用石灰石和稀盐酸反应制得二氧化碳
难度: 中等查看答案及解析
-
下列关于苯的叙述中错误的是
A.苯在催化剂作用下能与液溴发生取代反应
B.在苯中加入酸性KMnO4溶液,振荡并静置后下层液体为紫色
C.在苯中加入溴水,振荡并静置后下层液体为橙色
D.在一定条件下,苯能与氢气发生加成反应
难度: 中等查看答案及解析
-
下列物质中,不能使酸性KMnO4溶液褪色的物质是
①
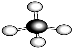 ②乙烯 ③CH3COOH;④CH3CH2OH ⑤CH2=CH—COOH ⑥
②乙烯 ③CH3COOH;④CH3CH2OH ⑤CH2=CH—COOH ⑥A.①⑥ B.①③④⑥ C.①④ D.①③⑥
难度: 中等查看答案及解析
-
下列说法中正确的是:
A.组成上相差一个或若干个CH2原子团,且符合同一通式的有机物之间互称为同系物
B.由于苯分子结构的特殊性,因此苯不能发生加成反应
C.淀粉、纤维素、天然油脂等都属于混合物
D.丙烷分子中所有原子不在一个平面上,但3个碳原子在一直线上
难度: 中等查看答案及解析
-
下列结论错误的是
A.氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 B.微粒半径:K+>Al3+>S2->Cl—
C.酸性:H2SO4>CH3COOH>H2CO3>HClO D.金属性:K>Ca>Mg>Be
难度: 中等查看答案及解析
-
某有机物的结构简式如右图.该物质不应有的化学性质是
①可燃烧②可跟溴加成③可使酸性KMnO4溶液褪色④可跟NaHCO3溶液反应⑤可跟NaOH溶液反应⑥可在碱性条件下水解⑦可与新制备的Cu(OH)2悬浊液煮沸生成红色沉淀
A. ①② B. ③④ C. ④⑤ D. ⑥⑦
难度: 中等查看答案及解析
-
将2.5 mol A和1.25 mol B通入容积为1L的真空密闭容器中,经5s达到平衡状态。3A(g)+B(g)
pC(g)+2D(g),生成0.5 mol D,又知C的平均反应速率是0.1 mol/(L·s),则下列说法中正确的是
①A的转化率为20% ②B的转化率为25% ③A的平均反应速率为0.1mol/(L·s) ④方程式中p=2 ⑤B的平均反应速率为0.05mol/(L·s)
A. ①② B. ②③ C. ③④ D. ④⑤
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.1mol C10H22含共价键数目32NA
B.常温常压下,8gCH4含有电子数目5NA
C.1L 0.1mol•L-1的醋酸溶液中含有CH3COO-的数目0.1NA
D.78g苯含有C=C双键的数目为3NA
难度: 中等查看答案及解析
-
将纯锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
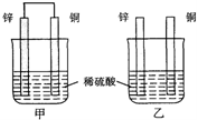
A.两烧杯中溶液的pH均增大
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中铜片表面均无气泡产生
D.甲、乙溶液均变蓝色
难度: 中等查看答案及解析
-
为提纯下列物质(括号内为杂质).所选试剂及方法均正确的是
选项
物质(括号内为杂质)
除杂试剂
方法
A
溴苯(溴)
CCl4
分液
B
硝基苯(NO2)
NaOH溶液
分液
C
乙烷(乙烯)
氢气
洗气
D
乙醇(乙酸)
NaOH溶液
分液
难度: 中等查看答案及解析
-
用下列实验装置进行的实验中,不能达到相应实验目的的是
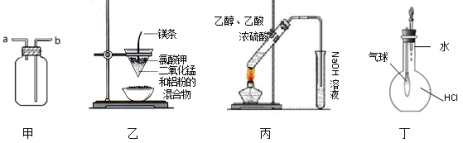
A.装置甲:气体从a口进入,收集NH3 B.装置乙:可制得金属锰
C.装置丙:实验室制取乙酸乙酯D.装置丁:验证HCl气体在水中的溶解性
难度: 中等查看答案及解析
-
下列反应中,反应后固体物质增重的是
A.乙醇蒸汽通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应 D.将锌粒投入Cu(NO3)2溶液
难度: 中等查看答案及解析
-
在
分子中,处于同一平面上的原子数最多可能是
A.15个 B.16个 C.17个 D.18个
难度: 中等查看答案及解析
-
实验室可以通过乙醇分子内的脱水反应制乙烯,反应方程式如下:
下列醇类物质中也能发生类似的脱水反应生成烯烃的是
A.
B.CH3OH C.
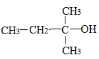 D.
D.难度: 中等查看答案及解析
-
a mL三种气态烃组成的混合物与足量氧气混合,点燃爆炸后,恢复到原来的状态(常温、常压),体积共缩小2a mL。则三种烃可能是
A.CH4、C2H4、C3H4 B.C2H6、C3H6、C4H6
C.CH4、C2H6、C3H8 D.C2H4、C2H2、CH4
难度: 中等查看答案及解析
-
丁烷CH3CH2CH2CH3的二氯代物有
A.8种 B.7种 C.6种 D.5种
难度: 中等查看答案及解析
-
分析下表中各项的排布规律,按此规律排布第26项应为
1
2
3
4
5
6
7
8
9
10
C2H4
C2H6
C2H6O
C2H4O2
C3H6
C3H8
C3H8O
C3H6O2
C4H8
C4H10
A.C7H16 B.C7H14O2 C.C8H18 D.C8H18O
难度: 中等查看答案及解析
-
氧化亚铁粉末和铝粉配成铝热剂,分成两等份。一份在高温下恰好完全反应后,在与盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两种情况下生成的气体的质量比是
A.1:1 B.2:3 C. 3:2 D 28:9
难度: 中等查看答案及解析
-
铜的冶炼大致可分为:①富集,将硫化物矿进行浮选;②焙烧,主要反应为2CuFeS2+4O2===Cu2S+3SO2+2FeO(炉渣);③制粗铜,在1200 ℃发生的主要反应为2Cu2S+3O2===2Cu2O+2SO2,2Cu2O+Cu2S===6Cu+SO2↑;④电解精炼铜。下列说法不正确的是 ( )
A.上述灼烧过程的尾气回收后可用来制硫酸
B.上述过程中,由6 mol CuFeS2制取6 mol Cu时共消耗15 mol O2
C.在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化产物与还原产物的物质的量比1:6
D.在反应2Cu2O+Cu2S===6Cu+SO2↑中,只有Cu2O作氧化剂
难度: 中等查看答案及解析
-
(10分)800℃时在2L密闭容器内反应:2NO(g)+O2(g)
2NO2(g)体系中, n(NO)随时间的变化如表:
时间/s
0
1
2
3
4
5
n(NO)/mol
0.020
0.010
0.008
0.007
0.007
0.007
(1)达平衡时NO的转化率_________________。
(2)下图中表示NO2的变化的曲线是________,
用O2表示从0~2s内该反应的平均速率v(O2)=_____。
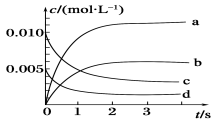
(3)能说明该反应一定达到平衡状态的是_ _
A.v(NO2)=2v(O2) B.容器内颜色保持不变
C.2V逆 (NO)=v正(O2) D.容器内压强保持不变
(4)能增大该反应的反应速率是
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效催化剂
难度: 中等查看答案及解析