-
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学论断等高科技领域。已知只有质子数或中子数为奇数的原子核才有NMR现象。试判断下列哪组原子均可产生NMR现象
A. 18O、31P、119Sn
B. 元素周期表中VA族所有元素的原子
C. 27Al、19F、12C
D. 元素周期表中第一周期所有元素的原子
难度: 中等查看答案及解析
-
下列表示方法正确的是
A.O2-的结构示意图:
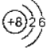
B.四氯化碳的电子式:
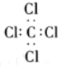
C.HClO的结构式为:H—O—Cl
D.用电子式表示氯化氢分子的形成过程:
难度: 中等查看答案及解析
-
下列说法不正确的是
A.研究物质在水溶液中的反应,溶液是环境,盛溶液的烧杯和溶液之外的空气等便是体系
B.能源的开发和利用可以用来衡量一个国家或地区的经济发展和科学技术水平
C.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加
D.在稀溶液中,H+(aq) +OH-(aq)=H2O(l) △H=-57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1mol KOH的溶液混合,放出的热量大于57.3kJ
难度: 中等查看答案及解析
-
下列有关化学反应方向及其判据的说法中正确的是
A.非自发反应就是不可能发生的反应,自发反应就是能较快进行的反应
B.高温高压下可以使石墨转化为金刚石是自发的化学反应
C.由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程
D.反应NH3(g)+HCl(g)=NH4Cl(s)在低温下能自发进行,说明该反应的△H>0
难度: 中等查看答案及解析
-
下列各粒子:①H3O+、NH4+、Na+;②OH-、NH2-、F-;③O2-、Na+、Mg2+;④CH4、NH3、H2O具有相同质子数和电子数的一组是
A. ①②③ B. ①②④ C. ②③④ D. ①③④
难度: 中等查看答案及解析
-
反应C(s)+H2O(g)
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加C的量
②将容器的体积缩小一半
③保持体积不变,充入N2 使体系压强增大
④保持压强不变,充入N2使容器体积变大
A.①④ B.②③ C.①③ D.②④
难度: 困难查看答案及解析
-
一定温度下,水存在H2O
H++OH- △H=Q(Q>0)的平衡,下列叙述一定正确的是
A.向水中滴入少量稀盐酸,平衡逆向移动,KW减小
B.将水加热,K w 增大,pH不变
C.向水中加入少量金属Na,平衡逆向移动,c(H +)降低
D.向水中加入少量固体硫酸钠,c(H+)和K w 均不变
难度: 中等查看答案及解析
-
X和Y两种元素可以形成XY2型共价化合物,则X和Y的原子序数为
A.3和17 B.6和8 C.12和9 D.8和16
难度: 中等查看答案及解析
-
下列事实不能用勒夏特列原理解释的是
A.合成氨工厂采用增大压强以提高原料的转化率
B.实验室用排饱和食盐水法收集氯气
C.打开汽水瓶有气泡从溶液中冒出
D.2NO2(g)=N2O4(g)的平衡体系中,加压缩小体积后颜色加深用来表示可逆反应
难度: 中等查看答案及解析
-
已知:①2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) △H1
②2CO(g)+O2(g)=2CO2(g) △H2
③2H2(g)+O2(g)=2H2O(l) △H3
④2H2(g)+O2(g)=2H2O(g) △H4
⑤CO(g)+2H2(g)=CH3OH(g) △H5
下列关于上述反应焓变的判断正确的是
A.△H1>0,△H2<0
B.△H3>△H4
C.△H1=△H2+2△H3-△H5
D.2△H5+△H1<0
难度: 困难查看答案及解析
-
有以下反应:
PCl5(g)
PCl3(g)+Cl2(g) ①
2HI(g)
H2(g)+I2(g) ②
2NO2(g)
N2O4(g) ③
在一定条件下,达到化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则转化率
A.①减少,②不变,③增大 B.均增大
C.①增大,②不变,③减少 D.均不变
难度: 困难查看答案及解析
-
下列装置或操作能达到实验目的的是
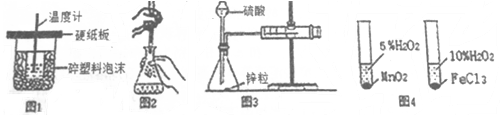
A.图1装置用于中和热的测定
B.图2装置用于高锰酸钾溶液滴定草酸
C.图3装置用于测定氢气的反应速率(单位mL/s)
D.图4装置用于研究不同催化剂对反应速率的影响
难度: 困难查看答案及解析
-
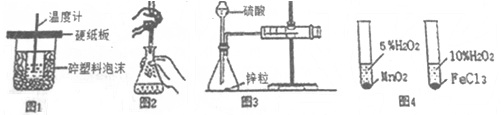
A.图1装置用于中和热的测定
B.图2装置用于高锰酸钾溶液滴定草酸
C.图3装置用于测定氢气的反应速率(单位mL/s)
D.图4装置用于研究不同催化剂对反应速率的影响
【答案】B
【解析】
A.缺少环形玻璃搅拌棒,错误;B.草酸溶液与酸性高锰酸钾溶液反应,加入最长一滴呈紫红色说明达到滴定终点,正确;C.缺少秒表,无法测定时间,故不能用于测定氢气的反应速率,错误;D.两试管中双氧水的浓度应保持一致,错误。
考点:考查化学实验方案的设计与评价的知识。
【题型】选择题
【适用】较难
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】下列结论正确的是
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
A. ②⑤⑦ B. ②⑥⑦ C. ②④⑤⑥⑦ D. ②④⑥
难度: 中等查看答案及解析
-
下列结论正确的是
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
A. ②⑤⑦ B. ②⑥⑦ C. ②④⑤⑥⑦ D. ②④⑥
【答案】C
【解析】试题分析:①电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->Cl->K+>Al3+,错误;②非金属性F>Cl>S>P>Si,氢化物稳定性:HF>HCl>H2S>PH3>SiH4,正确;③非金属性Cl>Br>I>S,阴离子还原性S2->I->Br->Cl-,错误;④非金属性Cl>S>Se>Te,单质氧化性Cl2>S>Se>Te,正确;⑤非金属性S>P>C,最高价含氧酸的酸性H2SO4>H3PO4>H2CO3,碳酸的酸性比HClO强,故酸性H2SO4>H3PO4>H2CO3>HClO,正确;⑥同周期随原子序数增大元素非金属性增强,同主族自上而下元素非金属性减弱,故非金属性O>N>P>Si,正确;⑦同主族自上而下金属性增强,同周期自左而右金属性减弱,故金属性:Be<Mg<Ca<K,正确。正确的判断是②④⑤⑥⑦ ,选项C符合题意。
考点:考查微粒半径比较、氧化性及还原性强弱比较及同周期、同主族元素金属性非金属性强弱比较的知识。
【题型】选择题
【适用】一般
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】下列图示与对应的叙述相符的是
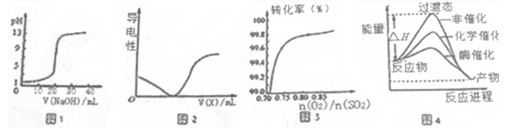
A.图一表示0.1000mol·L-1NaOH溶液滴定20.00ml 0.1000 mol·L-1醋酸溶液得到滴定曲线
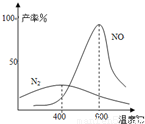
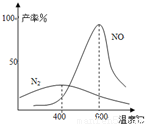
B.图2所示在H2S溶液导电性实验中,曲线可确定通入的气体X为Cl2
C.图3在其它条件不变时,2SO2(g)+O2(g)
2SO3(g)转化关系中,纵坐标表示O2的转化率
D.由图4所示曲线可知,酶催化比化学催化的效果好
难度: 困难查看答案及解析
-
下列图示与对应的叙述相符的是

A.图一表示0.1000mol·L-1NaOH溶液滴定20.00ml 0.1000 mol·L-1醋酸溶液得到滴定曲线
B.图2所示在H2S溶液导电性实验中,曲线可确定通入的气体X为Cl2
C.图3在其它条件不变时,2SO2(g)+O2(g)
2SO3(g)转化关系中,纵坐标表示O2的转化率
D.由图4所示曲线可知,酶催化比化学催化的效果好
【答案】D
【解析】
A.醋酸是弱酸,0.1mol/L的醋酸的pH>1,所以图一表示0.1000mol·L-1NaOH溶液滴定20.00ml 0.1000 mol·L-1一元强酸溶液得到滴定曲线,错误;B.在H2S的溶液中通入Cl2,会发生反应:Cl2+H2S=S↓+2HCl,溶液的酸性增强,离子浓度增大,溶液的导电性增强,与图像不吻合,错误;C.2SO2(g)+O2(g)
2SO3(g)是可逆反应,在其它条件不变时,增大氧气的浓度,化学平衡正向移动,但是O2的转化率会降低,不符合图像,错误;D.催化剂可以降低反应的活化能,使反应速率加快,反应需要的活化能越低,反应速率就越快。根据图示可知酶催化比化学催化的效果好,正确。
考点:考查图像方法在溶液的导电性、化学反应及催化剂的作用比较的应用的知识。
【题型】选择题
【适用】较难
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】已知:① 2CO(g)+O2(g)
2CO2(g) △H=-566kJ/mol;
②Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) △H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是
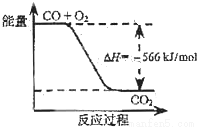
A.CO(g)与Na2O2(s)反应放出509kJ热量时,消耗的CO是28g
B.如上图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) △H<-452 kJ/mol
D.CO的燃烧热为-566 kJ/mol
难度: 中等查看答案及解析
-
已知:① 2CO(g)+O2(g)
2CO2(g) △H=-566kJ/mol;
②Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) △H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是
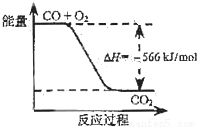
A.CO(g)与Na2O2(s)反应放出509kJ热量时,消耗的CO是28g
B.如上图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) △H<-452 kJ/mol
D.CO的燃烧热为-566 kJ/mol
【答案】A
【解析】
A.将①×1/2+②,整理可得CO(g)+Na2O2(s)= Na2CO3(s) △H=-509kJ/mol,即1molCO发生该反应放出热量是509kJ,现在放出热量就是509kJ,则消耗CO的物质的量是1mol,其质量是28g,正确; B.CO生成CO2的反应是放热反应,反应物的能量,图示没有注明物质的状态,不能体系能量变化关系,错误;C.根据反应可知2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=-452 kJ/mol,若CO2是固体,由于能量比气体低,反应放出的热量小于452 kJ,故2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) △H>-452 kJ/mol,错误;D.燃烧热是1mol可燃物完全燃烧产生稳定的氧化物时放出的热量,根据①可知CO的燃烧热是-283kJ/mol,错误。
考点:考查反应热的有关计算的知识。
【题型】选择题
【适用】一般
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】下列说法不正确的是
A.稀醋酸中加入少量醋酸钠固体减小醋酸的电离程度
B.0.02 mol·L-1HCl溶液与0.02 mol·L-1Ba(OH)2溶液等体积混合后,溶液pH约为12
C.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
D.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
难度: 困难查看答案及解析
-
下列说法不正确的是
A.稀醋酸中加入少量醋酸钠固体减小醋酸的电离程度
B.0.02 mol·L-1HCl溶液与0.02 mol·L-1Ba(OH)2溶液等体积混合后,溶液pH约为12
C.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
D.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
【答案】C
【解析】
A.醋酸在溶液中存在电离平衡:CH3COOH
CH3COO-+H+,当想稀醋酸中加入少量醋酸钠固体时,溶液中c(CH3COO-)增大,醋酸的电离平衡逆向移动,从而减小了醋酸的电离程度,正确;B.0.02 mol·L-1HCl溶液与0.02 mol·L-1Ba(OH)2溶液等体积混合后,溶液中c(OH-)=(0.02 mol·L-1×2-0.02 mol·L-1)÷2=0.01mol/L,由于在室温下水的离子积常数是10-14,所以c(H+)=10-12mol/L,故溶液pH约为12,正确;C.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,第一种溶液中氢离子的浓度是第二种溶液中氢离子浓度的10倍。由于溶液的浓度越大,其电离程度就越小,所以则c1>10c2,错误;D.pH=11的NaOH溶液的氢氧根离子的浓度与pH=3的醋酸溶液中氢离子的浓度相等。由于醋酸是弱酸,主要以电解质分子存在,在溶液中存在电离平衡,党二者等体积混合后,由于醋酸过量,溶液显酸性,滴入石蕊溶液时,溶液呈红色,正确。
考点:考查电解质溶液的有关知识。
【题型】选择题
【适用】较难
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(s)
zC(g),达到平衡后测得A气体的浓度为0.5 mol·L-1,当恒温下将密闭容器的容积扩大到两倍再达到平衡后,测得A的浓度为0.3 mol·L-1,则下列叙述正确的是
A.C的体积分数降低
B.x+y=z
C.平衡向正反应方向移动
D.x+y<z
难度: 中等查看答案及解析
-
一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(s)
zC(g),达到平衡后测得A气体的浓度为0.5 mol·L-1,当恒温下将密闭容器的容积扩大到两倍再达到平衡后,测得A的浓度为0.3 mol·L-1,则下列叙述正确的是
A.C的体积分数降低
B.x+y=z
C.平衡向正反应方向移动
D.x+y<z
【答案】A
【解析】
恒温扩大体积则气体的压强减小,平衡向气体总体积增大的方向移动。因原平衡时A的浓度为0.5 mol·L-1,当体积扩大两倍,假设平衡不移动,则A的浓度将变为0.25 mol·L-1,现新平衡时A的浓度为0.3 mol·L-1,说明减小压强,化学平衡向生成A的方向移动了,即平衡向逆反应方向移动,逆反应方向是气体体积增大的反应方向,所以x+y>z,则C的体积分数降低,古选项A正确。
考点:考查化学平衡移动的影响因素的判断的知识。
【题型】选择题
【适用】一般
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)
5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是
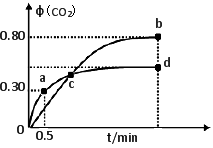
A.b点时,CO的转化率为20%
B.容器内的压强保持恒定,表明反应达到平衡状态
C.b点和d点的化学平衡常数:Kb>Kd
D.0到0.5min反应速率v(CO)=0.3 mol·L-1·min-1
难度: 困难查看答案及解析
-
利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)
5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是
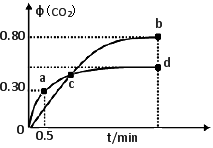
A.b点时,CO的转化率为20%
B.容器内的压强保持恒定,表明反应达到平衡状态
C.b点和d点的化学平衡常数:Kb>Kd
D.0到0.5min反应速率v(CO)=0.3 mol·L-1·min-1
【答案】C
【解析】
A.5CO(g) +I2O5(s)
5CO2(g)+I2(s)
起始量/mol 2 0
转化量/mol y y
b点量/mol 2-y y
根据b点时CO2的体积分数φ(CO2)=y÷2=0.80,得y=1.6mol,转化率等于=(变化量÷起始量)×100%=(1.6÷2)×100%=80%,错误;B.两边计量数相等,所以压强始终不变,不能做平衡状态的标志,错误;C.b点比d点时生成物CO2体积分数大,说明进行的程度大,则化学平衡常数:Kb>Kd,正确;
D.0到0.5min时:5CO(g) +I2O5(s)
5CO2(g)+I2(s)
起始量/mol 2 0
转化量/mol x x
a点量/mol 2-x x
根据a点时CO2的体积分数φ(CO2)=x÷2=0.30,得x=0.6mol;则从反应开始至a点时的反应速率为v(CO)=(0.6mol÷2L)÷0.5min=0.6 mol·L-1·min-1,错误。
考点:考查影响化学反应速率和化学平衡影响的因素的知识。
【题型】选择题
【适用】较难
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是
A. X、Y、Z、W的原子半径依次减小
B. 若W与Y的原子序数相差5,则二者形成化合物的化学式可能为Y2W3
C. W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D. W与X形成的化合物只含离子键
难度: 中等查看答案及解析
-
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是
A. X、Y、Z、W的原子半径依次减小
B. 若W与Y的原子序数相差5,则二者形成化合物的化学式可能为Y2W3
C. W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D. W与X形成的化合物只含离子键
【答案】A
【解析】试题分析:W、X、Y、Z为短周期元素,W、Z同主族,W的气态氢化物的稳定性比Z的气态氢化物的稳定性强,故W、Z为非金属,原子序数Z>W,W处于第二周期,Z处于第三周期,X、Y、Z同周期,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性,则原子序数Y>X,且二者处于第三周期,X、Y、Z的原子序数Z>Y>X。A.W、Z同主族,原子序数Z>W,X、Y、Z同周期,X、Y、Z的原子序数Z>Y>X,所以原子半径X>Y>Z>W,正确;B.若W为N元素,Y为Mg元素,二者的原子序数相差5,二者形成化合物的化学式可能为Mg3N2,为Y3W2,错误;C.W的气态氢化物为氨气、水、氟化氢时,分子间存在氢键,沸点高于同族其它氢化物的沸点,W为C、Z为Si时,W氢化物沸点较低,错误;D.若W与X形成的化合物为过氧化钠,既含离子键又含共价键,错误。
考点:考查元素周期表、元素周期律的应用的知识。
【题型】选择题
【适用】一般
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
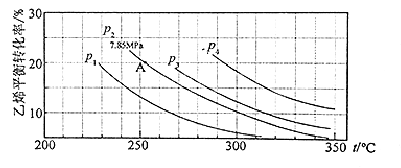
【结束】气相直接水合法制乙醇的方程式为:C2H4 (g)+H2O(g)=C2H5OH(g),其中乙烯的平衡转化率与温度、压强的关系如图[起始n(H2O)︰n(C2H4)=1︰1]。
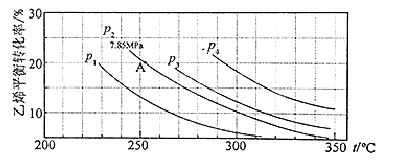
计算乙烯水合制乙醇反应在图中A点的平衡常数KP为(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
A.0.068 MPa-1 B.0.082 C.0.072 MPa-1 D.0.082 MPa-1
难度: 困难查看答案及解析
 2NH4Cl+Ca(OH)2
2NH4Cl+Ca(OH)2