-
下列说法不正确的是
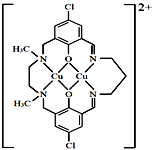
A.液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性
B.常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关
C.石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化
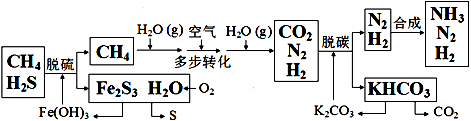
D.燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施
难度: 中等查看答案及解析
-
在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热。下列有关说法错误的是( )
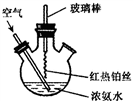
A. 反应后溶液中含有NO3-
B. 反应后溶液中c(H+)增大
C. 实验过程中有化合反应发生
D. 实验过程中NH3•H2O的电离常数不可能发生变化
难度: 中等查看答案及解析
-
a、b、c、d、e分别为MgCl2、KHSO4、KOH、NaHCO3、AlCl3五种溶液中的一种,其中a能与其余四种溶液反应,且与c、e反应时有明显的现象;b与d反应只产生气泡;e只能与a反应。下列推理不正确的是( )
A.a一定为KOH B.b一定为KHSO4
C.c一定为AlCl3 D.e一定为MgCl2
难度: 中等查看答案及解析
-
在25℃时,H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如下图所示,下列叙述错误的是

A.H2R是二元弱酸,其Ka1=1×10-2
B.当溶液恰好呈中性时,c( Na + )=2c ( R2- ) + c( HR- )
C.NaHR在溶液中水解倾向大于电离倾向
D.含Na2R与NaHR各0.1 mol的混合溶液的pH=7.2
难度: 困难查看答案及解析
-
利用如图所示装置进行下列实验,实验现象与结论均正确的是( )
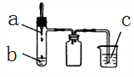
选项
实验试剂
实验现象
实验结论
a
b
c
A
浓氨水
碱石灰
FeCl2溶液
产生白色沉淀,迅速变为灰绿色,最后变为红褐色
氨气具有氧化性
B
稀硫酸
FeS
AgCl悬浊液
悬浊液由白色变为黑色
Ksp(AgCl)>Ksp(Ag2S)
C
浓硝酸
铜
BaSO3悬浊液
悬浊液变澄清
+4价硫具有还原性
D
浓盐酸
KMnO4
紫色石蕊试液
溶液先变红后褪色
Cl2有酸性和漂白性
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
在密闭容器中将2molNaHCO3(s)和一定量Na2O2混合,在加热条件下让其充分反应,150℃下所得气体仅含2种组分,反应后固体的物质的量(n)的取值范围是( )
A. n≥1 B. 1<n<2 C. 2≤n<4 D. n≥4
难度: 困难查看答案及解析
-
溶液的酸碱性可用酸度(AG)表示,
 。室温下,将0.0100mol•L-l盐酸逐滴滴入20.0mL 0.0100mol•L-l氨水中,溶液的AG变化如图所示。下列说法正确的是
。室温下,将0.0100mol•L-l盐酸逐滴滴入20.0mL 0.0100mol•L-l氨水中,溶液的AG变化如图所示。下列说法正确的是( )
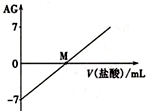
A. M点以后NH4+的水解程度逐渐增大
B. 室温下,0. 0100mol•L-l盐酸的AG =12
C. M点加入盐酸的体积大于20.0 mL
D. M点时溶液中:c(NH4+) =c(Cl-)
难度: 困难查看答案及解析