-
以下成语本意涉及氧化还原反应的是
A. 百炼成钢 B. 刻舟求剑 C. 水滴石穿 D. 暗香浮动
难度: 中等查看答案及解析
-
中华美食食材来源广泛,以下食材蛋白质含量最高的是
A. 海带 B. 豆腐 C. 竹笋 D. 萝卜
难度: 中等查看答案及解析
-
阿伏加德罗常数的值为NA,下列说法正确的是
A. 0.01mol乙烯气体被浓溴水完全吸收,反应伴随0.02NA个碳碳共价键断裂
B. 实验室用电解熔融NaOH制取金属钠,制得2.3g钠电路上至少转移0.1NA个电子
C. 标况下,44.8LHCl气体溶于1.0L水中,所得溶液每毫升中含2×10-3NA个H+
D. 含4molHC1的浓盐酸与足量的MnO2混合后充分加热,可产生NA个Cl2分子
难度: 中等查看答案及解析
-
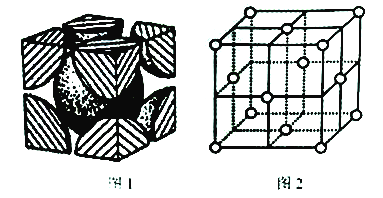
立方烷(C8H8)外观为有光泽的晶体。其八个碳原子对称地排列在立方体的八个角上。以下相关说法错误的是
A. 立方烷在空气中可燃,燃烧有黑烟产生
B. 立方烷一氧代物1种、二氯代物有3种、三氯代物也有3种
C. 立方烷是苯(C6H6)的同系物、也是苯乙烯(C6H5-CH=CH2)的同分异构体
D. 八硝基立方烷完全分解可能只产生二氧化碳和氮气
难度: 中等查看答案及解析
-
四种短周期主族元素甲、乙、丙、丁的原子序数呈等差递增。甲元素存在于所有有机化合物中、丙元素原子最外层电子数与最内层相同。下列关于这些元素的描述错误的是( )
A. 甲单质形成的多种新材料具有美好应用前景
B. 乙和丙可形成阴阳离子电子层结构相同的离子化合物
C. 它们的最高化合价均与其族序数相同
D. 丁元素单质有多种同素异形体
难度: 中等查看答案及解析
-
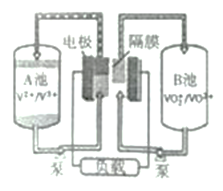
科研人员设计一种电化学反应器以Na2SO4溶液为电解质,负载纳米MnO2的导电微孔钛膜和不锈钢为电极材料。这种电催化膜反应器可用于正丙醇合成丙酸,装置示意图:
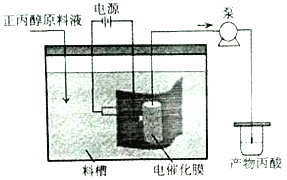
以下叙述错误的是
A. 微孔钛膜作阴极
B. 使用Na2SO4溶液是为了在电解开始时增强溶液导电性
C. 丙醇转化为丙酸的电极反应式为:CH3CH3CH2OH+H2O-4e-=CH3CH2COOH+4H+
D. 反应器工作时料槽中正丙醇分子向电催化膜移动
难度: 困难查看答案及解析
-
已知pOH=-lgc(OH)。t℃时,往50mL0.1mol/LMOH溶液滴加0.1mol/L盐酸,溶液pH、pOH随滴入盐酸体积的变化如下图所示,以下说法正确的是
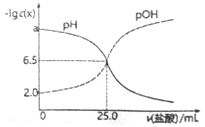
A. a=12
B. 盐酸与MOH溶液恰好中和时溶液pH=6.5
C. 滴人盐酸体积达26.0mL时,溶液中微粒浓度c(Cl-)>c(H+)>c(M+)>c(MOH)>c(OH-)
D. t℃时,MOH的Kb>1.0×10-3
难度: 困难查看答案及解析
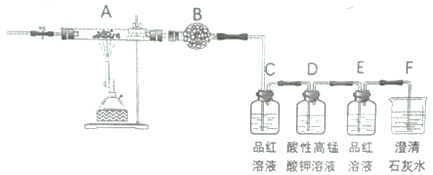





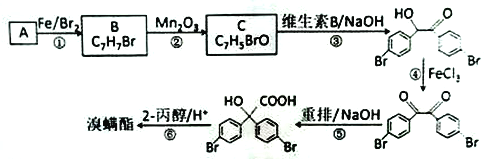
 的同分异构体,其核磁共振氢谱显示有4 种不同化学环境的氢,且数目比为4:4:1:1,M的结构简式为____________。
的同分异构体,其核磁共振氢谱显示有4 种不同化学环境的氢,且数目比为4:4:1:1,M的结构简式为____________。