-
目前世界上新建的金矿中约有80%都采用氧化法提金。某工厂利用锌冶炼渣回收金、银等贵金属的流程如下图所示:

已知:HCN有剧毒,其Ka(HCN)=5×10-10,
Au++2CN-=[Au(CN)2]-平衡常数KB=1×1038
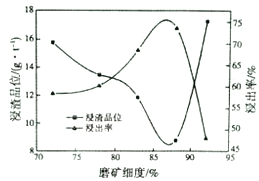
(1)磨矿细度对浸出率的影响如图所示,依据浸出率应选择磨矿细度_____为宜。
(2)生产中用生石灰调节矿泥pH>11.5,其目的之一是阻止溶液中的氰化物转化为HCN而挥发,其作用原理是________________(用离子方程式表示)。
(3)“氰化”环节,是以NaCN溶液浸取调节pH的矿泥,敞口放置,将Au转换为Na[Au(CN)2]。
①其化学方程式为________________。
② “氰化”环节中,金的溶解速率在80℃时达到最大值,但生产中控制反应液的温度在10-20℃,原因是:___________________________(答一点即可)。
③已知2H++[Au(CN)2]- Au++2HCN,该反应的K=____________。
Au++2HCN,该反应的K=____________。
(4)用锌还原NaAu(CN)2生成金,消耗的锌与生成的金的物质的量之比为____________。
(5)氰化物有剧毒,经合理处理就可以基本消除对环境的负面影响。H2O2可消除水中的氰化物(如NaCN),经以下反应实现:NaCN+H2O2+H2O=A+NH3↑。
①生成物A的化学式为______________。
②某废水用H2O2处理40min后,测得剩余总氰为0.16mg/L,除氰率达80%,计算0-40min时间段反应速率v(CN-)=____mg/(L·min)(结果保留两位有效数字)。
-
某化工厂冶炼金属、回收硫的工艺流程如下:

I.回收硫
(1)工业上,采用饱和亚硫酸钠溶液吸收烟气中二氧化硫,写出离子方程式: 。然后,加热吸收液收集SO2。将二氧化硫、空气在稀硫酸中构成原电池,负极反应式为 。
II.冶炼铜
(2)工业上,火法冶炼铜分两步:第一步,含铜矿(主要成分是Cu2S)在空气中煅烧生成氧化亚铜和刺激性气味气体;第二步,氧化亚铜和铜矿在高温下反应生成铜和刺激性气体。写出冶炼铜的总反应方程式: 。
(3)用电解法精炼粗铜(含银、金、铁、锌杂质),装置如图所示。下列说法不正确的是 。
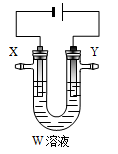
A.Y极为粗铜、X极为纯铜
B.X极净增质量等于Y极净减质量
C.铜盐溶液作精炼铜的电解质溶液
D.若电路有1 mol电子转移,则X极净增32 g
(4)几种金属离子的沉淀pH:
| 金属氢氧化物 | 开始沉淀pH | 完全沉淀的pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.7 |
| Cu(OH)2 | 4.6 | 6.4 |
| Zn(OH)2 | 5.9 | 8.9 |
铜盐溶液中Fe2、Zn2+对精炼铜可能会产生影响。工业上,除去Fe2+方法是,在酸性混合溶液中加入 (选填:双氧水、次氯酸钠、氯水或高锰酸钾溶液)将Fe2+氧化成Fe3+,离子方程式为 。加入碱调节溶液pH范围为 。
-
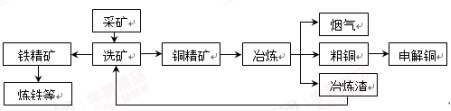
某化工厂冶炼金属、回收硫的工艺流程如下:
I.回收硫
(1)工业上,采用饱和亚硫酸钠溶液吸收烟气中二氧化硫,写出离子方程式:。
然后,加热吸收液收集SO2。将二氧化硫、空气在稀硫酸中构成原电池,负极反应式为。
II.冶炼铜
(2)工业上,火法冶炼铜分两步:第一步,含铜矿(主要成分是Cu2S)在空气中煅烧生成氧化亚铜和刺激性气味气体;第二步,氧化亚铜和铜矿在高温下反应生成铜和刺激性气体。写出冶炼铜的总反应方程式:。
(3)用电解法精炼粗铜(含银、金、铁、锌杂质),装置如图所示。下列说法不正确的是。
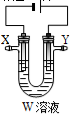
A.Y极为粗铜、X极为纯铜
B.X极净增质量等于Y极净减质量
C.铜盐溶液都可以作精炼铜的电解质溶液
D.若电路有1mol电子转移,则X极净增32g
(4)几种金属离子的沉淀pH:
| 金属氢氧化物 | 开始沉淀pH | 完全沉淀的pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.7 |
| Cu(OH)2 | 4.6 | 6.4 |
| Zn(OH)2 | 5.9 | 8.9 |
铜盐溶液中Fe2,Zn2+对精炼铜可能会产生影响。工业上,除去Fe2+方法是,在酸性混合溶液中加入(选填:双氧水、次氯酸钠、氯水或高锰酸钾溶液)将Fe2+氧化成Fe3+,离子方程式为。加入碱调节溶液pH范围为。
III.冶炼铁
(5)化工厂利用菱铁矿(主要成分是碳酸亚铁)冶炼铁的原理是(用化学方程式表示):。生铁炼钢的主要原理是。
(6)生铁在湿润空气中发生电化学腐蚀最终生成红色铁锈,金属电化腐蚀类型为。
-
镓是制作高性能半导体的重要原料。在工业上经常从锌矿冶炼的废渣中回收镓。已知锌矿渣中含有Zn、Fe、Pb、Ga以及二氧化硅等,目前综合利用锌矿渣的流程如下:
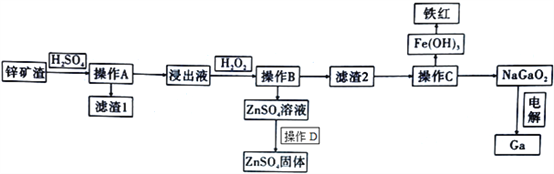
已知:①Ga性质与铝相似。
②lg2=0.3,lg3=0.48。
③如下表所示。
| Zn(OH)2 | Ga(OH)3 | Fe(OH)2 | Fe(OH)3 |
| Ksp | 1.6×10-17 | 2.7×10-31 | 8×10-16 | 2.8×10-39 |
(1)写出Ga的原子结构示意图______________________________。
(2)滤渣1的成分为________________________。
(3)加入H2O2的目的( 用离子方程式和适当语言回答) ____________________________________。
(4)室温条件下,若浸出液中各种阳离子的浓度均为0.01mo/L且某种离子浓度小于1×10-5 mol/L即认为该离子已完全除去,问操作B调节pH的范围是________________________。
(5)操作C中,需要加入氢氧化钠溶液,其目的是_____________________ (用离子方程式解释);能否用氨水代替NaOH溶液,为什么? ________________________;如何检测Fe(OH)3洗涤干净? ________________________。
(6)在工业上,经常用电解NaGaO2溶液的方法生产Ga,写出阴极的电极反应方程式:____________________________________。
-
云南是我国的矿产资源大省,被誉为“有色金属王国”。利用某冶炼废渣(主要成分为二氧化硅和锡、铜、铅、铁的氧化物)回收锡、铜、铅的工艺流程如下图所示:
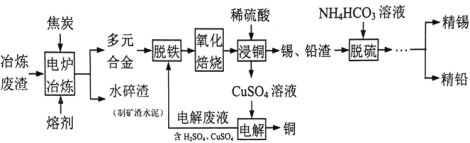
回答下列问题:
(1)电炉冶炼时,焦炭的作用是_____(填“氧化剂”或“还原剂”),将焦炭粉碎的目的是_____。熔剂的主要成分是氟石(CaF2),高温下能与 SiO2 反应生成两种钙,其中之一为 CaSiF6,该反应的化学方程式为_____。
(2)脱铁后的溶液中含有少量的 Sn2+,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为_____。
(3)已知 SnO2 不溶于稀硫酸。脱铁后氧化焙烧的目的是_____。
(4)电解 CuSO4 溶液时,阳极的电极反应式为_____。
(5)锡、铅渣中的铅主要以 PbSO4 存在,脱硫时发生的反应为PbSO4+HCO3-(aq)  PbCO3 (s)+H+(aq)+SO4 2-(aq)。脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是___。
PbCO3 (s)+H+(aq)+SO4 2-(aq)。脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是___。
(6)若该冶炼废渣中锡的质量分数为 5%,30t 废渣制得精锡 lt,则锡的回收率为_____。
-
电解精炼锡后的阳极泥中除含有一定量的Sn外,还含有Ag、Bi、Cu等金属,极具回收价值。某锡冶炼厂采用纯湿法工艺从阳极泥中提取Ag、Bi、Cu,流程如下:
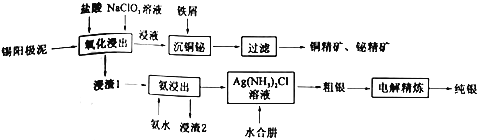
已知:①BiCl3+H2O BiOCl+2HCl
BiOCl+2HCl
②SnO2不溶于稀酸和碱溶液
(1)锡阳极泥在“氧化浸出”前需粉碎处理,目的是__________________________。
(2)“氧化浸出"时Cu发生反应的离子方程式为______________________。
(3)浸渣1的主要成分为AgCl和SnO2,则“氨浸出“时发生反应的化学方程式为______________。
(4)水合肼(N2H4·H2O)起_________作用(填“还原”或“氧化”)。已知N2H4为二元弱碱,在水中的电离与氨相似,其第一步电离的方程式为________________________。
(5)粗银电解冶炼时用_________作阳极,用_________溶液作电解液。
(6)“沉铜铋”时应将溶液的pH调至0.5~1.0之间,目的是____________________。
-
金属钒主要用于冶炼特种钢和在化学工业、炼油工业中作催化剂,被誉为“合金的维生素”。回收利用废钒催化剂(主要成分为V2O5、VOSO4和二氧化硅)的工艺流程如下图所示。
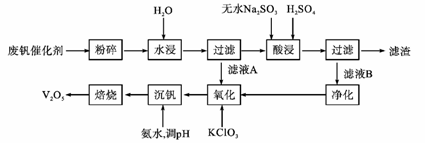
(1) 粉碎的作用是_______,滤渣可用于_______(填用途)。
(2) 25时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如下表所示:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 91.8 | 96.5 | 98 | 99.8 | 9.8 | 96.4 | 93.0 | 89.3 |
根据上表数据判断,加入氨水调节溶液pH的最佳选择为_____;上述过滤操作过程中所需用到的玻璃仪器有__________。
(3)为了提高钒的浸出率,用酸浸使废钒催化剂中的V2O5转变成可溶于水的VOSO4,酸浸过程中还原产物和氧化产物的物质的量之比为_______。
(4)完成并配平氧化过程中的离子方程式:_____
_____ClO3-+ VO2+ + = VO3++ Cl-+ 。
(5)废钒催化剂中V2O5的质量分数为6%(原料中的所有钒已换算成V2O5)。取100g此废钒催化剂按上述流程进行实验,当加入105 mL 0.1 mol·L-1的KClO3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该工业生产中钒的回收率是________。
-
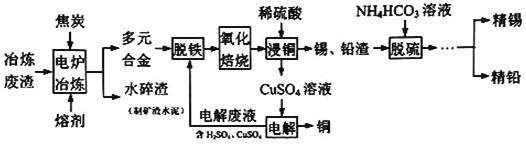
金属的回收是工业生产中的重要课题,利用某工业冶炼废渣 主要成分为
主要成分为 和铁、锡、铅、铜的氧化物
和铁、锡、铅、铜的氧化物 回收锡、铜、铅的工艺流程如图所示:
回收锡、铜、铅的工艺流程如图所示:
回答下列问题:
 电炉冶炼时,焦炭的作用是______
电炉冶炼时,焦炭的作用是______ 填“氧化剂”或“还原剂”
填“氧化剂”或“还原剂” ,将焦炭粉碎的目的是______。熔剂的主要成分是氟石
,将焦炭粉碎的目的是______。熔剂的主要成分是氟石 ,高温下能与
,高温下能与 反应生成两种钙盐,其中之一为CaSiF6,该反应的化学方程式为______。
反应生成两种钙盐,其中之一为CaSiF6,该反应的化学方程式为______。
 脱铁后的溶液中含有少量的
脱铁后的溶液中含有少量的  ,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为______。
,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为______。
 已知
已知  可表示为:
可表示为: ,则
,则  也可用氧化物表示为:______。
也可用氧化物表示为:______。
 脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是______。
脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是______。
 若该冶炼废渣中锡的质量分数为
若该冶炼废渣中锡的质量分数为  ,30t 废渣制得精锡
,30t 废渣制得精锡  ,则锡的回收率为______。
,则锡的回收率为______。
-
镓是制作高性能半导体的重要原料。工业上常从锌矿冶炼的废渣中回收镓。已知某锌矿渣主要含Zn、Si、Pb、Fe、Ga的氧化物,利用该矿渣制镓的工艺流程如下:
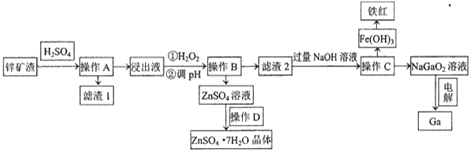
已知:①镓在元素周期表中位于第四周期第ⅢA,化学性质与铝相似。
②lg2=0.3,lg3=0.48。
③部分物质的Ksp如F表所示
(1)滤渣1的主要成分是_________(写化学式)。
(2)加入H2O2的目的是(用离子方程式表示)___________。
(3)调pH的目的是______;室温条件下,若浸出液中各阳离子的浓度均为0.01 mol/L,当溶液中某种离子浓度小于 mol/L时即认为该离子已完全除去,则pH应调节的范围为_______。
mol/L时即认为该离子已完全除去,则pH应调节的范围为_______。
(4)操作D包括:__________过滤、洗涤、干燥。
(5)制备、精炼金属Ga。
①电解法制备金属镓。用惰性电极电解 溶液即可制得金属镓,写出阴极电极反应式_________。
溶液即可制得金属镓,写出阴极电极反应式_________。
②电解法精炼金属镓(粗镓含Zn、Fe、Cu等杂质,已知氧化性:
下列有关电解精炼金属镓的说法正确的是_______(填字母序号)。
A .电解精炼镓时粗镓与电源的正极相连
B. 电解精炼过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,Cu和Fe沉积在电解槽底部形成阳极泥
D. 若用甲烷燃料电池电解精炼金属镓,当阴极有56.0 g镓析出时,电池负极最多消耗标准状况下的 6.72 L
6.72 L
-
辉铜矿是铜矿的主要品种之一传统的火法冶炼在资源的综合利用、环境保护等方面会遇到困难。辉铜矿的湿法冶炼目前国内外都处于探索阶段。自氧化还氨氮分离法是一种较为理想的湿法冶炼方法,工艺流程如下图所示:
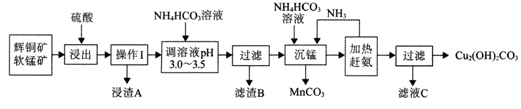
已知:
① 辉铜矿的主要成分是Cu2S,含有较多的Fe2O3、SiO2等。
② 软锰矿的主要成分是MnO2,含有较多的SiO2等。
③ 浸出时,生成一种非金属单质。
④ 室温下,Kap[Fe(OH)3]=4.0×10-38mol/L,Kap[Fe(OH)2]=8.0×10-16mol/L
完成下列填空:
(l)浸出前需要先将矿石粉碎,其目的是__________。
(2)写山浸出时主要反应的离子方程式_____________。
(3)浸渣A的主要成分为_______;调溶液pH 3.0-3.5的目的是除去______离子;室温下,若该离子的浓度为4.0×10-8mol/L,则溶液的pH=__________。
(4) 工业上可将MnCO3、在300℃左右氧化来制取具有较好催化性能的MnO2,则MnCO3在空气中受热制取MnO2的化学方程式为_________________。
(5)从滤液C中提取硫酸氨晶体的步骤为_______、_______、过滤、洗涤、干操。
(6)与火法冶炼辉铜矿相比,用图中方法冶炼辉铜矿的优点有________、_____。(列举其中2条)


Au++2HCN,该反应的K=____________。










