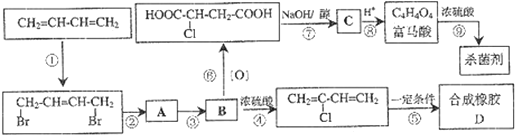
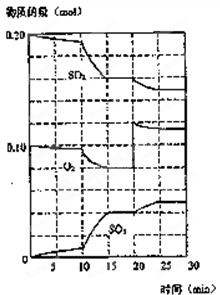
-
下列各组气体或溶液用括号内试剂加以鉴别,其中不合理的是( )
A.二氧化碳、二氧化硫、一氧化碳(品红试液)
B.氯化钠、硝酸银、碳酸钠(稀盐酸)
C.酒精、醋酸、醋酸钠(石蕊试液)
D.硫酸、硝酸钡、氯化钾(碳酸钠溶液)难度: 中等查看答案及解析
-
有关晶体的下列说法中正确的是( )
A.晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠熔化时离子键未被破坏难度: 中等查看答案及解析
-
下列实验操作中,错误的是( )
A.配制5%食盐溶液时,将称量的食盐放入烧杯中加适量的水搅拌溶解
B.铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C.测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2-3次
D.配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释难度: 中等查看答案及解析
-
下列产品的使用不会对环境造成污染的是( )
A.含磷洗衣粉
B.酒精
C.氟利昂
D.含汞电池难度: 中等查看答案及解析
-
下列物质中属于离子化合物的是( )
A.苛性钠
B.碘化氢
C.硫酸
D.醋酸难度: 中等查看答案及解析
-
据报道,月球上有大量3He存在,以下关于3He的说法正确的是( )
A.是4He的同素异形体
B.比4He多一个中子
C.是4He的同位素
D.比4He少一个质子难度: 中等查看答案及解析
-
在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是( )
A.Mg
B.Cu
C.Ag
D.H2难度: 中等查看答案及解析
-
氢氧化铁胶体稳定存在的主要原因是( )
A.胶粒直径小于1nm
B.胶粒作布朗运动
C.胶粒带正电荷
D.胶粒不能通过半透膜难度: 中等查看答案及解析
-
下列物质中不会因见光而分解的是( )
A.NaHCO3
B.HNO3
C.AgI
D.HClO难度: 中等查看答案及解析
-
实验室制取下列气体,其反应放热的是( )
A.由无水醋酸钠制CH4
B.由乙醇制C2H4
C.由电石制C2H2
D.由氯酸钾制O2难度: 中等查看答案及解析
-
将A g块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如下图的实线所示,在相同的条件下,将Bg(A>B)粉末状碳酸钙与同浓度盐酸反应,则相应的曲线(图中虚线所示)正确的是( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
将标准状况下的2.24L CO2通入150mL 1mol/LNaOH溶液中,下列说法正确的是( )
A.c(HCO3-)略大于c(CO32-)
B.能使酸性高锰酸钾溶液褪色
C.c(Na+)等于c(CO32-)与c(HCO3-)之和
D.c(HCO3-)略小于c(CO32-)难度: 中等查看答案及解析
-
据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:HC≡C-C≡C-C≡C-C≡C-C≡N.对该物质判断正确的是( )
A.晶体的硬度与金刚石相当
B.能使酸性高锰酸钾溶液褪色
C.不能发生加成反应
D.可由乙炔和含氮化合物加聚制得难度: 中等查看答案及解析
-
下图中能验证氯化钠溶液(含酚酞)电解产物的装置是( )
A.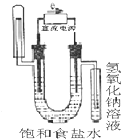
B.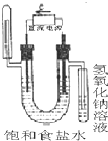
C.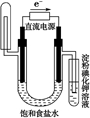
D.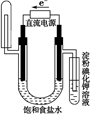
难度: 中等查看答案及解析
-
下列离子方程式中正确的是( )
A.硫化亚铁放入盐酸中 S2-+2H+→H2S↑
B.硫酸铜溶液中通入硫化氢 Cu2++H2S→CuS↓+2H+
C.氯化铝溶液中加入过量氯水 Al3++4NH3•H2O→AlO2-+4NH4++2H2O
D.碳酸氢铵溶液中加入过量氢氧化钠溶液 HCO3-+OH-→CO32-+H2O难度: 中等查看答案及解析
-
CuS和Cu2S都能溶于硝酸,它们高温灼烧的产物相同,以下鉴别CuS和Cu2S两种黑色粉末的方法合理的是( )
A.将两种样品分别溶于硝酸,区别所产生的气体
B.将两种样品分别溶于硝酸,区别溶液的颜色
C.取两种同质量的样品分别在高温灼烧,区别残留固体的质量
D.取两种同质量的样品分别在高温灼烧,区别残留固体的颜色难度: 中等查看答案及解析
-
将表面已完全钝化的铝条(表面是一层Al2O3薄膜),插入下列溶液中,不会发生反应的是( )
A.稀硝酸
B.稀盐酸
C.硝酸铜
D.氢氧化钠难度: 中等查看答案及解析
-
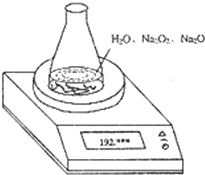
等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的
(同温同压),这时混合气体中N2、O2、CO2的物质的量之比为( )
A.3:4:1
B.3:3:2
C.6:7:3
D.6:9:0难度: 中等查看答案及解析
-
设NA为阿佛加德罗常数,下列叙述中正确的是( )
A.46 g NO2 和 N2O4混合气体中含有原子数为3NA
B.标准状况下22.4 L H2 中含中子数为2NA
C.1L 1mol/L醋酸溶液中离子总数为2NA
D.1mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子难度: 中等查看答案及解析
-
下列两种气体的分子数一定相等的是( )
A.质量相等、密度不等的N2和C2H4
B.等体积等密度的CO和C2H4
C.等温等体积的O2和N2
D.等压等体积的N2和CO难度: 中等查看答案及解析
-
常温时,向pH=2的硫酸中加入等体积的下列溶液后,滴入甲基橙试液,出现红色,该溶液可能是( )
A.pH=12的Ba(OH)2
B.pH=12的氨水
C.0.005 mol/L NaOH
D.0.05 mol/L BaCl2难度: 中等查看答案及解析
-
某芳香族有机物的分子式为C8H6O2,它的分子(除苯环外不含其他环)中不可能有( )
A.两个羟基
B.一个醛基
C.两个醛基
D.一个羧基难度: 中等查看答案及解析