-
Na2CO3的水溶液呈碱性,下列说法错误的是( )
A.碳酸钠在水中会电离出OH﹣
B.往碳酸钠溶液中加稀硫酸后溶液的pH降低
C.碳酸钠溶液中存在OH﹣
D.往碳酸钠溶液中滴加紫色石蕊试液后溶液显蓝色
难度: 简单查看答案及解析
-
如图所示的实验操作或装置正确的是( )




A.倾倒液体 B.氢气还原氧化铜 C.加热液体 D.稀释浓硫酸
难度: 简单查看答案及解析
-
下列是分析已变质氢氧化钠溶液的相关实验,其中合理的是( )
序号
实验目的
实验过程
①
证明变质
取少量溶液,滴加盐酸,将生成的气体通入石灰水
②
确定成分
取少量溶液,加入石灰水,过滤,向滤液中滴加酚酞溶液
③
测定纯度
取一定量溶液,加入浓盐酸,用氢氧化钠固体吸收气体,称量
④
除去杂质
取溶液,滴加石灰水至恰好完全反应,过滤
A.②③ B.①③ C.②④ D.①④
难度: 简单查看答案及解析
-
向盛有某液体的烧杯中逐滴加入x溶液至过量(如图1),生成沉淀或气体的质量与加入x溶液的质量关系符合图2的是( )
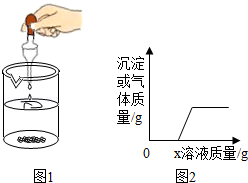
A.烧杯中的物质:H2SO4和CuSO4溶液,x溶液:NaOH溶液
B.烧杯中的物质:NaHCO3和NaCl溶液,x溶液:稀盐酸
C.烧杯中的物质:镁铝合金,x溶液:稀盐酸
D.烧杯中的物质:稀盐酸和稀硫酸,x溶液:Na2CO3溶液
难度: 中等查看答案及解析
-
向AgNO3、Cu(NO3)2和Mg(NO3)2的混合溶液中加入一些铁粉,充分反应后过滤.下列说法正确的是( )
A.滤纸上一定有Ag和Cu
B.滤纸上一定有Ag,可能有Cu、Fe和Mg
C.滤液中可能含有Fe2+、Mg2+
D.滤液中一定有Fe2+、Mg2+,可能含有Ag+、Cu2+
难度: 中等查看答案及解析
-
建立宏观和微观之间的联系是一种科学的思维方式,下列宏观事实的微观解释不正确的是( )
A.白色的无水硫酸铜遇水变蓝色,是因为CuSO4遇H2O转化为CuSO4•5H2O
B.警用缉毒犬能根据气味发现毒品,是因为分子在不断运动
C.5mL酒精和5mL水混合后体积小于10mL,是因为混合过程中分子变小了
D.不同种酸的化学性质有所不同,与酸电离生成的阴离子不同有关
难度: 简单查看答案及解析
-
用三块相同的铝片(均已去除氧化膜)进行如下实验.
实验1:取第一块铝片,放入稀硫酸中,有明显的现象
实验2:取第二块铝片,放入硫酸铜溶液中,铝片表面有红色物质析出
实验3:取第三块铝片,放入浓硫酸中,无明显的现象
实验4:将实验3中的铝片取出,洗净后放入硫酸铜溶液中,没有明显的现象
下列说法不正确的是( )
A.在实验1中可以观察到铝片表面有气泡产生
B.由实验2可以得出金属铝比铜活泼
C.铝片与浓硫酸不能发生化学反应
D.浓硫酸与稀硫酸的化学性质有差别
难度: 简单查看答案及解析
-
某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )

A.金属活动性由强到弱:X、Z、Y B.金属活动性由强到弱:X、Y、Z
C.X、Y、Z依次可能是Mg、Zn、Fe D.相对原子质量的大小:Y>Z>X
难度: 中等查看答案及解析
-
去年杭州市出现了明显的暖冬,冬季平均气温比正常年份明显偏高,科学家认为这是大气中CO2含量的增加而引起的“温室效应”.如何防止温室效应的加剧,科学家提出多种方法,其中有人提出将C02通过高压管道,通入深海海底储存,以减少CO2的排放,但也有一些人提出反对意见.下列反对意见中,你认为错误的是( )
A.将C02收集和通人深海海底要消耗大量的能源,消耗能源也会加剧C02的排放
B.几十万年以来,海水的pH保持在8.2左右,大量C02溶解在海水中,会使海水的酸性增大,破坏海洋的生态环境
C.将C02储存在海底,会严重影响陆上植物的光合作用
D.当发生海底地震时,深海海底储存的C02会被重新释放到大气中
难度: 简单查看答案及解析

