-
下列实验“操作和现象”与“结论”对应关系正确的是( )
操作和现象
结论
A
向装有Fe(NO3)2溶液的试管中加入稀H2SO4后,在试管口观察到红棕色气体
HNO3分解生成了NO2
B
向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有砖红色沉淀生成
淀粉不一定没有水解
C
向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去
使溶液褪色的气体是乙烯
D
常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有少量气泡产生
证明常温下KSP(BaSO4)>KSP(BaCO3)
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
化学与生产、生活、环境等社会实际密切相关。下列叙述正确的是( )
A. “滴水石穿、绳锯木断”不涉及化学变化
B. 明矾净水的原理和消毒液消毒的原理不相同
C. 氟利昂作制冷剂会加剧雾霾天气的形成
D. 汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数,下列说法正确的是( )
A. 2.3 g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1NA
B. 100g9.8%的硫酸与磷酸的混合液中含有氧原子数为0.4NA
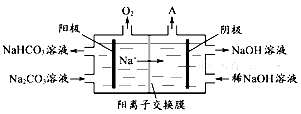
C. 惰性电极电解食盐水,若线路中通过1NA电子电量,则阳极产生气体11.2L
D. 0.1 mol的CaC2中含阴离子数是0.2 NA
难度: 中等查看答案及解析
-
下列相关反应的离子方程式书写正确的是( )
A. 氢氧化铁溶于氢碘酸:Fe(OH)3+3H+
Fe3++3H2O
B. 向含有0.4 mol FeBr2的溶液中通入0.1 mol Cl2:2Fe2++Cl2
2Fe3++2Cl-
C. NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-
AlO2-+2BaSO4↓+2H2O
D. NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-
BaCO3↓+2H2O+ CO32-
难度: 中等查看答案及解析
-
实现下列变化时,需克服相同类型作用力的是( )
A. 纯碱和烧碱的熔化 B. 食盐和冰醋酸熔化
C. 液溴和水晶的气化 D. 金刚石和干冰的熔化
难度: 简单查看答案及解析
-
好莱坞影片《终结者》中始终不会被击败的液态金属机器人,在被散弹枪和手榴弹击中后,既能像液体一样重新聚集在一起,恢复之前的结构,又能改变外形,呈现出各种造型。清华大学刘静教授等人联合中国科学院理化技术研究所研发出世界首个自主运动的可变液态金属机器。研究揭示,置于电解液中的镓基液态合金可通过“摄入”铝作为食物或燃料提供能量,实现高速、高效长时运转,这种柔性机器既可在自由空间运动,又能于各种结构槽道中蜿蜒前行,因此作者们将其命名为“液态金属软体动物”。下列关于此研究的说法正确的是( )
A. 人们最熟悉的液态金属是水银,因其价格太贵而限制了实际应用
B. 液态金属中存在的粒子有金属阳离子和自由电子,它们之间通过静电作用形成离子键
C. 铝在液态金属中燃烧放出热量从而提供能量,使液态金属实现高速、高效的长时运转
D. 液态金属机器“吞食”铝片后,在电解质里形成原电池反应,会产生电力和气泡,从而产生动力
难度: 困难查看答案及解析
-
下列图示实验合理的是 ( )
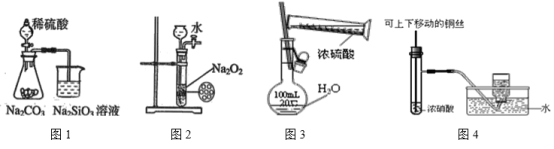
A. 图1为证明S、C、Si元素的非金属性强弱的装置
B. 图2为可随开随停制备少量氧气的装置
C. 图3为配制100mL一定浓度硫酸溶液
D. 图4制备并收集少量NO2气体
难度: 中等查看答案及解析
-
下列化学用语正确的是( )
A. 硫原子结构示意图:
B. 乙烯分子的结构式:CH2=CH2
C. H2O2的电子式:H+[
]H+
D. 碳酸氢钠的电离方程式NaHCO3=Na++HCO3-
难度: 简单查看答案及解析
-
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
① C、CO ② AlCl3 、Al(OH)3 ③ Na、 Na2O
④ NaOH 、Na2CO3 ⑤ AlO2 -、Al(OH)3 ⑥ Fe、Cl2
A. ①②⑥ B. ①②③④⑤
C. ①②③④⑤⑥ D. ①②④
难度: 中等查看答案及解析
-
下列有关有机物的说法正确的是( )
A. 分子式为C4H10的二氯取代物的同分异构体有8种
B. 相对分子质量相差14或14的整数倍的有机物互为同系物
C. 1mol有机物
最多可与5molH2发生加成反应
D. 用氯乙烯制聚氯乙烯的原子利用率为100%
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期且相邻,Z是地壳中含量最多的元素,W是短周期中金属性最强元素。下列说法正确的是( )
A. 原子半径: r(X) < r(Y) < r(Z) < r(W)
B. W的最高价氧化物的水化物是一种弱碱
C. Y的单质的氧化性比Z的强
D. X、Y、Z 三种元素可以组成共价化合物和离子化合物
难度: 中等查看答案及解析
-
下列变化不能用勒夏特列原理解释的是 ( )
A. 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
B. 红棕色的NO2加压后颜色先变深再变浅
C. H2、I2(g)混合气体加压后颜色变深
D. 实验室用排饱和食盐水的方法收集氯气
难度: 简单查看答案及解析
-
下列物质在给定条件下的同分异构体数目正确的是( )
A. C4H10属于烷烃的同分异构体有3种
B. 分子组成是C5H10O2属于羧酸的同分异构体有5种
C. 分子组成是C4H8O属于醛的同分异构体有3种
D. 结构简式为
的一溴代物有5种
难度: 困难查看答案及解析
-
在25℃时将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后,下列关系式中正确的是( )
A. c(Na+)=c(CH3COO-)+c(CH3COOH)
B. c(H+)=c(CH3COO-)+c(OH-)
C. c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D. c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
难度: 中等查看答案及解析
-
光电池是发展性能源。一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl (s)
Ag (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-=Cl- (aq),若将光源移除,电池会立即恢复至初始状态。下列说法不正确的是( )
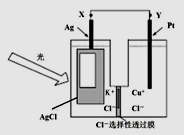
A. 光照时,电流由X流向Y
B. 光照时,Pt电极发生的反应为:2Cl-+2e-=Cl2↑
C. 光照时,Cl-向Pt电极移动
D. 光照时,电池总反应为:AgCl(s)+Cu+(aq)
Ag(s)+Cu2+(aq)+Cl-(aq)
难度: 困难查看答案及解析
-
常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,Kb (NH3·H2O) =1.76×10-5,下列说法正确的是( )
A. 浓度均为0.1 mol·L-1的 HCOONa和NH4Cl 溶液中阳离子的物质的量浓度之和:前者小于后者
B. 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等
C. 0.2 mol·L-1 HCOOH 与 0.1 mol·L-1 NaOH 等体积混合后的溶液中: c(HCOO-) + c(OH-) = c(HCOOH) + c(H+)
D. 0.10 mol·L-1CH3COONa溶液中通入HCl至溶液呈中性:c(Na+)>c(Cl-)=c(CH3COOH)
难度: 困难查看答案及解析