-
(物质结构与性质)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
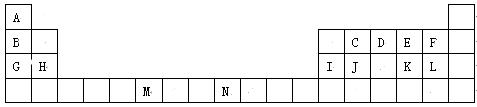
试回答下列问题:
(1)请写出元素N的基态原子电子排布式 。
(2)元素B、G形成的单质熔点更高的是_ ___(填化学式),原因是____ _
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是__________(填“极性”或“非极性”)分子。
(4)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有___________(填序号),CS2分子的空间构型是__________。
(5)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为 。
-
【化学一物质结构与性质】(15分)
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素n的基态原子的价电子排布式 ,元素O在周期表的位置是 ,属于 区。
(2)k在空气中燃烧产物的分子构型为 ,中心原子的杂化方式为 ,该分子是 (填“极性”或“非极性”)分子。
(3)第三周期8种元素按单质熔点高低的顺序如左下图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填下图中的序号)。
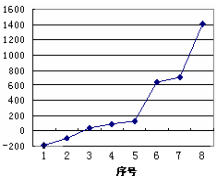
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如右下图乙所示。则晶胞中i原子的配位数为 。
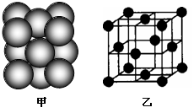
-
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
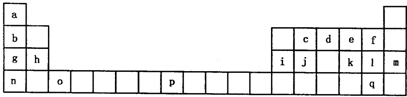
试回答下列问题:
(1)请写出元素o的基态原子电子排布式______,g元素的价电子的四个量子数依次是______.
(2)d的氢化物中心原子的杂化方式是______.
(3)o元素所在族的符号是______.
(4)d的氢化物与l的氢化物反应后的产物中包含的化学键是______.
(5)f、l、q的氢化物中沸点最高的是______.(写化学式)
(6)j原子形成的晶体与j原子跟c原子以1:1相互交替结合而形成的jc晶体类型相同.则j晶体的熔点______jc晶体的熔点(填“大于”“等于”“小于”)原因是______.
-
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)元素p为26号元素,请写出其原子的三价阳离子的电子排布式:______________。
(2)e与a反应的产物的分子中中心原子的杂化形式为__________,该分子是__________(填“极性”或“非极性”)分子。
(3)请写出f的氢化物在水中所存在氢键的表达式:(任写两种即可)_________________________。
(4)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p |
| 电离能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 |
| I3 | 3 248 | 2 957 |
| | | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是___________________________________;
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
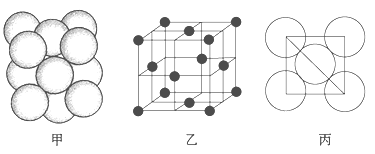
请问晶胞中i原子的配位数为________,一个晶胞中i原子的数目为________。
-
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:

(1)元素p为26号元素,请写出其基态原子的电子排布式________________。
(2)d与a反应的产物的分子中,中心原子的杂化形式为________________。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:________________________________________________。
(4)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p |
| 电离能/ (kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 |
| I3 | 3 248 | 2 957 |
| | | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是____________________________________。
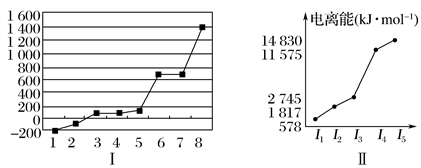
(5)第三周期8种元素按单质熔点高低的顺序如图Ⅰ所示,其中电负性最大的是________(填图中的序号)。
(6)表中所列的某主族元素的电离能情况如图Ⅱ所示,则该元素是________(填元素符号)。
-
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
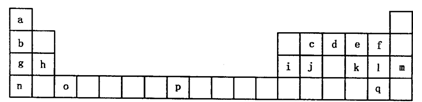
试回答下列问题:
(1)请写出元素o的基态原子电子排布式________,g元素的价电子的四个量子数依次是________。
(2)d的氢化物中心原子的杂化方式是________。
(3)o元素所在族的符号是________。
(4)d的氢化物与l的氢化物反应后的产物中包含的化学键是________。
(5)f、l、q的氢化物中沸点最高的是________。(写化学式)
(6)j原子形成的晶体与j原子跟c原子以1:1相互交替结合而形成的jc晶体类型相同。则j晶体的熔点________jc晶体的熔点(填“大于”“等于”“小于”)原因是________
-
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
试回答下列问题:
(1)请写出元素m的基态原子电子排布式______.
(2)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表______(填元素符号);其中电负性最大的是______(填图1中的序号).
(3)由a原子跟f原子以1:1相互交替结合而形成的晶体,晶型与晶体f相同.两者相比熔点更高的是______(填化学式).
(4)b、n、m元素化合物的晶体中的晶胞堆积方式如图2所示:
请回答:该化合物的化学式是:______(用元素符号表示),与m原子距离相等且最接近的m原子数为______.
-
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)写出元素g的基态原子电子排布式______________________。
(2)f在空气中燃烧产物的分子构型为____________,中心原子的杂化形式为____________,该分子是___________(选填“极性”、“非极性”)分子。
(3)由a原子跟e原子以1 : 1相互交替结合而形成的晶体,晶型与晶体e相同。两者相比熔点更高的是_____________(填化学式),试从结构角度加以解释______________________。
(4)c单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。
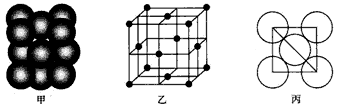
若已知c的原子半径为d厘米,NA代表阿伏加德罗常数,c的相对原子质量为M,请回答:①晶胞中c原子的配位数为_____,表示原子空间占有率的代数式为_____________。
②该晶体的密度为_____________g/cm3(用含有关字母的代数式表示),b、h中,与c单质晶体中原子的堆积方式相同的是__________(填元素符号)。
-
图是元素周期表中的一部分,表中所列字母分别代表一种化学元素,请回答下列问题:
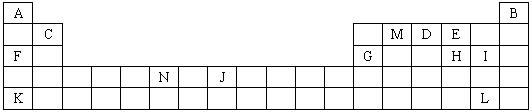
(1)上述所列元素的原子中,最外层电子层上只有两个电子的是______;(填“元素符号”)
(2)下列叙述正确的是______;(填字母序号)
a.K的最高价氧化物对应的水化物是一种强碱
b.硒化氢的稳定性强于H的氢化物的热稳定性
c.F与H形成化合物水溶液的pH大于F与I形成化合物水溶液的pH,说明相同浓度氢化物水溶液的酸性H弱于I
d.MA2E分子中M原子采取SP2杂化方式
e.N的电子排布式:ls22s22p63s23p63d44s2
f.电负性由大到小的顺序:E>D>M
g.第一电离能由大到小的顺序:E>D>M
(3)预测DA4+离子的空间构型为______,ME2的空间构型为______;
(4)向含有CoCl3•5NH3的溶液中加入硝酸银溶液,可析出AgCl沉淀.经测定,每1mol CoCl3•5NH3只生成2molAgCl.
请写出表示此配合物结构的化学式(钴的配位数为6):______,此配合物中Co的化合价为______.
-
(物质结构)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.请根据上表回答下列问题:

(1)G元素基态原子的电子排布式为______,其气态氢化物易液化,其原因是______.
(2)XR2中,X原子的轨道杂化类型为______,化合物ER2的熔点较XR2低,其原因是______.
(3)E、G、R三种元素的第一电离能由大到小的顺序是______(用元素符号填空).
(4)由A、E、G、R四种元素所形成的微粒中互为等电子体的有多组,请写出其中两组的化学式______.
(5)单质Z的晶体在1183K以下时为体心立方堆积,在1183K以上时为面心立方堆积,其晶胞结构如图所示.则体心立方晶胞和面心立方晶胞中实际含有的Z原子的个数之比为______.Z3+比Z2+更稳定一些,其原因可能是______.













