-
合金在生产生活中具有广泛的用途。不属于合金的是
A. 明矾 B. 硬铝 C. 生铁 D. 青铜
难度: 简单查看答案及解析
-
12C和13C原子之间,相等的是
A. 原子质量 B. 中子数 C. 质量数 D. 电子数
难度: 简单查看答案及解析
-
含有共价键的离子晶体是
A. H2SO4 B. KOH C. MgCl2 D. Na2O
难度: 中等查看答案及解析
-
硫化氢能与二氧化硫反应,说明硫化氢具有
A. 还原性 B. 氧化性 C. 酸性 D. 不稳定性
难度: 中等查看答案及解析
-
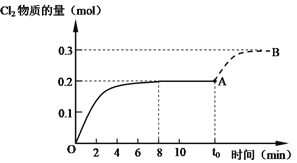
化学反应中的能量变化符合如图所示的是
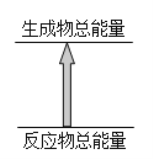
A. 甲烷燃烧
B. 碳酸钙高温分解
C. 电石与水反应
D. 酸碱中和
难度: 中等查看答案及解析
-
铁在一定条件下与下列物质发生的反应,不属于置换反应的是
A. 水 B. 稀盐酸 C. 硫粉 D. 硫酸铜
难度: 中等查看答案及解析
-
氮是植物生长的必需元素。有关说法中错误的是
A. 氮气分子很稳定 B. 氨气是极性分子
C. 尿素属于铵态氮肥 D. 闪电实现了大气固氮
难度: 中等查看答案及解析
-
有关Al2O3的叙述正确的是
A. 可用于净水 B. 是碱性氧化物
C. 可与水化合成Al(OH)3 D. 可通过铝热反应生成
难度: 中等查看答案及解析
-
下列物质中能使酸性高锰酸钾溶液褪色的是
A. 溴乙烷 B. 乙酸乙酯 C. 甲烷 D. 乙炔
难度: 中等查看答案及解析
-
物质之间发生化学反应时,一定发生变化的是
A. 总物质的量 B. 原子个数 C. 化学键 D. 化合价
难度: 中等查看答案及解析
-
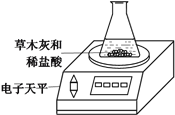
测定胆矾晶体中结晶水含量的实验中,有关操作所用仪器错误的是

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
有关水的表述正确的是
A. 电子式为
 B. 是直线型分子
B. 是直线型分子C. 是非电解质 D. 可以作氧化剂
难度: 中等查看答案及解析
-
能证明乙酸是弱酸的是
A. 乙酸钠溶液pH>7 B. 乙酸溶液能导电
C. 乙酸溶液能使石蕊变红 D. 乙酸溶液易挥发
难度: 中等查看答案及解析
-
氧和硫是同主族元素,下列事实不能说明氧的非金属性比硫强的是
A. 酸性:H2S>H2O B. 热稳定性:H2O>H2S
C. 原子半径:S>O D. 化合价:SO2中S为正价
难度: 中等查看答案及解析
-
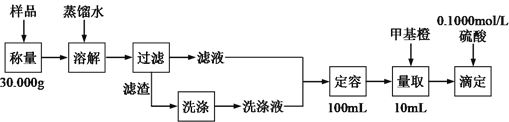
海水提溴和海带提碘都需要经过浓缩、氧化、提取三个步骤。有关叙述错误的是
A. 提溴的浓缩液来自于海水晒盐后的卤水 B. 氧化步骤都可以通入氯气来实现
C. 提取溴时利用溴的挥发性 D. 提取碘时利用碘的升华特性
难度: 中等查看答案及解析
-
用如图所示装置研究电化学腐蚀及防护。关于I和II的叙述正确的是

A. 负极反应均是Fe-2e → Fe2+
B. 正极反应均是O2+2H2O+4e → 4OH-
C. 均是化学能转变为电能
D. 铁均被保护
难度: 中等查看答案及解析
-
实验室加热浓H2SO4和乙醇混合液制乙烯。有关说法正确的是
A. 向烧瓶中依次加入碎瓷片、浓H2SO4和酒精
B. 用温度计测量生成气体的温度
C. 温度过高时制得的乙烯中混有SO2
D. 用排气法收集乙烯
难度: 中等查看答案及解析
-
合成氨是人类科学技术上的一项重大突破,有关合成氨的说法正确的是
A. 升温能提高氢气的转化率
B. 采用20~50 MPa能提高催化剂的效率
C. 使用催化剂能提高NH3的百分含量
D. 循环使用未反应的N2和H2能节约成本
难度: 中等查看答案及解析
-
化工生产要遵守三大原则:充分利用原料、充分利用能量、保护环境。下列描述不符合以上原则的是
A. 煅烧硫铁矿时使用沸腾炉 B. 制盐酸时通入过量氯气使氢气反应完全
C. 制硫酸时使用热交换器 D. 氨碱法生产中循环使用氨气和二氧化碳
难度: 中等查看答案及解析
-
某溶液中可能含有Na+、Al3+、Fe3+、NO3-、SO42-、Cl-,滴入过量氨水,产生白色沉淀,若溶液中各离子的物质的量浓度相等,则一定存在的离子是
A. SO42- B. NO3- C. Na+ D. Fe3+
难度: 中等查看答案及解析