-
草木灰的有效成分是K2CO3,还含有少量的Na+、Cl-、SO42-和大量不溶于水的固体。为测定其中K2CO3的含量,设计如下实验:
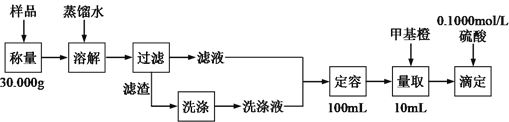
完成下列填空:
(1)洗涤滤渣的目的是_____________________________________。
(2)配制100 mL草木灰浸出液,需要使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、______。
(3)取用10.00 mL浸出液进行滴定,终点时溶液由______色变成______色。若三次平行实验消耗硫酸体积的平均值为25.00 mL,则该样品中碳酸钾的质量分数为______(精确到小数点后3位)。
(4)若没有用标准液润洗滴定管,则实验结果将___(填“偏大”、“偏小”或“无影响”)。
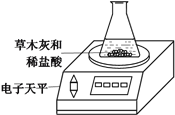
(5)利用如图装置,通过反应前后总质量的改变,确定CO2气体的质量,也可以测定样品中碳酸钾的含量。实验时发生反应的离子方程式为_______________________。判断反应完全的依据是_____________________。请对该实验方案的优缺点进行评价。________________
-
铵态氮肥不能与草木灰(有效成分K2CO3)混用的原因是铵态氮肥
A. 呈酸性 B. 受热易分解 C. 易溶于水 D. 遇碱放出氨气
-
化学与生产、生活息息相关,下列说法正确的是
A. SO2、CO2、NO2都是可形成酸雨的气体
B. 农业施肥作业时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用
C. 地沟油不宜食用,可以分馏提取汽油,做汽车的燃料
D. 向牛奶中加入果汁会产生沉淀,是因为发生了酸碱中和反应
-
下列有关“化学与生活”的叙述不正确的是
A.凡含有食品添加剂的食物对人体健康均有害
B.使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱
C.施肥时,农家肥草木灰(有效成分K2CO3)不能与氮肥NH4Cl混合使用
D.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质
-
蛋壳的主要成分是CaCO3,含有少量的SiO2、MgCO3及色素等杂质,测定蛋壳中钙含量的操作步骤如图所示:
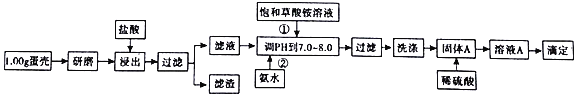
已知: CaC2O4、MgC2O4都难溶于水。
回答下列问题:
(1)样品溶于盐酸后得到的滤渣主要是______________。
(2)①②操作时,加入饱和(NH4)2C2O4溶液和氨水的作用是_________。
(3)洗涤固体A最好选用“冰水”洗涤,其目的是___________。
(4)在一定温度下,向2L的密闭容器中放人足量的草酸钙(固体所占体积忽略不计)发生反应: CaC2O4(s) CaO(s)+CO(g)+CO2(g) 若前5min内生成CaO的质量为l1.2g,则该段时间内v(CO)=_________。
CaO(s)+CO(g)+CO2(g) 若前5min内生成CaO的质量为l1.2g,则该段时间内v(CO)=_________。
(5)用标准酸性高锰酸钾溶液滴定生成的草酸,通过钙与草酸的定量关系,可间接求出钙的含量。
步骤1: 将溶液A加蒸馏水稀释至250mL。
步骤2: 取稀释后的溶液25.00mL于锥形瓶中,加稀H2SO4酸化。
步骤3: 用0.0190mol/LKMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1mI。
步骤4: 重复步骤2、步骤3的操作3次,记录数据如下表:
| 实验编号 | KMnO4溶液的浓度(mol/L) | KMnO4液滴入的体积(mL) |
| 1 | 0.0190 | V1=20.02 |
| 2 | 0.0190 | V2=20.00 |
| 3 | 0.0190 | V3=19.98 |
| 4 | 0.0190 | V4=20.80 |
①滴定终点的现象是______________________。
②该蛋壳中CaCO3的质量分数=______%,则此法求得的钙含量_____实际值(填“>”“=”或“<”)。
-
有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl—、SO42—、HCO3—、MnO4—中的几种。为确定其成分,做如下实验:①取部分溶液,加入少量Na2O2固体,产生无色无味的气体和白色沉淀,再加入过量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是
A.肯定有Al3+、Mg2+、HCO3— B.肯定有A13+、Mg2+、SO42—
C.肯定没有HCO3—、MnO4—、NH4+ D. 肯定有K+、Cl—
-
有一无色溶液,可能大量含有K+、A13+、Ba2+、NH4+、Cl-、SO42-、SO32-、HCO3-中的几种。为确定其成分,做如下实验:①取部分溶液,加入足量Na2O2固体,有气体产生,最后也有沉淀产生;②另取①中静置后少量上层清液,加入足量硝酸酸化的AgNO3溶液,但最后没有白色沉淀产生。下列推断正确的是
A.可能有A13+、NH4+、Cl- B.肯定有A13+、Ba2+、HCO3-
C.可能没有K+、HCO3-、NH4+ D.肯定没有A13+、SO32-、SO42-
-
二氧化锆(ZrO2)是最重要的氧离子固体电解质,用于制造燃料电池、氧气含量测定仪等。可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2;含有少量Fe2O3、Al2O3、SiO2杂质)通过如下工艺流程法制得。
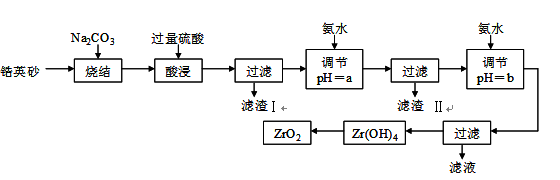
已知:①ZrO2具有两性,高温与纯碱共熔生成可溶于水的Na2ZrO3,与酸反应生成ZrO2+。②部分金属离子开始沉淀和完全沉淀的pH如下表:
| 金属离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀的pH | 1.9 | 3.3 | 6.2 |
| 沉淀完全的pH | 3.2 | 5.2 | 8.0 |
请回答下列问题:
⑴烧结时ZrSiO4发生反应的化学方程式为_______________________;
滤渣I的化学式为______________________________。
⑵调节pH=a 的目的是________________________________________;用氨水调节pH=b后发生反应的离子方程式为______________________________________________。
⑶以滤渣II为主要原料制取铁红,请简述实验方法________________________。
⑷工业上用铝热法冶炼锆,写出以ZrO2通过铝热法制取锆的化学方程式:
________________________________________________________。
⑸一种新型燃料电池用掺杂Y2O3的ZrO2晶体作电解质在熔融状态下传导O2-,一极通入空气,另一极通入甲烷,写出负极的电极反应式为___________________________。
-
二氧化锆(ZrO2)是最重要的氧离子固体电解质,用于制造燃料电池、氧气含量测定仪等。可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2;含有少量Fe2O3、Al2O3、SiO2杂质)通过如工艺流程法制得。
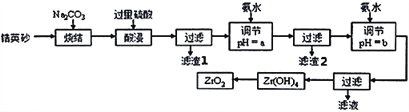
已知:①ZrO2具有两性,高温与纯碱共熔生成可溶于水的Na2ZrO3,与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表。
| 金属离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 |
| 沉淀完全时pH | 3.2 | 5.2 | 8.0 |
请回答下列问题:
(1)已知Zr元素的原子序数是40,请写出它在周期表中的位置:____________________________。
(2)烧结时ZrSiO4发生反应的化学方程式为__________________________;滤渣1的化学式为__________。
(3)调节pH=a时,a的范围应该是__________________;用氨水调节pH=b时,所发生反应的离子方程式为_______________________________________。
(4)本题的流程中,一共有三步过滤操作,北中最后一步过滤所得的Zr(OH)4沉淀需要洗涤,证明该沉淀已经洗涤干净的最佳操作方法是:______________________________________。
(5)工业上用铝热法冶炼锆,写出以ZrO2通过铝热法制取锆的化学方程式:________________。
(6)一种新型燃料电池用掺杂Y2O3的ZrO2晶体作电解质在熔融状态下传导O2-,一极通入空气,另一极通入乙烷,写出负极的电极反应式:________________________________。
-
粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液、 饱和K2CO3溶液 、NaOH溶液、 KOH溶液、 BaCl2溶液 、Ba(NO3)2溶液
(1)欲除去溶液中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的各种试剂,按滴加顺序依次为(填化学式);
(2)蒸发浓缩溶液Ⅱ得到的糊状物的化学成分最多的是(填化学式);
(3)用提纯过的NaCl固体来配制480 mL 0.4 mol·L-1NaCl溶液时,所用仪器除烧杯、药匙、玻璃棒、天平、胶头滴管外还有________(填仪器名称);需NaCl________g。
(4)电解饱和食盐水的装置如图所示:
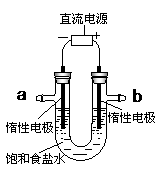
若收集到的H2为2 L,则同样条件下收集到的Cl2体积________(填“>”、“=”或“<”)2 L,其原因是:________(文字描述);若将此装置的b口密封住,则电解一段时间后,U型管中可以获得一种消毒液,写出获得此消毒液的一个总反应方程式:________。






