-
氯气在生产生活中有广泛的用途,制取氯气的途径有多种。完成下列填空:
(1)工业上用电解饱和食盐水制取氯气,氯气在电解池的______极产生;氯气与氢氧化钠反应得到消毒剂次氯酸钠,发生反应的化学方程式为________;向次氯酸钠溶液中加入少量稀盐酸,可以增强消毒效果,这是因为生成了_____(填物质名称)。
(2)实验室制取氯气的化学方程式为MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,该反应中,氯气是______(填“氧化”或“还原”)产物;若反应过程中转移了2 mol电子,则在标准状况下可以得到_______L氯气。
MnCl2+Cl2↑+2H2O,该反应中,氯气是______(填“氧化”或“还原”)产物;若反应过程中转移了2 mol电子,则在标准状况下可以得到_______L氯气。
(3)实验室常用排饱和食盐水的方法收集氯气,请用平衡移动原理解释用饱和食盐水而不用水的原因。___________
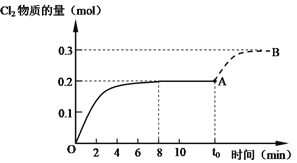
(4)有机化工中会利用反应4HCl(g)+O2(g) 2Cl2(g)+2H2O(g)+Q(Q>0)来产生氯气。向5 L的密闭容器中加入0.5 mol HCl与0.2 mol O2,在一定条件下发生反应,Cl2的物质的量与时间t的关系如图中OA段所示。0~8 min时Cl2的平均反应速率为_________________。t0时刻改变某一条件,Cl2的物质的量变化曲线如图中AB段所示,则t0时改变的条件一定是__________。
2Cl2(g)+2H2O(g)+Q(Q>0)来产生氯气。向5 L的密闭容器中加入0.5 mol HCl与0.2 mol O2,在一定条件下发生反应,Cl2的物质的量与时间t的关系如图中OA段所示。0~8 min时Cl2的平均反应速率为_________________。t0时刻改变某一条件,Cl2的物质的量变化曲线如图中AB段所示,则t0时改变的条件一定是__________。
a.降低温度 b.增大压强 c.加入HCl
-
氯气是工业生产中的重要原料,含氯消毒剂在生活中有着广泛的用途。
(1)工业生产通过电解饱和食盐水获取大量氯气,化学方程式为________。
(2)氯气可用于制取84消毒液(有效成分为NaClO),离子方程式为________。
(3)下列措施能增强84消毒液杀菌能力的是________。
A.加入适量醋酸 B.加入适量亚硫酸 C.加入少量NaOH粉末
(4)氯气与氢氧化钠溶液反应,若所得溶液恰好为中性,则溶液中离子浓度关系正确的是________。
A.c(Na+) + c(H+) = c(OH-) + c(Cl-)
B.c(Na+) = c(ClO-) + c(Cl-)
C.c(Na+) = 2c(ClO-) + c(HClO)
(5)84消毒液不能用于消毒钢铁(含Fe、C)制品,易发生电化学腐蚀,钢铁制品表面生成红褐色沉淀。正极反应为________。
-
工业上电解饱和食盐水可得到多种工业原料,其中氢气和氯气用途非常广泛.
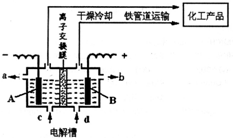
(1)如图所示是离子交换膜(允许钠离子通过,不允许氢氧根与氯离子通过)法电解饱和食盐水示意图.电解过程中,A极发生的是______(填“氧化”或“还原”)反应;B极的电极反应方程式为______.若将电极材料换为铁棒,则B极的电极反应为______.
(2)以上反应得到的H2和C12可直接化合制盐酸.有人设想利用原电池原理直接制备盐酸,同时获得电能.若这种设想可行,则通氢气的电极为______极;通氯气的电极反应式为______.
(3)工业制得的浓盐酸往往呈黄色,原因是输送氯气的铁管道被腐蚀所致.请写出有关反应的化学方程式______,这种腐蚀属于______.
(4)室温下,将1.000mo1•L-1盐酸滴入20.00mL1.000mo1•L-1氨水中,当溶液pH=7时,c(C1-)______c(NH4+)(填=、>、<);当滴入20.00mL盐酸时,溶液中各离子浓度由大到小的顺序为______.
-
世界上绝大部分卤素都存在于海洋。海水呈微碱性,海水晒盐可以得到粗盐和卤水,对粗盐和卤水进一步加工可以得到氯气、溴以及其他一些重要的化工产品。
完成下列填空:
(1)工业上用电解饱和食盐水的方法获取氯气。写出阴极的电极反应式_______________,该反应为________(选填“氧化”、“还原”)反应。若转移5mol电子,生成氯气______L(标准状况下)。
(2)工业上从卤水获取溴,涉及到“氧化”、“提取”等步骤。“氧化”时先在卤水中加入硫酸酸化,然后再通入氯气,硫酸酸化可以提高氯气的利用率,原因是________________。在“提取”过程中,用空气把溴吹出,然后用碳酸钠溶液吸收,这时溴转化为Br-和BrO3-,同时有CO2生成,写出反应的化学方程式________________________________。
(3)用上述方法制得的液溴常溶有少量氯气,除去氯气的方法是_____________。
(4)足量氯气与铁反应生成氯化铁,足量碘与铁反应生成碘化亚铁。运用原子结构和元素周期律简要说明导致产物中铁元素价态不同的原因__________________________________。
-
(12分)
钠是一种很活泼的金属,在工业上常用电解熔融NaCl的方法制得,其另一产物氯气的用途也十分广泛,工业上制取漂白粉就是其用途之一。
(1)请写出工业上用电解方法制取钠的化学方程式。
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是________。
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其它物质。
①提出合理假设。
假设1:该漂白粉未变质,只含________;
假设2:该漂白粉全部变质,只含________;
假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3。
② 设计实验方案,进行实验。请在答题卡上写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-,表格可以不填满。)
| 实验步骤 | 预期现象和结论 |
| ① | 取少量上述漂白粉于试管中,________ ________ | ________ |
| ② | | |
| ③ | | |
-
完成下列填空:某化学小组拟采用如下装置(夹持和加热仪器等已略去)来电解饱和食盐水,并用电解产生的 H2 还原 CuO 粉末来测定 Cu 的相对原子质量,同时验证氯气的氧化性。

完成下列填空:
(1) 写出甲装置中反应的化学方程式______________________________。
(2) 为完成上述实验,正确的连接顺序为 A 连______,B连_____(填写接口字母)。
(3)乙装置中 a 试剂可以是_______________。
(4) 测定 Cu 的相对原子质量。将w g CuO 置于硬质玻璃管中,按以下两个方案测得的数据计算 Cu 的相对原子质量
| 方案 1 | 方案 2 |
| U 型管+固体 | 硬质玻璃管+固体 |
| 反应前的总质量/g | a | c |
| 反应后的总质量/g | b | d |
你认为较佳方案是_____________,另一个方案得到的 Cu 的相对原子质量会_______(选填“偏低”、或“偏高”)
-
含氯消毒剂在生产生活中有着广泛的用途。完成下列填空:
(1)工业上将氯气溶于一定浓度的氢氧化钠溶于可制得“84消毒液”,反应的离子方程式为_________。
(2)“84消毒液”(主要成分是NaClO)不能和洁厕剂(主要成分是浓盐酸)混用。混用时反应的化学方程式是_______________________________;“84消毒液”不能对钢铁制品进行消毒,原因是____________。
(3)工业常用石灰乳和氯气反应制取漂粉精,其主要设备是氯化塔,将含有3%-6%水分的石灰乳从塔顶部喷洒而入,氯气从塔的最底层通入。这样加料的目的是__________;处理从氯化塔中逸出气体的方法是_____。
(4)二氧化氯(ClO2)是一种黄绿色易溶于水的气体。工业上常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为_________。
(5)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为___________________________。
-
钠是一种很活泼的金属,在工业上常用电解熔融NaCl的方法制得,其另一产物氯气的用途也十分广泛,工业上制取漂白粉就是其用途之一。
(1)请写出工业上用电解方法制取钠的化学方程式________。
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是________。
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其它物质。
①提出合理假设。
假设1:该漂白粉未变质,只含________;
假设2:该漂白粉全部变质,只含________;
假设3:该漂白粉部分变质,________。
② 设计实验方案,进行实验。请在答题卡上写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-,表格可以不填满。)
| 实验步骤 | 预期现象和结论 |
| ① | 取少量上述漂白粉于试管中,________ ________ | ________ |
| ② | | |
| ③ | | |
-
(16分)
钠是一种很活泼的金属,在工业上常用电解熔融NaCl的方法制得,其另一产物氯气的用途也十分广泛,工业上制取漂白粉就是其用途之一。
(1)请写出工业上用电解方法制取钠的化学方程式________。
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是________。
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其它物质。①提出合理假设。
假设1:该漂白粉未变质,只含________;
假设2:该漂白粉全部变质,只含________;
假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3。
② 设计实验方案,进行实验。请在答题卡上写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-,表格可以不填满。)
| 实验步骤 | 预期现象和结论 |
| ① | 取少量上述漂白粉于试管中,________ ________ | ________ |
| ② | | |
| ③ | | |
-
下列物质的制备,不符合工业生产实际的是( )
A.工业上用电解熔融氯化镁制备单质镁
B.工业上用电解饱和食盐水制备氯气
C.工业上用二氧化硅在高温下与焦炭反应制得高纯硅
D.工业上炼铁时,常用石灰石除去铁矿石中的二氧化硅
MnCl2+Cl2↑+2H2O,该反应中,氯气是______(填“氧化”或“还原”)产物;若反应过程中转移了2 mol电子,则在标准状况下可以得到_______L氯气。
2Cl2(g)+2H2O(g)+Q(Q>0)来产生氯气。向5 L的密闭容器中加入0.5 mol HCl与0.2 mol O2,在一定条件下发生反应,Cl2的物质的量与时间t的关系如图中OA段所示。0~8 min时Cl2的平均反应速率为_________________。t0时刻改变某一条件,Cl2的物质的量变化曲线如图中AB段所示,则t0时改变的条件一定是__________。


