-
某同学将燃着的红磷放入装有氧气的集气瓶中燃烧,一段时间后,红磷熄灭,他立刻将燃烧匙取出,但此时红磷又开始燃烧.解释这种现象的说法错误的是( )
A.红磷又接触到氧气
B.红磷的温度还高于它的着火点
C.瓶内的氧气不能耗尽红磷
D.燃烧时红磷转变成白磷,降低了着火点难度: 中等查看答案及解析
-
实验室使用大理石和盐酸反应制取的CO2是不纯净的,为证明该气体中含有多种物质,所用的试剂及使用顺序正确的是
( )
A.无水硫酸铜、硝酸银溶液、石灰水
B.浓硫酸、氢氧化钠溶液、石灰水
C.硝酸银溶液、石灰水、无水硫酸铜
D.氯化钙、石蕊试液、水难度: 中等查看答案及解析
-
用实际参加化学反应的离子符号来表示化学反应的式子叫离子方程式,在离子方程式中,反应前后的电荷是守恒的,原子个数也是守恒的.现有如下离子方程式:RO3n-+F2+2OH-=RO4-+2F-+H2O,由此可知在RO3n-中,元素R的化合价是( )
A.+4
B.+5
C.+6
D.+7难度: 中等查看答案及解析
-
现有100 gCuSO4和ZnSO4的混合溶液,向其中加入5.6 g铁粉,恰好完全反应后,过滤,则溶液的质量变化情况以及滤液中的金属离子判断正确的是( )
A.质量变大,Zn2+、Fe2+
B.质量变大,Cu2+、Zn2+
C.质量变小,Zn2+、Fe2+
D.质量变小,Cu2+、Fe2+难度: 中等查看答案及解析
-
可以用加热氯酸钾和二氧化锰混合物的方法在实验室制取氧气.下列是反应生成氧气和氯化钾的质量与反应时间的关系坐标图,其中合理的是( )
A.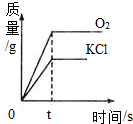
B.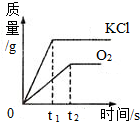
C.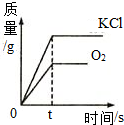
D.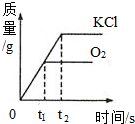
难度: 中等查看答案及解析
-
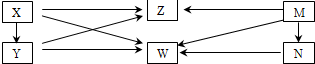
能实现下列物质间直接转化的元素是( )
单质→氧化物
酸或碱
盐.
A.硅
B.硫
C.铜
D.铁难度: 中等查看答案及解析