-
下列过程属于化学变化的是
A.苹果腐烂 B.湿衣晾干 C.石蜡熔化 D.辣椒剁碎
难度: 中等查看答案及解析
-
能供给呼吸的气体是
A.氧气 B.氮气 C.稀有气体 D.二氧化碳
难度: 简单查看答案及解析
-
决定元素种类的是
A.质子数 B.电子数 C.中子数 D.最外层电子数
难度: 中等查看答案及解析
-
下列物质中,属于氧化物的是
A.O2 B.H2O C.KMnO4 D.CaCO3
难度: 中等查看答案及解析
-
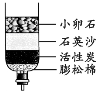
下列实验操作错误的是

难度: 中等查看答案及解析
-
下列食物中富含蛋白质的是
A.西瓜 B.鲫鱼 C.花生油 D.马铃薯
难度: 中等查看答案及解析
-
下列图标中,表示“禁止烟火”的是

难度: 简单查看答案及解析
-
下列物质在氧气中燃烧,产生大量白烟的是
A.木炭 B.红磷 C.蜡烛 D.甲烷
难度: 中等查看答案及解析
-
下列金属中,金属活动性最强的是
A.锌 B.铁 C.铜 D.银
难度: 中等查看答案及解析
-
一种氟原子的原子核内有9个质子和10个中子,该原子的核电荷数为
A.7 B.9 C.10 D.19
难度: 中等查看答案及解析
-
下列数据是一些食物的近似pH,其中呈碱性的是
pH
3.5~4.5
2.9~3.3
6.3~6.6
7.6~8.0
食物
A.葡萄汁
B.苹果汁
C.牛奶
D.鸡蛋清
难度: 中等查看答案及解析
-
下列方法能鉴别氧气和空气的是
A.闻气味 B.将集气瓶倒扣在水中
C.观察颜色 D.将燃着的木条伸入集气瓶中
难度: 中等查看答案及解析
-
下列物质放入水中,能形成溶液的是
A.面粉 B.牛奶 C.食盐 D.植物油
难度: 中等查看答案及解析
-
碘酸钙[Ca(IO3)2]可用于补碘剂,其中碘(I)元素的化合价为
A.+4 B.+5 C.+6 D.+7
难度: 中等查看答案及解析
-
尿素[CO(NH2)2]是一种化肥,它属于
A.磷肥 B.氮肥 C.钾肥 D.复合肥
难度: 简单查看答案及解析
-
用分子的相关知识解释生活中的现象,下列说法正确的是
A.冰融化成水,说明分子种类发生改变
B.分离液态空气制氧气说明分子可以再分
C.“酒香不怕巷子深”说明分子在不断运动
D.压瘪的乒乓球放入热水中重新鼓起是因为分子体积增大
难度: 中等查看答案及解析
-
下图为某化学反应的微观示意图,图中“
”表示氧原子,“
”表示氢原子。下列说法中错误的是

A.丙是O2
B.该反应属于分解反应
C.反应前后,分子、原子种类均不变
D.反应中,甲、乙、丙三种物质的分子个数比为2:2:1
难度: 中等查看答案及解析
-
a、b两种物质的溶解度曲线如下图所示。下列说法不正确的是

A.t1℃时,a、b溶解度相等
B.t2℃时,a、b饱和溶液中溶质的质量分数a>b
C.将t2℃时的a、b饱和溶液降温至t1℃,两种溶液一定都是饱和溶液
D.t2℃时,取等质量a、b的饱和溶液,分别蒸发等质量水后恢复至t2℃,析出溶质的质量a>b
难度: 中等查看答案及解析
-
下列图像能正确反映对应关系的是
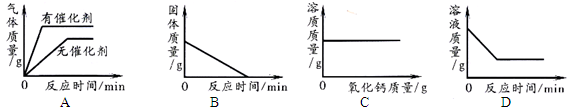
A.用一定量的双氧水制取氧气
B.加热一定量高锰酸钾固体产生氧气
C.向一定量的饱和石灰水中加入氧化钙
D.向一定量的硝酸银溶液中插入铜丝
难度: 中等查看答案及解析
-
通过下列实验操作和现象能得出相应结论的是
选项
实验操作
现象
结论
A
向收集满CO2的软塑料瓶中加入约1/3体积的水,旋紧瓶盖,振荡
塑料瓶变瘪
CO2能与水反应
B
点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯
烧杯内壁有无色液滴产生
被点燃的气体是CH4
C
50℃时,将34gKCl固体加入100g蒸馏水中
完全溶解
50℃时,KCl的溶解度为34g
D
将白磷浸没在热水中,再向热水中的白磷通氧气
通氧气前白磷不燃烧,通氧气后白磷
燃烧
氧气是可燃物燃烧的条件之一
难度: 困难查看答案及解析