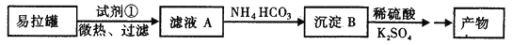-
材料与人类生活密切相关,下列物品中最难降解的是
A. 真丝围巾 B. 宣纸 C. PVC塑料卡片 D. 淀粉做的餐具
难度: 简单查看答案及解析
-
下列实验操作所得的现象及结论均正确的是
选项
实验操作
现象及结论
A
向酸性KMnO4溶液中通入乙烯
溶液紫红色褪去,说明乙烯具有还原性
B
向FeI2溶液中滴入少量氯水
溶液变黄,说明还原性:I−>Fe2+
C
将AlCl3溶液加热蒸干
得到白色固体,成分为纯净的AlCl3
D
将少量Na2SO3样品溶于水,滴入盐酸酸化的Ba(NO3)2溶液
有白色沉淀产生,说明Na2SO3已变质
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
化学与生产、实验密切相关。下列有关物质的性质与用途具有对应关系的是
A.Al2O3熔点高,可用作耐高温材料
B.FeCl3溶液呈酸性,可用于腐蚀电路板上的Cu
C.石墨具有导电性,可用于制铅笔芯
D.浓硫酸具有强氧化性,可用于干燥CO2
难度: 中等查看答案及解析
-
化学与生活、社会密切相关,下列说法正确的是( )
A.为了防止一些零食的氧化变质,厂家常常在包装袋内装有硅胶或生石灰
B.绚丽缤纷的烟花中添加了含钾、钠、铁、铜等金属元素的化合物
C.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
D.有人称“一带一路”是“现代丝绸之路”,丝绸的主要成分是纤维素,属天然高分子化合物
难度: 中等查看答案及解析
-
下列物质溶于水时会破坏水的电离平衡,且属于电解质的是
A. 氯气 B. 二氧化碳 C. 氯化钾 D. 醋酸钠
难度: 中等查看答案及解析
-
3-己烯醇乳酸酯(
)常被用于具有花香的日化香精中和具有果香的食品香精中,并为整个配方带来柔和青果香的效果,下列对其说法不正确的是( )
A.该物质难溶于水
B.该物质可以发生酯化反应和水解反应
C.1 mol该物质最多可与1 mol Na发生反应
D.该物质既能使酸性高锰酸钾溶液褪色,也能使溴的四氯化碳溶液褪色 ,且褪色原理相同
难度: 中等查看答案及解析
-
如图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )
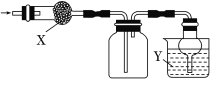
选项
X
收集气体
Y
A
碱石灰
HCl
水
B
碱石灰
NH3
水
C
氯化钙
SO2
氢氧化钠
D
氯化钙
NO
氢氧化钠
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
NA代表阿伏加德罗常数的值。下列叙述正确的是( )
A.常温常压下,2.24 LSO2中所含氧原子数为0.2NA
B.将1mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA
C.1mol NO2与足量H2O反应,转移的电子数为NA
D.0.1mol熔融的NaHSO4中阳离子数目为0.1NA
难度: 中等查看答案及解析
-
短周期元素A、B、C、D的原子序数依次增大。A原子的最外层电子数是内层电子数的2倍,元素B在同周期的主族元素中原子半径最大,元素C的合金是日常生活中常用的金属材料,元素D位于第ⅥA族。下列说法正确的是
A.原子半径:D>B>C>A
B.元素A、B的氧化物所含化学键的类型完全相同
C.元素B和C的最高价氧化物对应水化物的碱性:B<C
D.元素B、C、D的最高价氧化物对应的水化物能相互反应
难度: 中等查看答案及解析
-
已建立化学平衡的某可逆反应,当改变条件使平衡向正反应方向移动,正确的是
A.生成物的百分含量一定增加 B.正反应速率大于逆反应速率
C.反应物的转化率一定增大 D.反应物浓度一定降低
难度: 简单查看答案及解析
-
实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:

下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
难度: 中等查看答案及解析
-
分别用等量的铁与足量的稀硫酸和足量的CuO制备单质铜,有人设计了以下两种方案:①Fe
H2
Cu,②CuO
CuSO4
Cu,对制备得到Cu的量,下列判断正确的是( )
A.一样多
B.②多
C.①多
D.无法判断
难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中可能大量共存的是
A.澄清透明的溶液中: Fe3+、Mg2+、SCN-、Cl-
B.由水电离产生的c(H+)= 10-13mol/L 的溶液: K+、Na+、CH3COO-、AlO2-
C.c(Fe2+)= 1mol/L的溶液中: H+、NH4+、NO3-、SO42-
D.pH= 1的溶液中: Ba2+、Mg2+、HCO3-、SO42-
难度: 中等查看答案及解析
-
25℃时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的HA溶液,溶液的pH与所加NaOH溶液体积(V)的关系如图所示。下列说法不正确的是
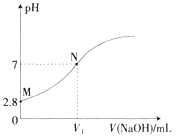
A.V1<20
B.Ka(HA)的数量级为10-5
C.M点溶液加少量水稀释,
增大
D.N点后,随着NaOH溶液的加入,溶液中水的电离程度逐渐增大
难度: 中等查看答案及解析
-
下列说法正确的是
A.甲基环已烷一氯代物有4 种
B.乙二醇与丙三醇互为同系物
C.蛋白质是仅由碳、氢、氧元素组成的物质
D.苯的邻二元取代物只有一种,可以证明苯分子中没有单、双键交替结构
难度: 中等查看答案及解析
-
我国最近在太阳能光电催化-化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是
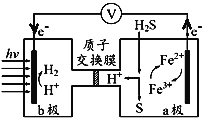
A.该装置工作时,H+由b极区流向a极区
B.该制氢工艺中光能最终转化为化学能
C.a极上发生的电极反应为Fe3++e-=Fe2+
D.a极区需不断补充含Fe3+和Fe2+的溶液
难度: 中等查看答案及解析