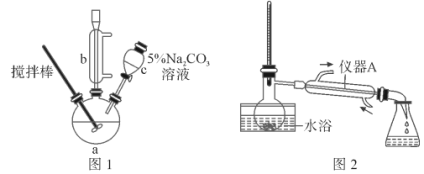
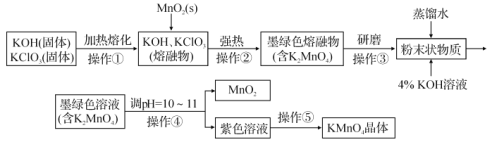
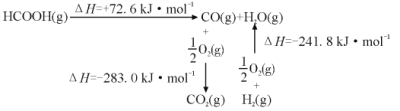
-
化学与生产、生活密切相关,下列有关说法正确的是( )
A.“玉兔号”月球车帆板太阳能电池的材料是氮化硅或二氧化硅
B.硅胶、CaO、P2O5都可用作食品干燥剂
C.我国积极倡导“低碳经济”,将煤液化就是一种“低碳”方式
D.可利用新制Cu(OH)2悬浊液检验患者尿液中是否含有葡萄糖
难度: 简单查看答案及解析
-
下列实验“操作和现象”与“结论”对应且正确的是( )
操作和现象
结论
A
向盛有浓硫酸的试管中加入铜片,铜片很快开始溶解,并放出刺激性气味的气体
浓硫酸具有强氧化性
B
向两支盛有KI3的溶液的试管中,分别滴加淀粉溶液和硝酸银溶液,前者溶液变蓝,后者有黄色沉淀
KI3溶液中存在平衡:I
⇌I2+I-
C
向一定量的硝酸银溶液中先滴加KCl溶液,再滴加KI溶液,先出现白色沉淀,后出现黄色沉淀
Ksp(AgCl)>Ksp(AgI)
D
室温下,用pH试纸分别测定浓度为0.1mol/LNaClO溶液和0.1mol/LCH3COONa溶液的pH
比较HClO和CH3COOH的酸性强弱
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
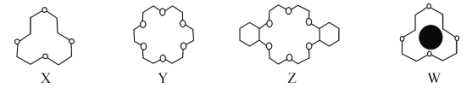
化合物A是一种危险化学制品,具有腐蚀性、可自燃性。主要用于医药工业,在有机合成中用作催化剂等。其结构如图所示,其中W、X、Y、Z是处于三个不同短周期且原子序数依次递增的常见元素,X、Y核外电子层数相同,Y核外最外层电子数是X内层电子数的3倍。下列叙述正确的是( )
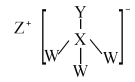
A.原子半径:Y>X>Z>W
B.简单气态氢化物的稳定性:X>Y
C.X与W形成的常见化合物有两种
D.W和Z形成的化合物为离子化合物
难度: 中等查看答案及解析
-
某酯的相对分子质量不大于160,可表示为CnH2nO2(n为整数)。在酸性条件下能水解生成两种相对分子质量相等的酸和醇,且该醇最终可被氧化为羧酸,不考虑立体异构,则满足该条件的酯有( )
A.12种 B.14种 C.23种 D.28种
难度: 中等查看答案及解析
-
铼(Re)是种银白色的重金属,是地球地壳中最稀有的元素之一,它广泛应用于航空航天领域。在工业上,高温灼烧含ReS2的矿粉,可以制备Re2O7。另一种途径是从炼铜的废液中提取铼,其简易工艺流程如图(部分副产物省略,铼在废液中以ReO4-形式存在)。下列说法错误的是( )

A.在“反萃取”中,加入氨水、水的目的是萃取有机层中的ReO4-
B.在NH4ReO4制备Re2O7的过程中,产生的副产物可回收利用
C.实验室在H2还原Re2O7的过程中,一共消耗7 mol H2,则可制得2 mol Re
D.以含ReS2的矿石原料生产48.4 t Re2O7,理论上转移电子3.0×106 mol
难度: 中等查看答案及解析
-
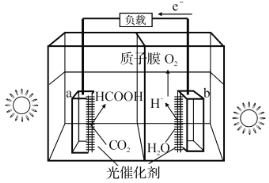
制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题。一定条件下,如图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其他有机物生成)。电流效率=(生成目标产物消耗的电子数/转移的电子总数)×100%,则下列说法错误的是( )
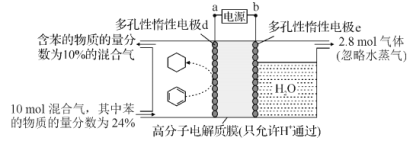
A.电子移动方向为:a→d;e→b
B.d电极反应式为C6H6+6H++6e-=C6H12
C.该储氢装置的电流效率明显小于100%,其原因可能是除目标产物外,还有H2生成
D.由图中数据可知,此装置的电流效率约为32.1%
难度: 中等查看答案及解析
-
常温时,浓度均为1mol·L-1的CH3NH2和NH2OH两种碱溶液,起始时的体积都为10mL。分别向两溶液中加水进行稀释,所得曲线如图所示(V表示溶液的体积),pOH=-lg[c(OH-)]。下列说法正确的是( )

A.当两溶液均稀释至lg
=5时,溶液中水的电离程度:NH2OH<CH3NH2
B.常温下,用盐酸滴定NH2OH时,可用酚酞作指示剂
C.CH3NH3Cl溶液中存在关系:2c(H+)+c(CH3NH)=c(CH3NH2)+2c(OH-)+c(Cl-)
D.等浓度的CH3NH3Cl和NH3OHCl的混合溶液中离子浓度大小关系为:c(NH3OH+)>c(CH3NH+)
难度: 中等查看答案及解析