-
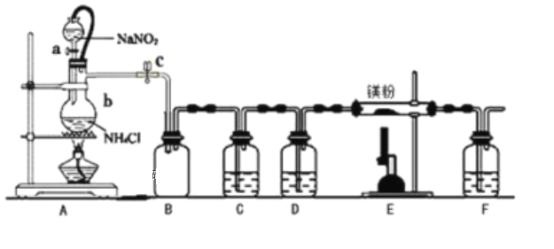
向铝粉中添加少量NH4C1固体并充分混合,将其加热到1000℃时可与N2反应制备A1N,下列说法正确的是
A. A1N是一种金属材料
B. A1N与足量氢氧化钠溶液共热时生成氢氧化铝和氨气
C. 少量NH4C1能够破坏A1表面的Al2O3薄膜
D. A1N与足量盐酸反应的离子方程式为AlN+3H+=Al3++NH3↑
-
向含有c(FeCl3)=0.2mol·L−1、c(FeCl2)=0.1mol·L−1的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其中分散质粒子是直径约为9.3nm的金属氧化物,下列有关说法中正确的是
A. 该分散系的分散质为Fe2O3
B. 可用过滤的方法将黑色金属氧化物与Na+分离开
C. 向沸水中逐滴滴加0.1mol·L−1 FeCl3溶液也可得到Fe(OH)3胶体
D. 加入NaOH时发生的反应可能为Fe2++2Fe3++8OH-===Fe3O4+4H2O
-
在一些高档茶叶、点心等食品的包装盒中有一个小袋,将小袋打开,可看到灰黑色粉末,其中有些已变成棕褐色。将灰黑色粉末溶于盐酸,取上层清液,滴入几滴氯水,再滴入KSCN溶液,马上出现血红色。以下结论不正确的是
A.该灰黑色粉末作抗氧化剂 B.该灰黑色粉末不可食用
C.小袋中原来装有铁粉 D.小袋中原来装有Fe2O3
-
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为
A. 9.0L B. 13.5L C. 15.7L D. 16.8L
-
LiAlH4( )、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125 ℃分解为LiH、H2和Al。下列说法不正确的是( )
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125 ℃分解为LiH、H2和Al。下列说法不正确的是( )
A.LiH与D2O反应,所得氢气的摩尔质量为4 g/mol
B.1 mol LiAlH4在125 ℃完全分解,转移3 mol电子
C.LiAlH4溶于适量水得到无色溶液,化学方程式可表示为:LiAlH4+2H2O═LiAlO2+4H2↑
D.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
-
下列解释事实的方程式不正确的是
A. 焊接铁轨:2Fe+Al2O3 2Al+Fe2O3
2Al+Fe2O3
B. 人工固氮:N2+3H2 2NH3
2NH3
C. 用纯碱除油污:CO32-+H2O HCO3-+OH-
HCO3-+OH-
D. 用湿润的淀粉KI试纸检验Cl2:Cl2+2I-=2Cl-+I2
-
中国传统文化对人类文明贡献巨大。下列两篇古代文献中都涉及到了KNO3。文献①:《开宝本草》记载:(KNO3)所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”,文献②《本草纲目》“火药乃焰硝(KNO3)、硫黄、山木炭所合,以为烽燧餇诸药者。”下列对其解释不合理的是
A.文献①中提取KNO3利用了溶解、蒸发结晶的实验过程
B.用文献①中方法制取KNO3是因为KNO3的溶解度受温度影响不大
C.文献②中火药的使用体现了硝酸钾的氧化性
D.文献②中使用火药的产物会污染环境
-
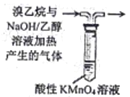
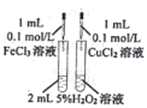
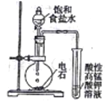
下列实验方案,能达到相应实验目的的是
| 实验目的 | A.探究铁钉发生析氢腐蚀 | B.验证溴乙烷发生消去反应 | C.对比Fe3+与Cu2+的氧化能力强弱 | D.探究乙炔的性质 |
| 实验方案 | 
| 
| 
| 
|
A.A B.B C.C D.D
-
建构数学模型来研究化学问题,既直观又简洁,下列建构的数轴模型正确的是( )
A.钠在氧气中燃烧,钠的氧化产物: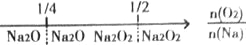
B.铁在Cl2中燃烧,铁的氧化产物: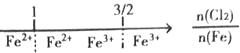
C.A1Cl3溶液中滴加NaOH溶液后体系中铝元素的存在形式: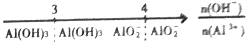
D.FeI2溶液中通入Cl2,铁元素存在形式:
-
向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如右图所示。下列结果不正确的是( )
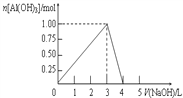
A.反应过程中,沉淀最多时的质量为78g
B.反应过程中,Al3+离子有1/3转化为Al(OH) 3沉淀,则加入的NaOH溶液的体积可能为3.5L
C.AlCl3溶液的浓度为2.0mol/L
D.当V(NaOH)=4.0 L时,得到的溶液中Na+、Cl-浓度一定不相等
-
已知HCO3-+AlO2-+H2O==CO32-+Al(OH)3↓。将足量的KHCO3溶液不断滴入含等物质的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与滴入的KHCO3溶液体积的关系可表示为
A.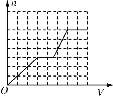 B.
B. C.
C.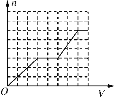 D.
D.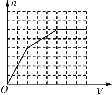
-
工业上曾经通过反应“3Fe+4NaOH Fe3O4+2H2↑4Na↑”生产金属钠,己知铁的熔点1535℃、沸点3000℃。下列有关说法正确的是
Fe3O4+2H2↑4Na↑”生产金属钠,己知铁的熔点1535℃、沸点3000℃。下列有关说法正确的是
A.增大铁的量可以使反应速率加快
B.将生成的气体在空气中冷却可获得钠
C.每生成1molH2,转移的电子数约为4×6.02×1023
D.该反应条件下铁的金属性比钠强
-
利用如图所示装置进行下列实验,能得出相应实验结论的是

| 选项 | ① | ② | ③ | 实验结论 |
| A | 浓氨水 | NaOH | 酚酞试液 | 碱性:NaOH>NH3·H2O |
| B | 浓硫酸 | 蔗糖 | 品红溶液 | 浓硫酸具有脱水性、氧化性 |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐反应均可生成白色沉淀 |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D
-
化学与生活密切相关,下列有关说法错误的是
A.新能源汽车的推广与使用,有助于减少光化学烟雾的产生
B.普通玻璃是由纯碱、石灰石和石英制得的
C.高纯度的SiO2是制备光导纤维、太阳能电池板的主要材料
D.海带中碘元素确定的实验主要步骤骤是:前期处理-灼烧-溶解-氧化-淀粉溶液检验
-
把少量废铁屑溶于过量稀硫酸中,过滤,除去杂质,在滤液中加入过量氯水,再加入过量的氨水,有沉淀生成。过滤,加热沉淀物至质量不再发生变化,得到固体残渣。上述沉淀和残渣分别为
A.Fe(OH)2 ;Fe2O3 B.Fe(OH)2;FeO
C.Fe(OH)2、Fe(OH)3;Fe2O3 D.Fe(OH)3;Fe2O3
-
某溶液中可能含有K+、Na+、Fe3+、Fe2+、SO42﹣、CO32﹣、I﹣、Cl﹣中的一种或多种,进行如图所示的实验,下列说法正确的是( )
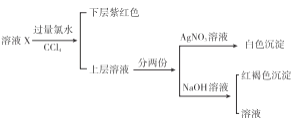
A.溶液X中有Fe3+、SO42﹣
B.溶液X中有Fe2+、I﹣可能有SO42﹣、Cl﹣
C.溶液X中有I﹣、Cl﹣,无CO32﹣
D.溶液X中有I﹣,Fe2+和Fe3+两种离子中至少有一种
-
X、Y、Z、W 为原子序数依次增大的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W形成的最高价氧化物分别为甲、乙、丙。x、y2、z、w分别为X、Y、Z、W的单质,丁是化合物。其转化关系如图所示,下列判断错误的是

A.反应①、②、③都属于氧化还原反应
B.X、Y、Z、W四种元素中,Y的原子半径最小
C.Na 着火时,可用甲扑灭
D.一定条件下,x与甲反应生成丁
-
N2O(笑气)、CHCl3(氯仿)都曾在医学上被用作麻醉剂。下列说法正确的是( )
A.N2O、CHCl3都易溶于水 B.N2O、CHCl3都属于电解质
C.N2O只有氧化性没有还原性 D.N2O、CHCl3都是共价化合物
-
在密闭容器中将2molNaHCO3(s)和一定量Na2O2混合,在加热条件下让其充分反应,150℃下所得气体仅含2种组分,反应后固体的物质的量(n) 的取值范围是
A. n≥1 B. 1 C. 2≤n<4 D. n≥4
-
下列实验装置设计正确、且能达到目的的是
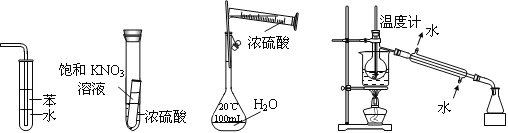
Ⅰ Ⅱ Ⅲ Ⅳ
A.实验I:可用于吸收氨气,并能防止倒吸
B.实验Ⅱ:静置一段时间,小试管内有晶体析出
C.实验III:配制一定物质的量浓度的稀硫酸
D.实验Ⅳ:海水的淡化
-
设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,4.48 L CH3Cl中所含原子数目为NA
B.所含共价键数均为0.4NA的白磷(P4)和甲烷的物质的量相等
C.将2 g H2与足量的N2混合,充分反应后转移的电子数为2NA
D.电解精炼铜,当电路中通过的电子数为0.1NA时,阳极质量减少3.2 g
-
“水飞”是传统中医中将药材与适量水共研细,取极细药材粉末的方法。《医学人门》中记载提纯铜绿的方法:“水洗净,细研水飞,去石澄清,慢火熬干。”文中涉及的操作方法是
A.洗涤、溶解、过滤、灼烧 B.洗涤、溶解、倾倒、蒸发
C.洗涤、萃取、倾倒、蒸馏 D.洗涤、萃取、过滤、蒸发
-
从某含Br—废水中提取Br2的过程包括:过滤、氧化、萃取(需选择合适萃取剂)及蒸馏等步骤。已知:
| 物质 | Br2 | CCl4 | 正十二烷 |
| 密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
| 沸点/℃ | 58.76 | 76.8 | 215~217 |
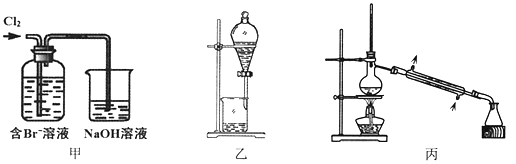
下列说法不正确的是
A.甲装置中Br—发生的反应为:2Br-+ Cl2 = Br2 + 2Cl-
B.甲装置中NaOH溶液每吸收0.1mol Cl2,转移0.1mol e—
C.用乙装置进行萃取,溶解Br2的有机层在下层
D.用丙装置进行蒸馏,先收集到的是Br2
-
“神舟十号”的运载火箭所用燃料是偏二甲肼(C2H8N2 )( 其中N 的化合价为-3 )和四氧化二氮(N2O4)。在火箭升空过程中,燃料发生反应: C2H8N2 +2N2O4→2CO2+3N2+4H2O 提供能量。下列有关叙述正确的是
A.该燃料无毒,在燃烧过程中不会造成任何环境污染
B.每有0.6molN2生成,转移电子数目为2.4NA
C.该反应中N2O4是氧化剂,偏二甲肼是还原剂
D.N2既是氧化产物又是还原产物,CO2既不是氧化产物也不是还原产物
 2NH3
2NH3



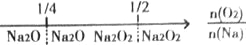
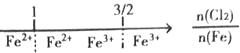
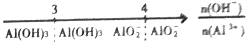


 B.
B. C.
C. D.
D.





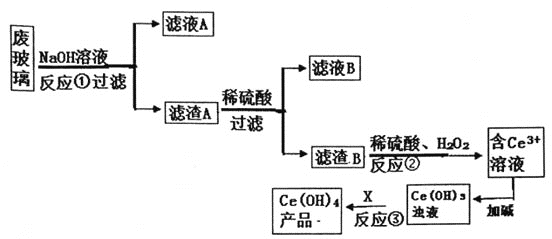

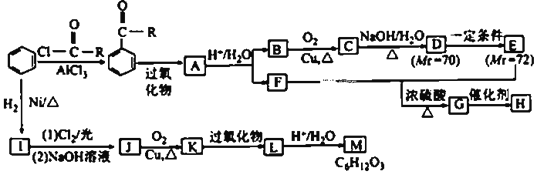
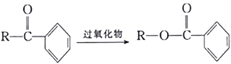 (R为烃基);
(R为烃基);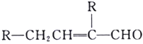 。
。