-
下列有关描述中正确的是
A.久置的氯水与新制的氯水,都能使有色布条褪色
B.钠在空气中燃烧,发出淡蓝色的火焰,生成淡黄色固体
C.硅能导电,可用作光导纤维
D.玻璃花瓶和餐桌上的瓷盘都是硅酸盐制品
难度: 中等查看答案及解析
-
下列实验方案设计中,可行的是
A.加稀硝酸后过滤,除去混在铜粉中的少量镁粉和铝粉
B.利用丁达尔效应鉴别Fe(OH)3胶体与FeCl3溶液
C.用溶解、过滤的方法分离CaCl2和NaCl固体混合物
D.用澄清石灰水试液鉴别SO2和CO2两种气体
难度: 中等查看答案及解析
-
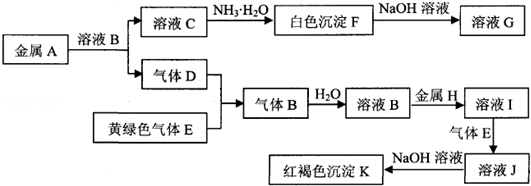
对实验I~IV的实验操作现象判断正确的是
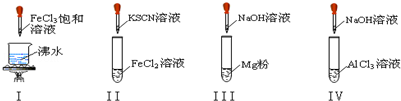
A.实验Ⅰ:产生红褐色沉淀
B.实验Ⅱ:溶液颜色变红
C.实验Ⅲ:放出大量气体
D.实验Ⅳ:先出现白色沉淀,后溶解
难度: 中等查看答案及解析
-
下列离子反应方程式正确的是
A.小苏打溶液与盐酸反应:CO32﹣+2H+=CO2↑+H2O
B.氯化铝溶液中加入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+
C.钠与水反应:Na+H2O=Na++OH﹣+H2↑
D.Fe溶于稀硫酸:Fe+3H+=Fe3++H2↑
难度: 中等查看答案及解析
-
某溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是
A.NH4+、Fe2+、NO3﹣、SO42﹣
B.Na+、K+、Cl﹣、SO42﹣
C.Mg2+、H+、Cl﹣、NO3﹣
D.K+、Ca2+、HCO3﹣、Cl﹣
难度: 中等查看答案及解析
-
在常温下,下列溶液不能溶解铁的是
A.稀硫酸 B.FeCl3溶液 C.CuCl2溶液 D.浓硫酸
难度: 简单查看答案及解析
-
有下列三个反应:
①Cl2+FeI2═FeCl2+I2
②2Fe2++Br2═2Fe3++2Br﹣
③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O下列说法正确的是
A.①②③中的氧化产物分别是I2、Fe3+、CoCl2
B.根据以上方程式可以得到氧化性Cl2>Fe3+>Co2O3
C.可以推理得到Cl2+FeBr2═FeCl2+Br2
D.在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化
难度: 困难查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,22.4L H2 与O2的混合气体所含原子数为2NA
B.标准状况下,18g H2O的体积是22.4L
C.NA个SO2的体积是22.4L
D.在常温、常压下,11.2L N2含有的分子数为0.5NA
难度: 中等查看答案及解析
-
下列关于钠的化合物的说法正确的是
A.等物质的量NaHCO3、Na2CO3分别与同浓度盐酸完全反应,消耗的盐酸体积Na2CO3是NaHCO3的二倍
B.Na2O2和Na2O均可以和盐酸反应生成相应的盐,都属于碱性氧化物
C.将澄清石灰水分别加入NaHCO3和Na2CO3两种盐溶液中,只有Na2CO3溶液产生沉淀
D.Na2O2和Na2O中Na2O更稳当,Na2O2在一定条件下可以转化为Na2O
难度: 困难查看答案及解析
-
用1L1.0mol/LNaOH溶液吸收0.8molCO2,所得溶液中的CO32﹣和HCO3﹣的物质的量浓度之比约是
A.2:3 B.1:2 C.1:3 D.3:2
难度: 中等查看答案及解析
-
向含有1mol KAl(SO4)2的溶液中加入适量的Ba(OH)2溶液,使SO42﹣恰好转化为沉淀,此时Al(OH)3物质的量是
A.0mol B.0.67mol C.1mol D.1.33 mol
难度: 中等查看答案及解析
-
甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,有白色沉淀生成,继续滴加则沉淀消失;丁溶液滴入甲溶液中,无明显现象,据此可推断丙物质是
A.Al2(SO4)3 B.NaOH C.BaCl2 D.FeSO4
难度: 中等查看答案及解析
-
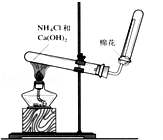
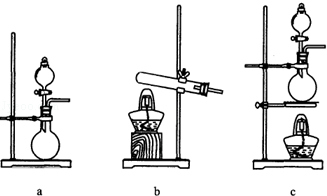
下列有关氢氧化亚铁及其制备方法的叙述中,不正确的是

A.氢氧化亚铁易被空气氧化
B.氢氧化亚铁为灰绿色絮状沉淀
C.可利用如图所示装置,制备氢氧化亚铁
D.实验制备中,氢氧化钠溶液应预先煮沸
难度: 中等查看答案及解析
-
关于SiO2的叙述中,错误的是
A.SiO2和CO2都是酸性氧化物,都能与强碱溶浓反应
B.SiO2和CO2都能溶于水且与水反应生成相应的酸
C.工艺师利用HF溶液刻蚀石英制作艺术品
D.除去SiO2中混有的CaCO3可加入适量的稀盐酸,然后过滤
难度: 中等查看答案及解析
-
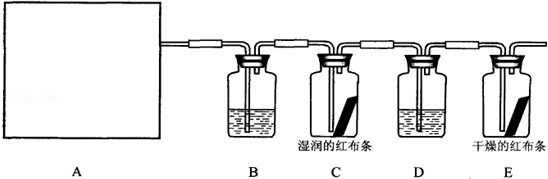
下列关于氯气的实验装置能达到实验目的或实验效果的是

①可用于氯气的收集
②可用于除去氯气中少量的氯化氢气体
③可证明氯气具有漂白性
④可用于实验室氯气的尾气吸收.
A.①② B.①③ C.②③ D.①④
难度: 中等查看答案及解析
-
稀硫酸中插一块铜片,加入下列物质后,可使铜片迅速发生反应的是
A.稀盐酸 B.硫酸钠晶体 C.硝酸钾晶体 D.氯化钠晶体
难度: 中等查看答案及解析
-
下列表述正确的是
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑥二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6.
A.①③④ B.①② C.① D.①②⑤⑥
难度: 中等查看答案及解析
-
将2.56g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12L(标准状况),则反应中消耗HNO3的物质的量为
A.0.05 mol B.1 mol C.1.05 mol D.0.13 mol
难度: 困难查看答案及解析
-
向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液.下列图象中,能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)
A.
 B.
B. C.
C. D.
D.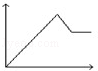
难度: 中等查看答案及解析
-
下列物质的分类合理的是
碱
酸
盐
酸性氧化物
A
纯碱
盐酸
烧碱
二氧化硫
B
烧碱
硫酸
食盐
一氧化碳
C
苛性钠
醋酸
石灰石
水
D
KOH
碳酸
纯碱
三氧化硫
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
在托盘天平右盘上放一个盛有100mL3mol/L NaOH溶液的烧杯,左盘上放一个盛有100mL3mol/L盐酸的烧杯,调节天平至平衡,然后在两烧杯中各加入等质量的铝片(铝片均不剩余),反应完全后,则天平可能出现的情况是
A.左盘下沉 B.右盘下沉 C.仍保持平衡 D.无法判断
难度: 困难查看答案及解析