-
下列属于含有共价键的化合物的是
A. N2 B. CaCl2 C. KF D. NaOH
难度: 简单查看答案及解析
-
下列鉴别或检验有关物质的方法能达到目的的是
A. 用丁达尔现象区分氢氧化铁胶体与氯化铜溶液
B. 用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液
C. 将某气体通入品红溶液中,溶液褪,说明该气体一定是SO2
D. 用淀粉溶液检验食盐溶液中是否存在IO3-
难度: 中等查看答案及解析
-
美国犹他州立大学(USU)和俄罗斯南联邦大学的科学家,利用计算机模型设计出比水还轻的超轻晶体铝,这种超轻晶体铝属于
A. 有机物 B. 单质 C. 化合物 D. 氧化物
难度: 简单查看答案及解析
-
纪录片《穹顶之下》再次引起人们对大气环境的强烈关注.下列燃料中最环保的是( )
A.石油 B.煤 C.氢气 D.天然气
难度: 简单查看答案及解析
-
下列变化属于物理变化的是
A. 用石油分馏炼制汽油 B. 用煤干馏制备焦炭
C. 用铝土矿冶炼铝 D. 用海带提取碘单质
难度: 简单查看答案及解析
-
最近有科学家研究发现器82212Pb 具有杀死癌细胞的功效。下列关于82212Pb的说法正确的是
A. 质子数是212 B. 电子数是294 C. 中子数是130 D. 质量数是82
难度: 简单查看答案及解析
-
在野外焊接钢轨过程中存在的反应:Fe2O3+2Al
Al 2O3+2Fe。该反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
难度: 中等查看答案及解析
-
下列化学用语正确的是
A. 乙醇分子的结构式:
B. 氯原子的结构示意图:

C. 过氧化氢分子的电子式:
D. 硫酸钠的电离方程式:Na2SO4=Na2++ SO42-
难度: 中等查看答案及解析
-
下列气体可用下图所示装置收集的是 ( )
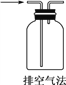
A. CO2 B. H2 C. NO D. N2
难度: 中等查看答案及解析
-
一定条件下将1 mol N2和3 mol H2置于密闭容器中发生反应N2+3H2
 2NH3(正反应是放热反应)。下列关于该反应的说法正确的是
2NH3(正反应是放热反应)。下列关于该反应的说法正确的是A. 降低温度可以加快反应速率
B. 达到化学反应限度时,生成2mol NH3
C. 向容器中再加入N2可以加快反应速率
D. 1mol N2 和3mol H2的总能量低于2mol NH3的总能量
难度: 中等查看答案及解析
-
下列食用品的有效成分正确的是
A.
 C6H12O6 B.
C6H12O6 B.  Na2CO3
Na2CO3C.
 CH3COOH D.
CH3COOH D.  Al(OH)3
Al(OH)3难度: 简单查看答案及解析
-
某无色溶液中存在大量的NH4+、H+、Clˉ,该溶液中还可能大量存在的离子是
A. CO32ˉ B. OHˉ C. Cu2+ D. Al3+
难度: 中等查看答案及解析
-
下列关于浓硝酸的说法正确的是
A. 难挥发 B. 有吸水性
C. 常温下能使铁片钝化 D. 保存在无色试剂瓶中
难度: 中等查看答案及解析
-
下列关于NO2的制取、净化、收集及尾气处理的装置和原理不能达到实验目的的是
A.
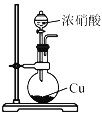 制取NO2 B.
制取NO2 B. 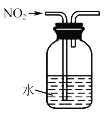 净化NO2
净化NO2C.
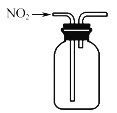 收集NO2 D.
收集NO2 D. 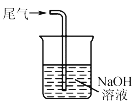 尾气处理
尾气处理难度: 中等查看答案及解析
-
乙醇和乙酸是生活中两种常见的有机物。下列说法正确的是
A.乙醇、乙酸互为同分异构体
B.乙醇、乙酸都能与钠反应
C.乙醇、乙酸都能与NaOH溶液反应
D.乙醇、乙酸都能使紫色石蕊试液变红色
难度: 中等查看答案及解析
-
二氧化氯(ClO2)是一种高效消毒剂,下列反应可制得ClO2:
2NaClO3 +Na2SO3 +H2SO4 = 2ClO2 +2Na2SO4 +H2O
对于该反应,下列说法正确的是( )
A.H2SO4发生氧化反应 B.NaClO3是还原剂
C.Na2SO4 是还原产物 D.当转移1mol电子时,该反应生成1 mol ClO2
难度: 中等查看答案及解析
-
下列物质能与SiO2反应的是
A. 氢氟酸 B. 盐酸 C. 硫酸 D. 水
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A. 铁和盐酸反应:Fe+2H+ =Fe3++H2↑
B. 氢氧化钡溶液和稀硫酸反应:Ba2++SO42ˉ=BaSO4↓
C. 氢氧化镁和盐酸反应:H++OHˉ=H2O
D. 氯化铝溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
难度: 中等查看答案及解析
-
下列化学反应属于吸热反应的是
A. 氢氧化钠与稀盐酸反应 B. 氢氧化钙与氯化铵晶体混合
C. 镁与稀盐酸反应 D. 生石灰溶于水
难度: 简单查看答案及解析
-
某原电池的结构如图所示,下列有关该原电池的说法正确的是
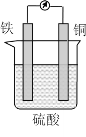
A. 该电池工作时电能转变为化学能 B. 铜片的质量增加
C. H+向铁片移动 D. 铁片上发生的反应是Fe-2e-=Fe2+
难度: 中等查看答案及解析
-
下列有机反应不属于取代反应的是
A.C2H5OH+CH3COOH
CH3COOC2H5+H2O
B.H﹣C≡C﹣H+HCl
H2C=CHCl
C.
D.
难度: 中等查看答案及解析
-
短周期主族元素W、R、X、Y、Z的原子序数依次增大,W的原子半径是周期表中所有元素中最小的,R是地壳中含量最多的元素,X与W同主族,Y的最外层电子数是最内层电子数的3倍。下列说法正确的是( )
A. 原子半径:R<Y<Z
B. 简单气态氢化物的热稳定性:R>Y
C. R与Y只能形成一种化合物
D. 最高价氧化物对应水化物的酸性:Y>Z
难度: 中等查看答案及解析
-
黄铜矿(主要成分CuFeS2)是提取Cu的主要原料。已知:2CuFeS2+4O2
Cu2S+3SO2+2FeO(Ⅰ)产物Cu2S在1200 ℃高温下继续反应:2Cu2S+3O2
2Cu2O+2SO2 (Ⅱ)2Cu2O+Cu2S
6Cu +SO2↑ (Ⅲ)假定各步反应都完全。则下列说法正确的是
A. 由6molCuFeS2生成6molCu消耗O2的物质的量为15mol
B. 6molCuFeS2和14.25molO2反应,理论上可得到铜的物质的量为3mol
C. 反应Ⅰ中CuFeS2仅作还原剂
D. 取12.5g黄铜矿样品,经测定含3.60g硫,则矿样中CuFeS2质量分数一定为82.8%
难度: 困难查看答案及解析

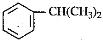 。
。