-
“柴、米、油、盐”是厨房常备用品其主要成分属于无机物的是
A. 柴(纤维素) B. 米(淀粉) C. 油(脂肪) D. 盐(氯化钠)
难度: 简单查看答案及解析
-
实验室取用药品的操作正确的是( )
A.
 滴加液体 B.
滴加液体 B.  倾倒液体
倾倒液体C.
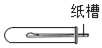 装入粉末状固体 D.
装入粉末状固体 D. 装入块状固体
难度: 简单查看答案及解析
-
如图为元素周期表的一部分(X元素信息不全).下列说法不正确的是( )
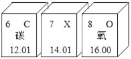
A. X用符号表示为N
B. 等质量的三种物质所含原子个数最多的是碳
C. 三种元素原子的核外电子层数不同
D. 质子数由小到大依次为C<X<O
难度: 中等查看答案及解析
-
和县城北20公里覆釜山下有一温泉,名“香淋泉”,也叫“太子汤”.泉水四季常温,可治皮肤病、关节炎等症.明代戏曲家汤显祖在《送客避和州》诗中写道:“晓色连古观,春香太子泉”.下列能解释“春香”的是( )
A. 分子的质量和体积都很小
B. 分子总是在不断运动着
C. 分子间是有间隔的
D. 分子是由原子构成的
难度: 简单查看答案及解析
-
如图所示,甲、乙、丙、丁、戊五种物质分别是铁、盐酸、氢氧化钙、硫酸铜、碳酸钠中的一种。连线两端的物质间能发生化学反应,甲与戊反应产生的气体能使澄清石灰水变浑浊,丙溶液为蓝色。下列能替代图中丁物质的是( )
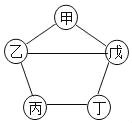
A. Ag B. BaCl2 C. CuO D. NaOH
难度: 中等查看答案及解析