-
某学习小组辨析以下说法:①粗盐和酸雨都是混合物;②非金属氧化物一定都是酸性氧化物;③冰和干冰既是纯净物又是化合物;④金属钠和镁的化学性质不同,主要是由于钠原子和镁原子的最外层电子数不同;⑤磷酸和醋酸都是多元酸;⑥纯碱和烧碱都是碱。说法正确的是 ( )
A. ②③④ B. ①②⑤ C. ③⑤⑥ D. ①③④
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. O和O2-都是氧元素,所以它们的化学性质相同
B. m g食盐和n g水充分振荡,形成的溶液的质量一定是(m+n)g
C. 化学式为AB型的离子化合物中,阴阳离子所带电荷的数值必然相等
D. 混合物一定是由多种元素组成的物质
难度: 中等查看答案及解析
-
某同学欲配制溶质质量分数为8%的食盐水80g,在用托盘天平称量食盐时,他把食盐和砝码的位置放颠倒了(1g以下用游码),那么实际上他所配制的食盐水的溶质质量分数为
A. 8.5% B. 7.5% C. 14% D. 7.1%
难度: 中等查看答案及解析
-
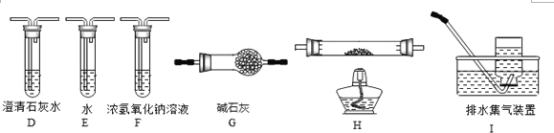
化学是一门以实验为基础的自然科学,用下列各装置或其组合能完成相应实验的是(已知实验室可用块状硫化亚铁(FeS)与稀硫酸反应制取硫化氢(H2S)气体)
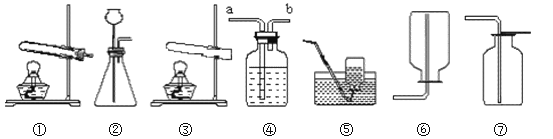
A. 装置②⑦可用于制取并收集干燥的CO2
B. 装置①⑤可用于制取并收集氧气
C. 装置②⑥可用于制取并收集硫化氢(H2S)气体
D. 装置④装满水后可以收集并储存氧气,需要氧气时可用水将装置中的氧气排出,水应从b端通入
难度: 中等查看答案及解析
-
根据下列叙述,对其“式”进行判断:①碱式磷酸钙的化学式为Ca4(OH)(PO4)3,②Fe3O4若看做“混合氧化物”时,可改写成FeO·Fe2O3,根据化合价规律和前述写法,则Pb3O4(四氧化三铅)可改写为2PbO·PbO2 (Pb的化合价为+2价、+4价),③为了方便某些化学计算质量分数为98%的浓H2SO4改写为9H2SO4·H2O。其中错误的是
A. 只有① B. 只有② C. ①③ D. ②③
难度: 中等查看答案及解析
-
下列有关化学知识的叙述I和II均正确并有因果关系的是( )
选项
叙述I
叙述II
A
KNO3的溶解度大
用蒸发结晶法除去KNO3中混有的NaCl
B
BaSO4难溶于酸
用盐酸和BaCl2溶液检验SO42-
C
在食物中可适量使用食品添加剂
食品添加剂都是用来增加食物的营养成分的
D
Ca(OH)2能制成澄清石灰水
可配制溶质质量分数为20﹪的Ca(OH)2溶液
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
现有Na2CO3和NaHCO3的混合物a克,下列实验方案不能测定混合物中Na2CO3质量分数的是 ( )
A. 与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
B. 充分加热,得b克固体
C. 与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
D. 与足量CaCl2溶液充分反应,过滤、洗涤、烘干,得b克固体
难度: 困难查看答案及解析
-
欲检验某混合气体中是否有CO2、H2O、CO有如下试剂:①灼热CuO②浓H2SO4③无水CuSO4④澄清石灰水⑤NaOH溶液则气体应依次通过( )
A. ③②④①④ B. ③④①④⑤ C. ③④⑤④②①④ D. ③④①④②
难度: 中等查看答案及解析
-
下列四个坐标图分别表示四个实验过程中某些量的变化,其中不正确的是( )
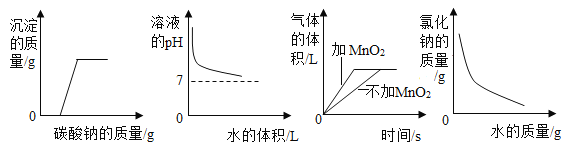
A. 向盐酸和氯化钙的混合溶液中加入碳酸钠 B. 向氢氧化钠溶液中加水
C. 双氧水分解 D. 向饱和氯化钠溶液中加水稀释
难度: 中等查看答案及解析
-
某有机物4.6g完全燃烧,需要消耗氧气9.6g,生成二氧化碳8.8g、水5.4g.则关于该有机物,下列说法正确的是( )
A. 只含有碳,氢元素 B. 只含有碳氢氧元素
C. 不能确定是否含氧元素 D. 不只含有碳氢氧元素
难度: 中等查看答案及解析