-
已知:C(s)+H2O(g)=CO(g)+H2(g) △H=a kJ/mol
C(s)+O2(g)=2CO(g) △H=-220 kJ/mol
H-H、O=O和O-H键的键能分别为436、496和462 kJ/mol,则a为
A. -332 B. -118 C. +350 D. +130
难度: 困难查看答案及解析
-
下列反应中,属于吸热反应同时又是氧化还原反应的是( )
A. Ba(OH)2·8H2O与NH4Cl反应 B. 铝与稀盐酸
C. 灼热的炭与水蒸气生成一氧化碳和氢气的反应 D. 铝热反应
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A. 钢铁的吸氧腐蚀和析氢腐蚀的负极反应均为:Fe-2e-=Fe2+
B. 钢铁发生吸氧腐蚀,正极的电极反应为:O2+4e-+2H2O=4OH-
C. 破损后的镀锌铁板比镀锡铁板更耐腐蚀
D. 用牺牲阳极的阴极保护法保护钢铁,钢铁作原电池的负极
难度: 简单查看答案及解析
-
在2A+B
3C+4D反应中,表示该反应速率最快的是( )
A. v(A)=0.5mol/(L·s) B. v(B)=0.3mol/(L·s)
C. v(C)=1.2mol/(L·min) D. v(D)=1mol/(L·s)
难度: 中等查看答案及解析
-
下列措施既能加快工业合成氨的速率,又能增大该反应的反应物转化率的是( )
A. 缩小容器容积 B. 移走 NH3
C. 提高反应温度 D. 使用催化剂
难度: 中等查看答案及解析
-
用惰性电极分别电解下列各物质水溶液一小段时间后,向剩余电解质溶液中加入适量水,能使溶液恢复到电解前浓度的是( )
A. AgNO3 B. Na2SO4 C. CuCl2 D. KI
难度: 困难查看答案及解析
-
下图所示各烧杯中均盛有海水,铁在其中被腐蚀最快和被保护最好的分别为( )
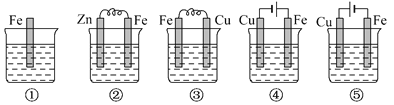
A. ①⑤ B. ③② C. ④⑤ D. ④①
难度: 困难查看答案及解析
-
下列有关电化学装置完全正确的是
A
B
C
D

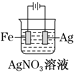
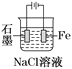
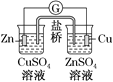
铜的精炼
铁上镀银
防止Fe被腐蚀
构成铜锌原电池
A. A B. B C. B D. D
难度: 中等查看答案及解析
-
已知①碳酸钙的分解CaCO3(s)=CaO(s)+CO2(g) ΔH 1 仅在高温下自发进行;②氯酸钾的分解 2KClO3 (s)=2KCl(s)+3O2(g) ΔH 2 , 在任何温度下都自发进行,下面有几组焓变数据,其中可能正确的是
A. ΔH 1 =+178.32 KJ.mol -1 ΔH 2 =-78.3 kJ·mol -1
B. ΔH 1 =-178.32 kJ.mol -1 ΔH 2 =+78.3 kJ·mol -1
C. ΔH 1 =-178.32 kJ.mol -1 ΔH 2 =-78.3 kJ·mol -1
D. ΔH 1 =+178.32 kJ.mol -1 ΔH 2 =+78.3 kJ·mol -1
难度: 中等查看答案及解析
-
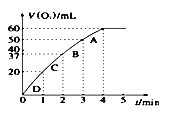
可逆反应A(g)+B(g)
C(g) +D(g)在反应过程中的能量变化如图所示,下列叙述不正确的是( )
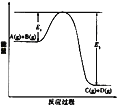
A. 该反应是放热反应
B. 向反应体系中加入催化剂对反应热无影响
C. 向反应体系中加入催化剂,E1减小,E2增大
D. 该反应ΔH=-(E2-E1)kJ·mol-1
难度: 中等查看答案及解析
-
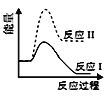
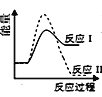
反应Ⅰ:CaSO4(s)+4CO(g)
CaS(s)+4CO2(g) ΔH1=-175.6 kJ·mol-1反应Ⅱ:CaSO4(s)+CO(g)
CaO(s)+SO2(g)+CO2(g) ΔH2=+218.4 kJ·mol-1假设某温度下,反应Ⅰ的速率(v1)小于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是( )
A.
 B.
B. 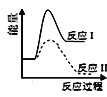
C.
 D.
D. 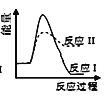
难度: 困难查看答案及解析
-
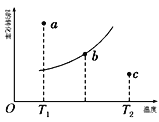
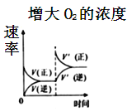
对可逆反应
,下列图象正确的是( )
A.
 B.
B. 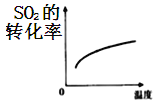
C.
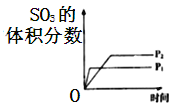 D.
D. 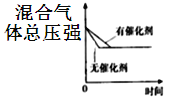
难度: 简单查看答案及解析
-
下列事实不能用化学平衡移动原理解释的是( )
A. 光照新制的氯水时,溶液的pH逐渐减小
B. 工业生产中,500℃左右比常温下更有利于合成氨
C. 反应 CO +NO2
CO2 +NO △H<0达平衡后,升高温度体系颜色变深
D. 增大压强,有利于SO2和O2反应生成SO3
难度: 中等查看答案及解析
-
可逆反应:2A(s)
B(g)+C(g),在一定条件下的刚性密闭容器中,起始时加入一定量的A,能判断反应达到平衡状态的有( )
①单位时间内生成2molA的同时生成1molB ②v (B): v (C)=1:1 ③密闭容器中混合气体的平均摩尔质量不变 ④混合气体的密度不再改变 ⑤B的体积分数不再改变 ⑥混合气体的压强不再改变
A. 3个 B. 4个 C. 5个 D. 6个
难度: 中等查看答案及解析
-
在一定温度下、1L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示,下列有关说法正确的是
x
y
w
n(起始)/mol
2
l
0
n(平衡)/mol
l
0.5
1.5
A. 该温度下,此反应的平衡常数表达式是
B. 升高温度,若w的体积分数减小,则此反应ΔH>0
C. 增大压强,正、逆反应速率均增大,平衡向正反应方向移动
D. 该温度下,再向容器中通入3molw,达到平衡时,n(x)=2mol
难度: 中等查看答案及解析
-
有关电化学知识的描述正确的是( )
A. 原电池的两极一定是由活动性不同的两种金属组成
B. 一般地说,能自发进行的氧化还原反应可设计成原电池
C. CaO+H2O=Ca(OH)2可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能
D. 某原电池反应为Cu+2AgNO3=Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液
难度: 中等查看答案及解析
-
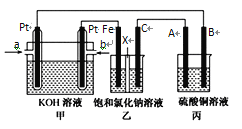
按下图装置实验,若x轴表示流出负极的电子的物质的量,则y轴应表示
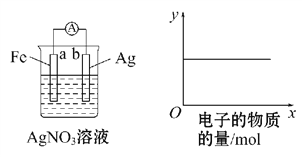
①c(Ag+) ②c(N
) ③a棒的质量 ④b棒的质量 ⑤溶液的质量
A. ①③ B. ③④ C. ①②④ D. ②
难度: 简单查看答案及解析
-
将Ba(OH)2、CuCl2、AgNO3、Na2SO4按物质的量比1∶1∶2∶1混合均匀,取一定量该混合物放入水中,充分振荡,插入惰性电极,通电一段时间后,下列说法中正确的是( )
①阴极、阳极所得的产物质量比为1∶8 ②通电过程中阳离子向阴极移动 ③阴极电极反应为Ag++e-=Ag ④电解过程中溶液pH升高
A. ①② B. ②③ C. ③④ D. ①④
难度: 困难查看答案及解析
-
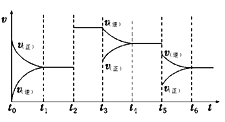
已知反应:2NO2(红棕色)
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
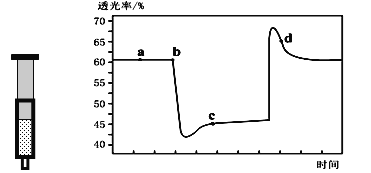
A. b点的操作是拉伸注射器
B. d点:v(正)< v(逆)
C. c点与a点相比,c(NO2)增大,c(N2O4)减小
D. 若不忽略体系温度变化,且没有能量损失,则T(b)>T(c)
难度: 中等查看答案及解析
-
某化工厂用石墨电解Na2CrO4溶液制备Na2Cr2O7的模拟装置如下图所示,下列有关说法错误的
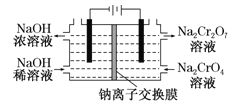
A. 溶液中OH-由阴极区流向阳极区
B. 阳极的电极反应式为2H2O-4e-=O2↑+4H+
C. 阳极区产生的气体与阴极区产生的气体在相同状况下体积之比为1∶2
D. Na2CrO4转化为Na2Cr2O7的离子方程式为2CrO42-+2H+=Cr2O72-+H2O
难度: 困难查看答案及解析
-
下列关于测定中和热的说法中正确的是( )
A. 实验中需要用到的主要玻璃仪器有:两只大小相同的烧杯、两只大小相同的量筒、温度计、环形玻璃搅拌棒
B. 可以用保温杯来代替烧杯做有关测定中和热的实验
C. 在测定中和热的实验中,至少需要测定并记录的温度是2次
D. 实验中若所使用的稀NaOH溶液的物质的量稍大于稀盐酸,则会导致所测得的中和热数值偏高
难度: 中等查看答案及解析
-
燃烧a g乙醇(液态),生成二氧化碳气体和液态水,放出的热量为Q kJ,经测定,a g乙醇与足量钠反应,能生成标准状况下的氢气5.6L,则表示乙醇燃烧热的热化学方程式书写正确的是( )
A. C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1) △H = -Q kJ/mol
B. C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1) △H = - Q / 2 kJ/mol
C. 1/2 C2H5OH(l)+3/2O2(g)=CO2(g)+3/2H2O(1) △H = -Q kJ/mol
D. C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1) △H = -2Q kJ/mol
难度: 中等查看答案及解析
-
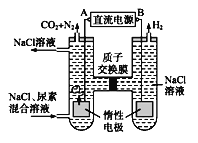
利用反应6NO2+8NH3===7N2+12H2O构成电池的装置如图所示。此方法既能实现有效清除氮氧化物的排放,减轻环境污染,又能充分利用化学能。下列说法正确的是
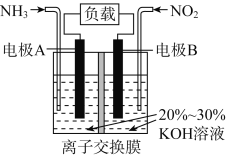
A. 电流从左侧电极经过负载后流向右侧电极
B. 为使电池持续放电,离子交换膜需选用阴离子交换膜
C. 电极A极反应式为2NH3-6e-===N2+6H+
D. 当有4.48 L NO2被处理时,转移电子数为0.8NA
难度: 困难查看答案及解析
-
下列说法或表示方法中正确的是( )
A. 一定条件下进行的化学反应,只能将化学能转化成光能或热能
B. 由C(金刚石)=C(石墨)ΔH=-1.9 kJ·mol-1 ,可知金刚石比石墨稳定
C. 在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧热的化学方程式为:2H2(g)+ O2(g) =2H2O(l) ΔH = -571.6 kJ·mol-1
D. 稀溶液中:H+(aq)+ OH-(aq)=H2O(l) ΔH= -57.3 kJ·mol-1 ,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于57.3KJ
难度: 中等查看答案及解析